Progredující demence s parkinsonizmem a poruchami chování – od prvních příznaků k neuropatologické diagnóze (kazuistika)
Progressive Dementia with Parkinsonism and Behavioral Changes – from the First Manifestations to the Neuropathological Confirmation (a Case Study)
We describe a case of a 69-year-old man with an atypical course of dementia with Parkinsonism and progressive severe behavioral abnormalities. Clinical presentation was compatible with dementia with Lewy bodies or frontotemporal dementia with Parkinsonism. The rapid and atypical progression was related to neuropathological findings of two co-morbid neurodegenerative entities. Fully developed dementia with Lewy bodies predominated, while markers of Alzheimer’s disease were also present in the brain tissue. However, their less expressed and more widespread distribution was probably related to the absence of clinical manifestations of progressive amnestic dementia, a typical symptom of Alzheimer’s disease. We retrospectively completed missing data and retraced the clinical course from the first disease manifestations to the definite neuropathological diagnosis.
Key words:
delirium – dementia with Lewy bodies –Alzheimer’s disease – frontotemporal dementia – differential diagnosis – parkinsonism
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
V. Franková 1; R. Matěj 2,3; R. Rusina 3,4
Působiště autorů:
Psychiatrická nemocnice v Dobřanech
1; Oddělení patologie a molekulární medicíny, Thomayerova nemocnice, Praha
2; Neurologická klinika a Centrum klinických neurověd 1. LF UK a VFN v Praze
3; Neurologické oddělení, Thomayerova nemocnice, Praha
4
Vyšlo v časopise:
Cesk Slov Neurol N 2015; 78/111(2): 209-214
Kategorie:
Kazuistika
doi:
https://doi.org/10.14735/amcsnn2015209
Souhrn
Prezentujeme kazuistiku 69letého muže s atypickým průběhem demence s parkinsonizmem a progredujícími závažnými poruchami chování. Klinický obraz evokoval demenci s Lewyho tělísky nebo frontotemporální demenci s parkinsonizmem. Poněkud atypický průběh a rychlý vývoj nemoci lze vysvětlit neuropatologickým nálezem komorbidity dvou neurodegenerativních entit. V popředí byla plně vyvinutá forma demence s Lewyho tělísky, v mozkové tkáni byly přítomny i markery Alzheimerovy nemoci, ale vyvinuty v menší míře a difúzněji. To mohlo korelovat s absencí klinické manifestace progresivní amnestické demence, která je pro Alzheimerovu nemoc typická. Post mortem se podařilo shromáždit dostatek informací a kompletně zmapovat průběh onemocnění od prvních příznaků až k definitivní neuropatologické diagnóze.
Klíčová slova:
delirium – demence s Lewyho tělísky – Alzheimerova nemoc – frontotemporální demence – diferenciální diagnostika – parkinsonizmus
Úvod
Demence postihují zhruba 5 % lidí nad 65 let a přes 30 % ve věkové skupině 80– 90 let. Příčinou více než poloviny všech případů je Alzheimerova nemoc. Dalšími častými etiologiemi je vaskulární demence, nemoc s Lewyho tělísky (asi 15– 25 % všech případů) a frontotemporální lobární degenerace (asi 10 % všech případů) [1]. Řada lékařů se nepouští do bližší specifikace demence; častým závěrem tak bývá Alzheimerova nemoc nebo vaskulární demence.
Klíčové v diferenciálně diagnostickém procesu je podrobné klinické vyšetření a zhodnocení objektivních anamnestických údajů. Přínosné mohou být zobrazovací metody strukturální i funkční a vyšetření mozkomíšního moku s detekcí hladin tau proteinu a beta amyloidu [2]. Tato vyšetření však nejsou v klinické praxi rutinně využívána. Je‑li provedena magnetická rezonance, pak zůstává mnohdy „neúplně“ popsána, např. chybí posouzení velikosti hipokampů nebo rozsahu vaskulárních lézí. Vyšetření likvoru se provádí pouze na specializovaných pracovištích [3]. Kvalitní neuropatologické vyšetření je post mortem provedeno jen u části pacientů, a chybí tak definitivní diagnóza a zpětná vazba pro klinické lékaře.
Rozlišení jednotlivých neurodegenerací je důležité nejen pro odhad dalšího průběhu onemocnění, ale i pro volbu terapie [1]. U Alzheimerovy nemoci, demence s Lewyho tělísky a demence u Parkinsonovy nemoci jsou standardní léčbou inhibitory cholinesteráz, které ale mohou zhoršovat chování u frontotemporální demence [4,5]. U demence s Lewyho tělísky a demence u Parkinsonovy nemoci je velké riziko závažných nežádoucích účinků při podávání antipsychotik, včetně atypických, jež jsou naopak mnohdy prospěšná v léčbě behaviorálních poruch u pokročilé Alzheimerovy nemoci [6,7]. U demence při Parkinsonově nemoci zůstává nadále nezbytným podávání levodopy, byť mnohdy bývá dostačující podstatně nižší dávka než v předchozím stadiu onemocnění. U demence s Lewyho tělísky může mít snížení dávky případně nasazené levodopy příznivý efekt na psychické symptomy bez zhoršení extrapyramidových příznaků [2,6].
Kazuistika
Popisujeme případ 69letého muže s progredující demencí, parkinsonizmem a závažnými poruchami chování.
Pacientův otec zemřel v 75 letech následkem demence s poruchami chování, agresivitou a halucinacemi, provázené třesem, ztuhlostí a zhoršenou hybností.
V osobní anamnéze měl pacient infarkt myokardu s aortokoronárním bypassem a hypertenzi. Dosáhl vysokoškolského vzdělání, aktivně sportoval, měl dvě zdravé děti.
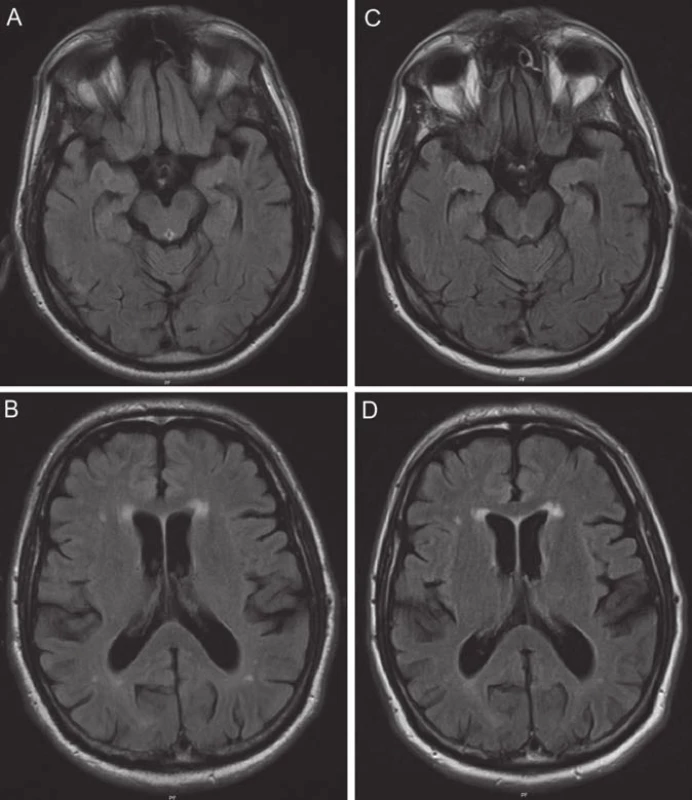
V r. 2004 (věk 61 let) se začalo postupně objevovat zpomalení a ztuhlost při chůzi a hraní tenisu, a pomalejší řeč. Neurologické vyšetření o dva roky později konstatovalo setřelou monotónní řeč, topornou pomalejší chůzi s omezením synkinéz horních končetin a axiální reflexy. Obraz byl uzavírán jako počínající Parkinsonova nemoc, nasazen byl selegilin 10 mg/ den, po dvou měsících byla přidána levodopa 150 mg/ den. Postupně se rozvinula úzkostná symptomatika, léčená přechodně alprazolamem. Magnetická rezonance (MR) mozku zobrazila mírnou atrofii v temporální a frontální oblasti (obr. 1A,B).
Psychologické vyšetření v r. 2006 prokázalo počínající deterioraci kognitivních funkcí s převažujícím postižením paměti, exekutivních funkcí, prostorového vnímání a porozumění sociálním situacím. Nápadné bylo zpomalení pracovního tempa a úzkostně‑depresivní ladění s obavami o zdraví, finanční zajištění, trvání vztahu atd., pochybnosti a nejistota v řešení běžných záležitostí. Pacient byl anosognostický, měl tendence bagatelizovat či disimulovat potíže. Syn referoval změnu osobnosti se sebestředností a lhostejností vůči potřebám a pocitům druhých.
V r. 2008 neurolog konstatoval stabilizaci stavu na kombinaci selegilinu a malých dávek levodopy, s mírným klidovým tremorem levé ruky. Rodina informovala, že v noci při spánku pacient několikrát napadl partnerku, poprvé již v r. 2004, tedy dva roky před zahájením antiparkinsonské léčby.
V r. 2009 se objevily partnerské problémy se strukturovanými emulačními bludy a hypersexualitou. Objektivně byl zjištěn kognitivní deficit – Mini Mental State Examination skór (MMSE) byl 19 bodů, skór revidované verze Addenbrookského kognitivního testu (ACE‑ R) byl 67 bodů. Pacient selhával zejm. v paměťových testech, dále byla přítomna akalkulie, v sémantické verbální fluenci řekl pouze šest slov, ve fonémické osm slov. Zrakově‑prostorové úkoly provedl správně. Diagnosticky byl stav zhodnocen jako demence u Parkinsonovy nemoci a byl nasazen rivastigmin s titrací do max. terapeutické dávky, pro popsanou paranoidní symptomatiku quetiapin 25 mg/ den, pro úzkostnou symptomatiku escitalopram 10 mg/ den. Kvůli zhoršování tremoru byla postupně navyšována levodopa na 750 mg/ den, byl vysazen selegilin.
Na kontrolní MR mozku v r. 2010 byla patrna jen mírná atrofie temporálně a frontálně bilaterálně bez výraznější progrese a nevýrazná mikroangiopatie (obr. 1 C,D).
V r. 2011 se objevil intermitentní třes celého těla, zejm. končetin, pocity vnitřního chvění. Pacient byl ale dál schopen hrát tenis a jezdit na kole, byť již s potížemi. Nápadné bylo kolísání kognitivního výkonu referované rodinou a objektivizované kognitivními testy prováděnými v intervalech jednoho až tří měsíců (MMSE 30...18...24 bodů).
Postupně se výrazně zhoršila motorika i míra soběstačnosti, pacient se stal zcela závislým na druhých, ztratil hygienické návyky i sociální kontrolu sfinkterů (vyměšoval na nevhodných místech). Začaly se objevovat stavy zmatenosti, bezradnost při běžných činnostech, halucinace postav a četné agresivní výpady vůči blízkým. Komunikace se stala obtížnější s projevy nonfluentní afázie. V tomto stadiu byla doporučena hospitalizace.
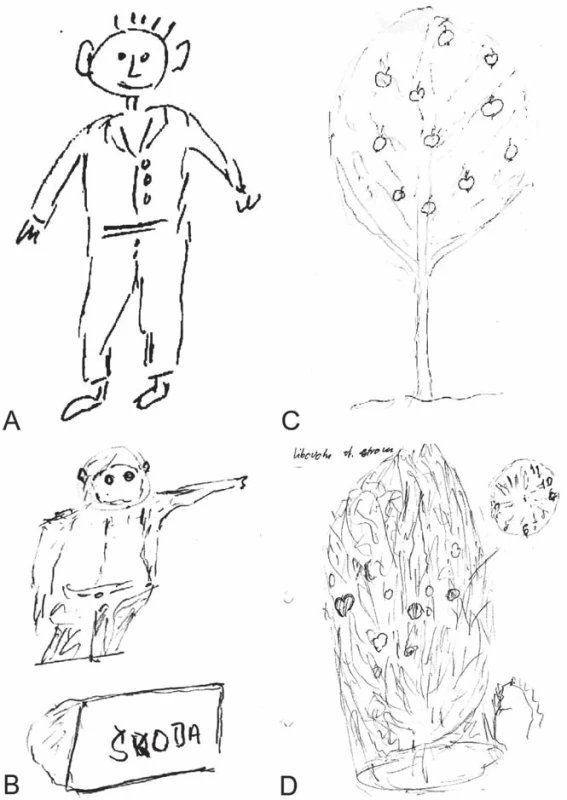
Při přijetí na gerontopsychiatrii měl pacient parkinsonské projevy akineto‑ rigidní s dyskinezami hlavně dolních končetin akrálně, místy i trupového svalstva. V MMSE měl 15 bodů, v testu hodin nedokázal zakreslit číslice ani ručičky. Při progresi onemocnění docházelo i k patrnému horšení schopnosti figurální kresby (obr. 2A– D). Během vyšetření uchopoval a zkoumal věci na stole. Projev byl špatně srozumitelný, zpomalený, s výrazně sníženou verbální fluencí a četnými sémantickými i fonémickými parafáziemi.
V průběhu hospitalizace se objevovaly poruchy chování s agresivitou, zmateností, strukturovanými halucinacemi: „Kdy už tam budeme?“, „To budeme spát v jednom kupé?“, „Budu mít přednášku?“, hledal „psy, co tu běželi“, slyšel neexistující zvonění. Byly přítomny misidentifikace („V televizi, ta žena...ona sem přijde...“) a další psychotické symptomy (na dece aktivně hledal „otvor“). Opakovaně v různých denních i nočních hodinách zaujímal „boxerské“ pozice, vymršťoval paže kolem sebe, vyhrožoval násilím. Několikrát se reálně pokusil napadnout personál. Stav v průběhu dne nápadně kolísal, jen místy ale splňoval kritéria pro delirium. Nasazení antipsychotik (quetiapin 25– 75 mg/ den, olanzapin 2,5– 5 mg/ den, tiaprid 100– 200 mg/ den) vedlo ke zhoršování extrapyramidové symptomatiky a horšení chůze bez celkového pozitivního vlivu na chování.
Rychle progredovala demence, dále se horšila řeč a objevil se těžký frontální syndrom, pacient nevěděl, co s oblečením, nebyl schopen se najíst, převracel lžíci v ruce. Nechápal, jak si má lehnout na lůžko, svlékal se a neovládal sfinktery. Bezradně hleděl na zvonící telefon, nevěděl, jak zvednout sluchátko. Jindy mluvil do sluchátka bez vytočení čísla.
Pro výrazné dyskineze byla postupně snížena dávka levodopy, poté vymizely mimovolní pohyby, aniž se zhoršila hybnost nebo třes. Vzhledem k těžké demenci se stavy agresivity byl postupně vysazen rivastigmin. Pacient se zklidnil, byl více odevzdaný, pasivní.
Poslední tři týdny života se horšila chůze, pacient se stal postupně imobilním. Při pokusu o navýšení dávky levodopy se objevovala deliria, hybnost nebyla zlepšena. Pacient odmítal péči, byl apatický. Po devíti týdnech hospitalizace zemřel na bronchopneumonii. Klinický vývoj je schematicky shrnut v časové ose (schéma 1).

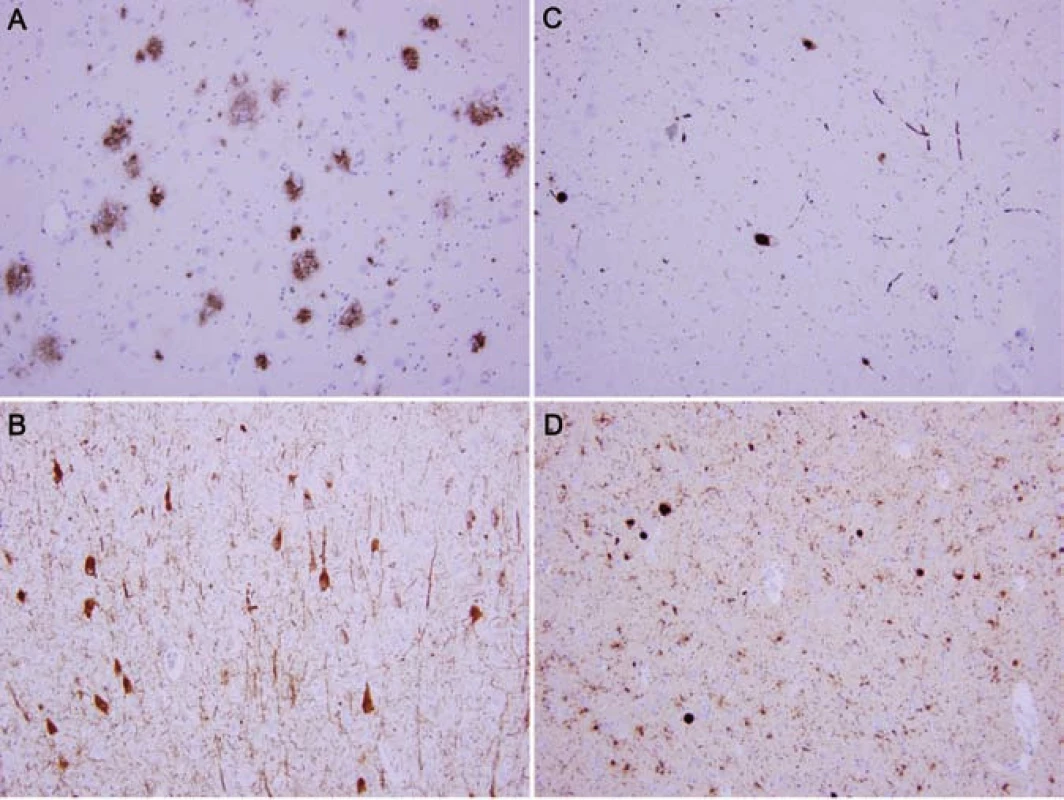
Při pitvě byla neuropatologickým a imunohistochemickým vyšetřením mozku nalezena kombinace dvou neurodegenerativních entit: Alzheimerova nemoc, pozdní varianta, limbické stadium vývoje v přechodu do neokortikálního (A2B2C2 dle NIA [8]) (obr. 3A,B) s mírnou amyloidovou angiopatií (CAA Vonsattel grade 1) a plně vyvinutá difúzní korová choroba s Lewyho tělísky v neokortikálním stupni (Braak 6, McKeith III [9]) (obr 3C,D). Změny asociované s Alzheimerovou nemocí jsou podle revidované „ABC“ klasifikace NIA v pásmu „intermediate“, nemoc s Lewyho tělísky je vyvinutá velmi výrazně – pásmo „high“ [10].
Diskuze
Naše kazuistika demonstruje rozvoj demence s parkinsonizmem a progredujícími závažnými poruchami chování u 69letého muže s neuropatologicky prokázanou komorbiditou dvou neurodegenerativních onemocnění, demence s Lewyho tělísky a Alzheimerovy nemoci.
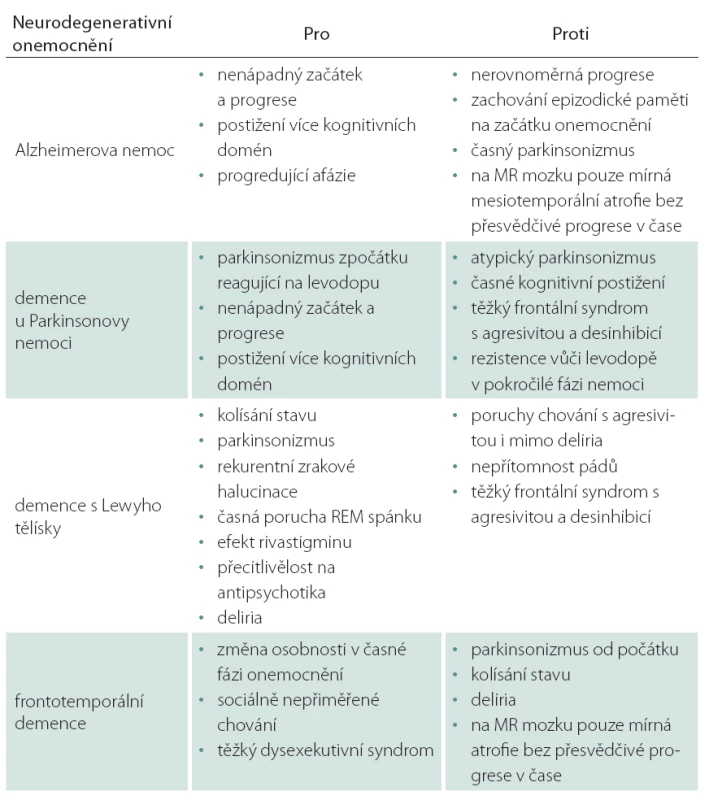
Při přijetí pacienta k hospitalizaci na gerontopsychiatrické oddělení byly zvažovány různé možné etiologie poruchy: frontotemporální lobární degenerace s parkinsonizmem, demence u Parkinsonovy nemoci, Alzheimerova nemoc a demence s Lewyho tělísky (tab. 1).
Po celou dobu psychiatrické ambulantní péče byl pacient veden s diagnózou demence u Parkinsonovy nemoci a adekvátně tomu léčen. Teprve v době hospitalizace byla tato diagnóza přehodnocena. Klinický obraz parkinsonizmu s částečnou odpovídavostí na dopaterapii byl již v časné fázi onemocnění provázen deteriorací kognitivních funkcí, v neuropsychologickém profilu převažovalo postižení frontálních a zrakově‑prostorových funkcí. Následně se rozvinulo velmi nápadné kolísání stavu, deliria a vizuální halucinace, zhoršení hybnosti s dalším horšením po nasazení antipsychotik. Obraz splňoval kritéria pro klinickou diagnózu demence s Lewyho tělísky (splněny tři „core“ podmínky a jedna „suggestive“) [6].
Diagnóza demence u Parkinsonovy nemoci se nabízela vzhledem ke klinicky zjevnému extrapyramidovému syndromu stabilizovanému na levodopě a uváděnému rozvoji demence až po několika letech trvání parkinsonské symptomatiky. Zhodnocení dostupných nálezů ale ukázalo, že psychologické vyšetření nalezlo projevy kognitivní deteriorace již velmi záhy, těžký frontální behaviorální syndrom s agresivitou a ztrátou zábran není typický pro demenci u Parkinsonovy nemoci a v terminální fázi onemocnění navíc navýšení levodopy i její následné vysazení nemělo vliv na motorické projevy.
Pro nejčastější příčinu demencí, Alzheimerovu nemoc, mohla svědčit postupná progrese kognitivního deficitu a generalizovanější kognitivní deficit při psychologickém vyšetření. Klinický obraz ale nebyl typický, chyběla časná porucha epizodické paměti, v popředí byly poruchy chování a hybnosti. Výrazná alterace zrakově‑prostorových funkcí a jen mírná atrofie meziotemporální krajiny na MR bez progrese v čase nejsou příznačné pro Alzheimerovu nemoc. Konstruktivní apraxie s progresí v čase (obr. 2) odpovídá výraznému postižení zrakově‑prostorových funkcí u demence s Lewyho tělísky ve srovnání s Alzheimerovu nemocí [11].
Pro možnost frontotemporální demence mohl svědčit obraz časných frontálních projevů: axiální jevy, kognitivní profil převážně dysexekutivního rázu, změna osobnosti s lhostejností vůči druhým, rozvoj psychotických příznaků s emulačními bludy a hypersexualitou a následně těžká frontální demence s progredující afázií, desinhibicí, agresivitou, úplnou ztrátou soběstačnosti a společenských zábran.
Demenci s Lewyho tělísky by od frontotemporální demence a Alzheimerovy nemoci mohl odlišit DaTSCAN (receptorové scintigrafické vyšetření prokazující ztráty funkčních zakončení presynaptických dopaminových neuronů ve striatu) [10], od kterého ale bylo upuštěno kvůli závažným psychiatrickým příznakům, nespolupráci nemocného a zhodnocení celkově velmi pokročilého stupně neurodegenerace. Limitující je rovněž absence vyšetření likvoru a MR volumometrie. Tato vyšetření mohou být přínosná pro diferenciální diagnostiku demencí, ale zatím nejsou v běžné ambulantní praxi prováděna [3].
Poněkud atypický klinický průběh a rychlý vývoj nemoci lze vysvětlit neuropatologickým nálezem komorbidity dvou neurodegenerativních entit. Plně vyvinutá forma demence s Lewyho tělísky byla v popředí, alzheimerovské změny byly v mozkové tkáni vyvinuty méně a difúzněji, což mohlo korelovat s absencí klinické manifestace progresivní amnestické demence i výrazné meziotemporální atrofie, které jsou pro Alzheimerovu nemoc typické.
Závěr
U našeho pacienta byly v neuropatologickém vyšetření nalezeny známky plně vyjádřené demence s Lewyho tělísky a zároveň i známky Alzheimerovy nemoci. Atypický obraz je tedy v našem případě důsledkem kombinace dvou neurodegenerativních jednotek. Případ popisovaného pacienta jednoznačně podtrhuje nutnost provádění detailního neuropatologického vyšetření mozku pacientů s atypickým průběhem neurodegenerativních onemocnění. Jen tak lze následnou klinicko‑patologickou korelací analyzovat vliv jednotlivých komorbidit na celkový průběh onemocnění a zohlednit možnost přítomnosti více neurodegenerativních entit u budoucích pacientů s potenciálními terapeutickými konsekvencemi.
Autoři děkují PhDr. P. Chodorové, MU Dr. J. Murgašové a MU Dr. P. Králíčkovi za poskytnutí dokumentace z ambulantní péče o pacienta a MU Dr. J. Kastnerovi z FN Plzeň za zapůjčení snímků magnetické rezonance. Autoři děkují rodině pacienta za souhlas s publikací této kazuistiky.
Podpořeno granty Univerzity Karlovy PRVOUK‑ P26/ LF1/ 4 a IGA MZ ČR NT13543- 4/ 2012 a IGA MZ NT 12094- 5/ 2011.
Přijato k recenzi: 4. 2. 2014
Přijato do tisku: 8. 1. 2015
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
doc. MUDr. Robert Rusina, Ph.D.
Neurologická klinika a Centrum klinických neurověd
1. LF UK a VFN v Praze
Kateřinská 30
120 00 Praha 2
e-mail: robert.rusina@lf1.cuni.cz
Zdroje
1. Aarsland D, Rongve A, Nore SP, Skogseth R, Skulstad S, Ehrt U et al. Frequency and case identification of dementia with Lewy bodies using the revised consensus criteria. Dement Geriatr Cogn Disord 2008; 26(5): 445– 452. doi: 10.1159/ 000165917.
2. Sorbi S, Hort J, Erkinjuntti T, Fladby T, Gainotti G, Gurvit H et al. EFNS‑ ENS Guidelines on the diagnosis and management of disorders associated with dementia. Eur J Neurol 2012; 19(9): 1159– 1179. doi: 10.1111/ j.1468‑ 1331.2012.03784.x.
3. Sheardová K, Hort J, Rektorová I, Rusina R. Dementia Diagnosis and Treatment in Czech Neurological and Psychiatric Practices. Cesk Slov Neurol N 2012; 75/ 108(2): 208– 211.
4. Franková V. Frontotemporální demence – kazuistiky z klinické praxe. Psychiatr Praxi 2004; 5(3): 146– 149.
5. Mendez MF, Shapira JS, McMurtray A, Licht E. Preliminary findings: behavioral worsening on donepezil in patients with frontotemporal dementia. Am J Geriatr Psychiatry 2007; 15(1): 84– 87.
6. McKeith IG, Dickson DW, Lowe J, Emre M, O’Brien JT, Feldman H et al. Diagnosis and management of dementia with Lewy bodies: third report of the DLB Consortium. Neurology 2005; 65(12): 1863– 1872.
7. Huang Y, Halliday G. Can we clinically diagnose dementia with Lewy bodies yet? Transl Neurodegener 2013; 2(1): 4– 12. doi: 10.1186/ 2047‑ 9158‑ 2‑ 4.
8. Montine TJ, Phelps CH, Beach TG, Bigio EH, Cairns NJ,Dickson DW et al. National Institute on Aging‑ Alzheimer‘s Association guidelines for the neuropathologic assessment of Alzheimer‘s disease: a practical approach. Acta Neuropathol 2012; 123(1): 1– 11. doi: 10.1007/ s00401‑ 011‑ 0910‑ 3.
9. Parkkinen L, Pirttilä T, Alafuzoff I. Applicability of current staging/ categorization of alpha‑ synuclein pathology and their clinical relevance. Acta Neuropathol 2008; 115(4): 399– 407. doi: 10.1007/ s00401‑ 008‑ 0346‑ 6.
10. Halliday GM, Holton JL, Revesz T, Dickson DW. Neuropathology underlying clinical variability in patients with synucleinopathies. Acta Neuropathol 2011; 122(2): 187– 204. doi: 10.1007/ s00401‑ 011‑ 0852‑ 9.
11. Mitolo M, Salmon DP, Gardini S, Galasko D., Enzo Grossi E,Caffarrac P. The new Qualitative Scoring MMSE Pentagon Test (QSPT) as a valid screening tool between autopsy‑ confirmed dementia with Lewy Bodies and Alzheimer’s disease. J Alz Dis 2014; 39(4): 823– 832. doi: 10.3233/ JAD‑ 131403.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2015 Číslo 2
Nejčtenější v tomto čísle
- Agresivní hemangiom obratle
- Neuromyelitis optica
- Kongenitální centrální hypoventilační syndrom (Ondinina kletba)
- Radiologické hodnocení lumbální spinální stenózy a jeho klinická korelace
