Elektrostimulace suprahyoidních svalů u pacientů po cévní mozkové příhodě s dysfagií
Electrical Stimulation of the Suprahyoid Muscles in Post Stroke Patients with Dysphagia
Aim:
Dysphagia is a risk for complications (an aspiration and a malnutrition) and therefore it is necessary to treat it. The aim of the study was to assess the changes of swallowing in patients after stroke with dysphagia after four weeks of orofacial rehabilitation with or without electrostimulation of the suprahyoid muscles.
Methods:
A prospective study of patients in the early phase post stroke with dysphagia was done from 1/2015 to 12/2016. In the experimental group of 54 patients (26 men, average age 70 years) was performed electrostimulation of the suprahyoid muscles 20 min a day, 5 days per week. In the control group of 54 patients (31 men, average age 69 years) was performed the standard orofacial rehabilitation without electrostimulation. Dysphagia was assessed at the beginning and in the end of orofacial therapy using clinical tests: The Gugging Swallowing Screen (GUSS) and Functional oral intake scale (FOIS).
Results:
The difference of the change in score between the GUSS experimental group (mean 5.77 ± 0.45; median 6) and the control group (mean 4.03 ± 0.57; median 4) was statistically significant (p = 0.0198). The difference of change in the FOIS test between the experimental group (mean 1.87 ± 0.22; median 2) and the control group (mean 1.01 ± 0.31; median 1) was statistically significant (p = 0.0013).
Conclusion:
Electrical stimulation of the suprahyoid muscles improves swallowing in dysphagia patients post stroke.
Key words:
stroke – dysphagia – electrical stimulation – suprahyoid muscles
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Chinese summary - 摘要
中风后吞咽障碍患者的舌骨肌电刺激目标:
吞咽障碍是误吸和营养不良并发症风险因素之一,因此有必要对其进行治疗。本研究旨在评估伴有吞咽障碍的中风患者使用或不使用舌骨肌电刺激口面康复治疗4周后的吞咽变化情况。
方法:
在2015年1月至2016年12月期间,对伴有吞咽障碍的中风早期患者进行了前瞻性研究。 在54名患者(26名男性,平均年龄70岁)的实验组中,实施每周5天,每天20分钟的舌骨肌电刺激治疗。在对照组54例患者(男31例,平均年龄69岁)中,进行标准口面康复治疗,无电刺激。在口面康复治疗开始和结束时,使用临床测试(Gugging吞咽屏幕(GUSS)和功能口服摄入量表(FOIS))评估患者的吞咽障碍情况。
结果:
GUSS实验组(均值5.77±0.45;中位数6)和对照组(均值4.03±0.57;中位数4)之间的得分变化具有显著性差异(p=0.0198)。实验组(均值1.87±0.22;中位数2)与对照组(均值1.01±0.31;中位数1)相比,FOIS检验变化的差异具有统计学显著性(p = 0.0013)。
结论:
舌骨肌电刺激可改善中风后吞咽障碍患者的吞咽状况。
关键词:
中风 - 吞咽障碍 - 电刺激 - 舌骨肌
Autoři:
P. Konečný 1–4; M. Elfmark 2; M. Rosolová 1; P. Bastlová 2; I. Lerchová 2; A. Můčková 2
Působiště autorů:
Rehabilitace NMB Brno a CLR nemocnice SMN Prostějov
1; Ústav fyzioterapie, FZV UP v Olomouci
2; Katedra fyzioterapie a rehabilitace, LF MU, Brno
3; Neurologická klinika LF UP a FN Olomouc
4
Vyšlo v časopise:
Cesk Slov Neurol N 2017; 80/113(5): 578-581
Kategorie:
Původní práce
doi:
https://doi.org/10.14735/amcsnn2017578
Souhrn
Cíl:
Dysfagie je riziková pro své komplikace (aspirace a malnutrice) a proto je nutné ji léčit. Práce hodnotila změny polykání pacientů v časné fázi po cévní mozkové příhodě s dysfagií po 4týdenní orofaciální rehabilitaci s elektrostimulací suprahyoidních svalů nebo bez ní.
Soubor a metodika:
Prospektivní studie byla prováděna od 1/2015 do 12/2016. V experimentálním souboru 54 pacientů (26 mužů, průměrný věk 70 let) probíhala elektrostimulace suprahyoidních svalů 20 min denně, 5 dní v týdnu. V kontrolním souboru 54 pacientů (31 mužů, průměrný věk 69 let) byla prováděna standardní orofaciální rehabilitace bez elektrostimulace. Dysfagie byla hodnocena na začátku a na konci terapie pomocí klinických testů: test hodnotící schopnost polykání (The Gugging Swallowing Screen; GUSS) a podle funkční škály příjmu potravy (Functional Oral Intake Scale; FIOS).
Výsledky:
Rozdíl změn v GUSS skóre mezi experimentální skupinou (průměr 5,77 ± 0,45; medián 6) a kontrolní skupinou (průměr 4,03 ± 0,57; medián 4) byl statisticky významný (p = 0,0198). Rozdíl změn v testu FOIS mezi experimentální skupinou (průměr 1,87 ± 0,22; medián 2) a kontrolní skupinou (průměr 1,01 ± 0,31; medián 1) byl statisticky významný (p = 0,0013).
Závěr:
Elektrostimulace suprahyoidních svalů zlepšuje polykání u dysfagických pacientů po cévní mozkové příhodě.
Klíčová slova:
cévní mozková příhoda – dysfagie – elektrostimulace – suprahyoidní svaly
Úvod
Dysfagie po cévní mozkové příhodě (CMP) se projevuje obtížným nebo až nemožným polykáním potravy. Incidence dysfagie u pacientů po CMP je 20– 65 % [1,2]. K diagnostice a terapii dysfagie je nutný komplexní interdisciplinární přístup v rámci dysfagiologického týmu [3]. Při hodnocení poruch polykání používáme mezinárodní klinické dotazníky. V České republice je nově používán test hodnotící schopnost polykání (The Gugging Swallowing Screen; GUSS) a klinický dotazník pro dysfagie, tzv. funkční škála příjmu potravy (Functional Oral Intake Scale; FOIS).
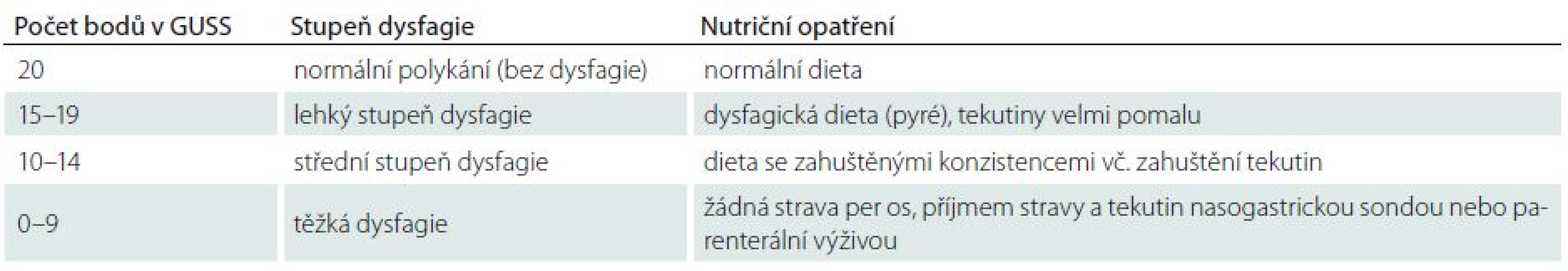
GUSS test je screeningové vyšetření schopnosti polykání a je určeno pro pacienty po CMP v akutní fázi onemocnění. Cílem vyšetření je kvantitativní a kvalitativní zhodnocení schopnosti polykání a určení rizika aspirace potravy. Na základě standardizovaného testování a vyplnění klinického formuláře se zhodnotí polykání zahuštěné tekutiny, vody a tuhé stravy, dále pak výskyt kašle, změna hlasu po polknutí a tzv. drooling (vytékání slin, event. potravy z úst). Testem stanovujeme celkové skóre 0 (nejhorší) až 20 (nejlepší) a stupeň dysfagie s tíží rizika aspirace potravy. Na základě výsledku vyšetření GUSS se doporučuje vhodný typ (konzistence) stravy, možnosti hydratace, způsob podávání potravy a zahájení včasného logopedicko-rehabilitačního terapeutického postupu (tab. 1) [3–5].
FOIS hodnotí schopnost polykání potravy. Je založen na klinickém hodnocení schopnosti pacienta přijmout potravu podle různé konzistence a podle nutného času pro tento příjem. Na základě tohoto zhodnocení se rozlišuje 7 stupňů od patologického nepříjmu jakékoli potravy (1 – nejhorší stupeň) až po normální příjem per os (7 – nejlepší stupeň) [6].
Podle příčin a klinického nálezu dysfagie používáme v léčbě poruch příjmu potravy kompenzační a terapeutické strategie. Při kompenzační strategii se snažíme zajistit příjem potravy nebo zlepšit polykání. Používáme k tomu různé náhradní způsoby výživy (nazogastrická sonda – NG, perkutánní endoskopická gastrostomie – PEG nebo parenterální intravenózní výživa), úpravy konzistence a výběr vhodné potravy. Při terapeutické strategii procvičujeme orofaciální motoriku a polykací manévr pomocí terapeutických cvičení, což je vlastní orofaciální rehabilitace (OFR) [7–10].
V terapii poruch polykání je prováděná OFR společně s logopedickou stimulační terapií, která má vliv nejen na obnovu příjmu potravy, ale i na další orofaciální funkce (mimiku, řeč), na celkový zdravotní stav a na kvalitu života [10,11]. K obnově funkce polykacích svalů je nově doporučována elektromyostimulace (ES) hyoidních svalů. V současné době se doporučuje stimulace infrahyoidních i suprahyoidních svalů [12,13]. V klinické praxi není ES běžně užívaná terapeutická metoda u dysfagických pacientů po CMP. K zlepšení elevace laryngu, uzavření dýchacích cest, a tím zabránění aspirace potravy je vhodnější stimulovat suprahyoidní svaly s doporučenými parametry stimulačních pravoúhlých proudů o frekvenci 60 Hz, délky impulsu 300 mikrosekund a intenzity nad prahově motorické [12–15].
Cílem naší prospektivní studie bylo porovnat změny polykání dysfagických pacientů po CMP pomocí GUSS a FOIS, po 4 týdny probíhající OFR s ES suprahyoidních svalů oproti kontrolní skupině se standardní 4týdenní OFR bez ES.
Soubor a metodika
Indikací zařazení do studie byla porucha polykání (pozitivní GUSS test) v časné fázi po CMP (1– 4 týden po vzniku CMP) a schopnost aktivní spolupráce. Všichni pacienti podepsali informovaný souhlas a studie byla provedena v souladu s etickými principy Helsinské deklarace klinického výzkumu.
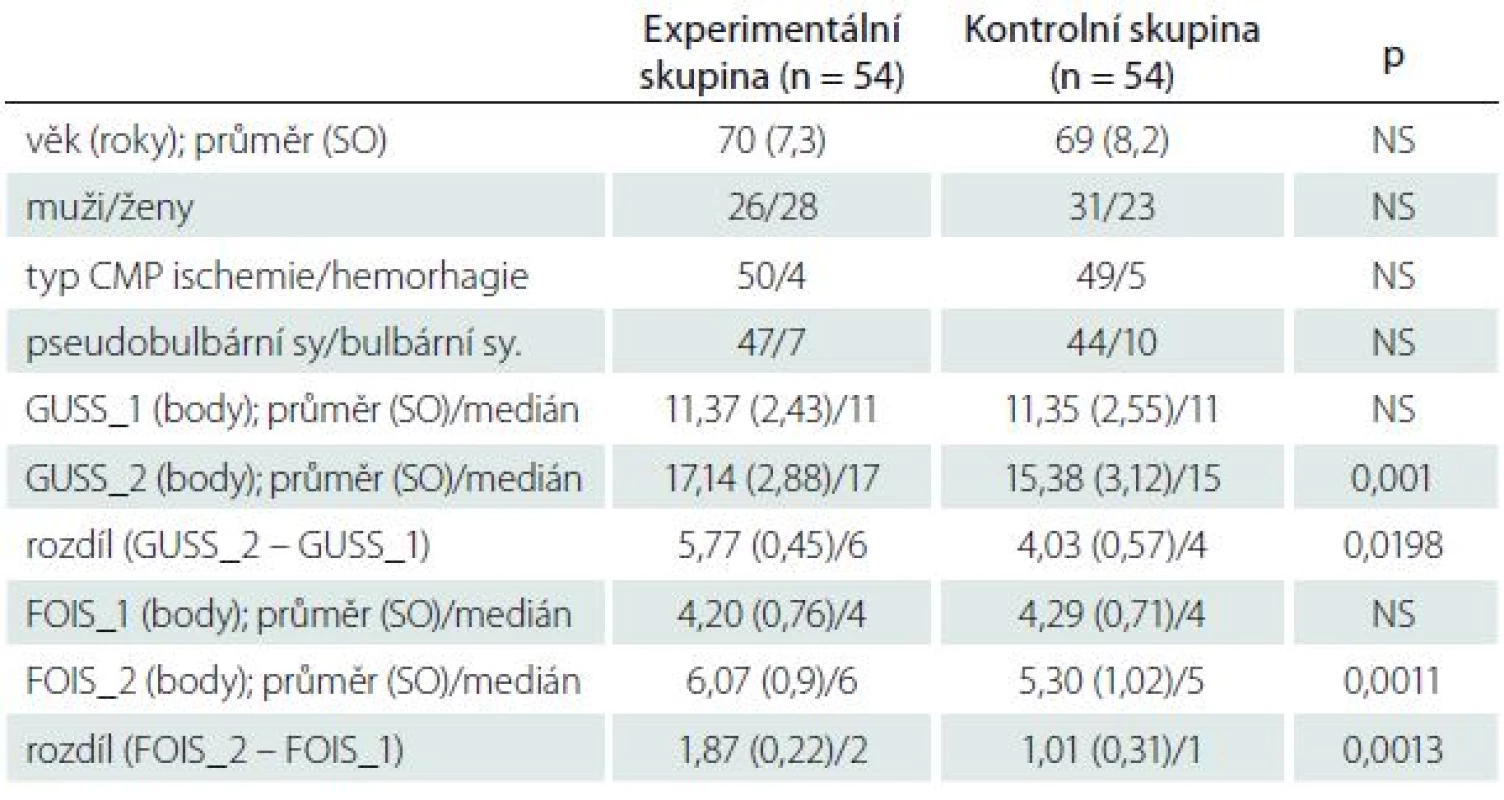
Experimentální soubor tvořilo 54 pacientů, z toho 28 žen a 26 mužů, průměrný věk 70 let. Ischemických CMP bylo 50 (92 %) případů a hemoragické CMP byly 4 (8 %) případy. Postižení kmene mozku s bulbární symptomatikou bylo 7 (13 %) případů, postižení v oblasti kortikálně-subkortikální s pseudobulbárním syndromem se vyskytovalo u 47 (87 %) nemocných. Kontrolní soubor tvořilo 54 pacientů – 23 žen a 31 mužů, průměrný věk 69 let. V tomto souboru bylo 49 (90,5 %) ischemických postižení a 5 (9,5 %) hemoragických postižení, 10 (18 %) pacientů mělo bulbární syndrom při postižení mozkového kmene a 44 (82 %) pacientů mělo pseudobulbární syndrom při kortiko-subkortikální mozkové lézi (tab. 1).
Vyšetření polykacích funkcí proběhlo pomocí klinického vyšetření polykání podle GUSS a FOIS. Hodnocení pacientů bylo provedeno na začátku rehabilitace (před OFR) a po 4 týdnech (po OFR) za hospitalizace na rehabilitačním oddělení NMB Brno a CLR nemocnice Prostějov. Studie byla provedena v období 1/2015 až 12/2016.
Cílená OFR probíhala v obou skupinách 1× denně 30 min, 5 dní v týdnu a zahrnovala tři základní fáze.
1. Přípravná fáze: posturální terapii a dechovou rehabilitaci s nácvikem uzavření hrtanové úžiny. 2. fáze: nácvik polykání „nasucho“, cvičení orální fáze a cvičení hltanové fáze s posílení hlasivkového uzávěru. 3. fáze: přímá rehabilitace polykání, která zahrnuje nácvik polykání s použitím různé konzistence potravy a tekutin, aktivace propulzní síly (tlak jazyka se soustem na patro), nácvik supraglotického polykání a event. nácvik kompenzační strategie polykání pomocí řízené polohy hlavy (otočení, předklon) [16,17].
V experimentální skupině navíc probíhala ES suprahyoidních svalů pomocí transkutánní elektro-neuro stimulace (VocaSTIM) s frekvencí 60 Hz, intenzitou nad prahově motorickou, 20 min denně, 5 dní v týdnu. ES suprahyoidních svalů a 1. fázi OFR prováděl fyzioterapeut a funkční terapii polykání (2. a 3. fázi OFR) prováděl klinický logoped.
Klinické hodnocení a vyplnění klinických formulářů (testování podle GUSS a FOIS) prováděly zaučené zdravotní sestry se supervizí klinického logopeda a ošetřujícího lékaře obeznámeného s problematikou hodnocení dysfagií. Zhodnocení výsledků dělal nezávisle (zaslepeně) statistik. Naměřené hodnoty a změny před terapií a po ní byly statisticky zpracovány a vyhodnoceny pomocí ANOVA testu (analýza rozptylu opakovaných měření) na hladině statistické významnosti p < 0,05.
Výsledky
Po čtyřtýdenní komplexní OFR bylo celkem bylo zhodnoceno 108 pacientů po CMP s dysfagickými potížemi. V experimentální skupině 54 pacientů s OFR a ES suprahyoidních svalů nacházíme statisticky významné změny v kvalitě i kvantitě polykání při hodnocení GUSS testem (p = 0,001) a FOIS testem (p = 0,0011). V kontrolní skupině zjišťujeme po terapii OFR podobně signifikantní změny v zlepšení polykání při hodnocení testy GUSS (p = 0,034) a FOIS (p = 0,044). Při zhodnocení rozdílů hodnot skóre testů před terapií a po ní mezi experimentální a kontrolní skupinou nacházíme statisticky významné změny s hodnotou p = 0,0198 pro test GUSS (tab. 2, graf 1) a s hodnotou p = 0,0013 pro test FOIS (tab. 2, graf 2).


Diskuze
Signifikantní změny hodnot rozdílů před terapií a po ní mezi experimentální a kontrolní skupinou naměřených pomocí klinických testů GUSS a FOIS nám přináší pozitivní důkaz o efektivnosti ES suprahyoidních svalů při cílené OFR dysfagií po CMP. Zvláště důležité a názorné jsou hodnoty skóre testu GUSS (tab. 2, graf 1). V naší studii jsou popsány změny ze skupiny středního stupně dysfagie s vysokým rizikem aspirace potravy (GUSS medián: 11) do skupiny lehkého stupně dysfagie s nízkým rizikem aspirace (GUSS medián 17 u skupiny s ES oproti GUSS skore 15 v kontrolní skupině). Tyto změny korelují i s úpravou klinického stavu – příjmu potravy, vyjádřené testem FOIS. Vstupně průměrně dominovala dysfagie stupně č. 4 podle FOIS, tzn. příjem jen kašovité stravy. Po 4týdenní terapii jsme nacházeli zlepšení příjmu potravy, a to v kontrolní skupině, kde se vyskytoval průměrně stupeň č. 5 podle FOIS (příjem mleté nebo tužší stravy), a též v experimentální skupině, kde se průměrně vyskytoval stupeň č. 6, tedy samostatné polykání všech konzistencí potravy, ovšem s delší dobou nutnou pro příjem potravy (tab. 2, graf 2).
Význam orofaciální rehabilitace u pacientů po CMP s dysfagií byl potvrzen v práci Hägga a Larsonna, kteří ve své prospektivní klinické studii po 6měsíční orofaciální regulační terapii hodnocené podle klinického testu FOIS vyšetřením prokázali jednoznačně signifikantní terapeutický efekt [18]. Podobnou standardní terapii OFR a testy FOIS jsme používali i v naší studii. Rozdílné názory panují na použití neuromuskulární ES hyoidních svalů při terapii dysfagií. Ve studii Permsirivanicha et al byl srovnáván efekt 4týdenní orální regulační rehabilitační terapie (u 11 pacientů s dysfagií po CMP) proti ES (12 pacientů s dysfagií po CMP). V obou skupinách došlo ke zlepšení příjmu potravy (hodnoceno podle FOIS). Lepší výsledky však byly popsány ve skupině s ES [19]. Podobně další studie podle autorů Ludlow et al [14] používající ES hyoidních svalů přináší pozitivní a dlouhodobé výsledky ve zlepšení polykání. Naopak studie Powera et al neprokázala jednoznačný přínos ES. Po hodinové ES faryngeálních svalů prováděné denně během jedno měsíční rehabilitace nebyla pozorována významná signifikantní funkční ani neurofyziologická změna u dysfagických pacientů po CMP oproti kontrolní konvenční rehabilitaci dysfagií [20].
Studie Powera et al probíhala na relativně malém vzorku 16 pacientů (8 experimentálních a 8 kontrolních probandů) a byly srovnávány výsledky stimulací pomocí frekvence 0,2 Hz. V naší studii jsme používali ES suprahyoidních svalů, ale frekvencí 60 Hz. Podobnou ES suprahyoidních svalů u dysfagických pacientů po lézi v CNS používali ve své studii Beom et al. V této studii byly u 7 exponovaných probandů oproti 21 kontrolním probandům pozorovány pozitivní klinické změny ve zlepšení polykání, avšak statisticky nevýznamné. Tato statistická nevýznamnost byla dána relativně malým počtem probandů v dané studii [13].
Závěr
V naší studii byl pozorován klinický i statisticky signifikantní pozitivní efekt ES terapie. Po 4týdenní OFR s důrazem na ES suprahyoidních svalů došlo ke zlepšení polykání potravy u dysfagických pacientů po CMP. ES ve spojení s OFR je spolehlivá účinná metoda s minimem kontraindikací a nežádoucích účinků při obnově funkce polykání.
Terapie dysfagie po CMP je důležitá z hlediska obnovy fyziologického příjmu potravy a tekutin, a tím zlepšením základních životních funkcí (nutrice a hydratace), kvality života, snížení morbidity a mortality.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Petr Konečný, Ph.D., MBA
Neurologická klinika LF UP a FN Olomouc
I. P. Pavlova 185/6
779 00 Olomouc
e-mail: dr.petr.konecny@gmail.com
Přijato k recenzi: 4. 7. 2017
Zdroje
1. Herzig R, Vlachová I. Cévní onemocnění mozku a míchy. In: Kaňovský P, Herzig R, et al. Speciální neurologie. Olomouc: Univerzita Palackého 2007:7– 36.
2. Martino R, Foley N, Bhogal S, et al. Dysphagia after stroke. Stroke 2005;36:2756– 63. doi: 10.1161/ 01.STR.0000190056.76543.eb.
3. Václavík D, Solná G, Lasotová N, et al. Péče o pacienty s dysfagií po cévnímozkové příhodě. Cesk Slov Neurol N 2015;78/ 111(6):721– 27. doi: 10.14735/ amcsnn2015721.
4. Lasotová N, Bednařík J. Koncept péče o neurogenní dysfagie. [cit. 22. 2.2017]. Dostupné z URL: http://www.fnbrno.cz/nemocnice-bohunice/neurologicka-klinika/koncept-pece-o-neurogenni-dysfagie/t4942.
5. Trapl M, Enderle P,Nowotny M, et al. Dysphagia bedside screening for acute stroke patients: The gugging swallowing screen. Stroke 2007;38(11):2948– 52. doi: 10.1161/ STROKEAHA.107.483933.
6. Crary MA, Carnaby-Mann GD, Groher ME. Initial psychometric assessment of a functional oral intake scale for dysphagia in stroke patients. Arch Phys Med Rehabil 2005;86:1516– 20. doi: 10.1016/ j.apmr.2004.11.049.
7. Castillo Morales R. Die Orofaziale Regulationstherapie. Munchen, Berlin, Heidelberg: Pflaum 1998.
8. Gangale DC. Rehabilitace orofaciální oblasti. Praha: Grada Publishing 2004.
9. Kittel A. Myofunkční terapie. Praha: Grada Publishing 1999.
10. Tedla M, et al. Poruchy polykání. Halvíčkův Brod: Tobiáš 2009.
11. Konecny P, Elfmark M, Urbanek K. Facial paresis after stroke and its impact on patients’ facial movement and mental status. J Rehabil Med 2011;43(1):73– 5. doi: 10.2340/ 16501977-0645.
12. Freed ML, Freed L, Chatburn RL, et al. Eletrical stimulation for swallowing disorders caused by stroke. Respir Care 2001;46(5):466– 74.
13. Beom J, Kim JS, Han RT. Eletrical stimulation of suprahyoid muscules in brain-injured patienst with dysphagia. Ann Rehabil Med 2011;35:322– 27. doi: 10.5535/ arm.2011.35.3.322.
14. Ludlow CL, Humbert IA, Saxon K, et al. Effects of surface electrical stimulation both at rest and during swallowing in chornic pharyngeal dysphagia. Dysphagia 2007;22:1– 10. doi: 10.1007/ s00455-006-9029-4.
15. Humbert IA, Michou E, MacRae PR, et al. Electrical stimulation and swallowing. How much dowe know? Semin Speech Lang 2012;33(3):203– 16. doi: 10.1055/ s-0032-1320040.
16. Konecny P, Elfmark M, Bastlova P, et al. New orofacial physiotherapy of dysphagia after stroke. Int J Phys Med Rehabil 2017;5(3):406. doi: 10.4172/ 2329-9096.1000406.
17. Konečný P, Elfmark M, Horák S, et al. Dysfagie po cévní mozkové příhodě. Rehabil Fyz Lék 2015;22(4):181– 84.
18. Hägg M, Larsson B. Effects of motor and sensory stimulation in stroke patiens with long-lasting dysphagia. Dysphagia 2004;19(4):219– 30.
19. Permsirivanich W, Tipchatyotin S, Wongchai M, et al. Comparing the effects of rehabilitation swallowing therapy vs. neuromuscular electrical stimulation therapy among stroke patients with persistent pharyngeal dysphagia: a randomized controlled study. J Med Assoc Thai 2009;92(2):259– 65.
20. Power ML, Fraser CH, Hobsaon A, et al. Evaluating oral stimulation as a treatment for dysphagia afterstroke. Dysphagia 2006;21(1):49– 55. doi: 10.1007/ s00455-005-9009-0.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2017 Číslo 5
Nejčtenější v tomto čísle
- Esenciální tremor – vzniká nový nozologický koncept?
- Leberova hereditární neuropatie optiku
- Statiny indukovaná nekrotizující autoimunitní myopatie
- Terapia pokročilých štádií Parkinsonovej choroby invazívnymi postupmi
