Validace české verze Neuropathic Pain Symptom Inventory (NPSIcz)
Validation of the Czech Version of the Neuropathic Pain Symptom Inventory (NPSIcz)
Introduction:
Simple questionnaires based on so called “neuropathic pain descriptors” are the most frequently used screening tools in the diagnosis of neuropathic pain, especially by non‑specialists. However, no validated Czech version of any of the internationally accepted nueropathic pain questionnaires is available.
Aim:
The aim of this study was to develop and validate a Czech version of the Neuropathic Pain Symptom Inventory (NPSI), a questionnaire that allows the user to characterize subtypes of neuropathic pain, is sensitive to change, and has discriminatory power.
Patients and methods:
The NPSI was translated into the NPSIcz using the forward‑ backward translation method and validated in a group of patients suffering from neuropathic pain of peripheral (n = 66) or central origin (n = 30) due to polyneuropathy or multiple sclerosis, and in a group of individuals suffering from nociceptive pain (due to severe osteoarthritis of the knee or hip joint; n = 70). The NPSIcz was repeated within three hours in 19 individuals to determine test‑ retest reliability.
Results:
The NPSIcz showed good diagnostic validity in discriminating between patients with neuropathic and nociceptive pain (p < 0.001) but low ability to discriminate between patients with central and peripheral neuropathic pain (p > 0.05). Repeated administration confirmed acceptable test‑ retest reliability (intra‑ class correlation coefficient of 0.86 for the NPSIcz sum score). Cluster analysis identified six different pain profiles.
Conclusions:
The NPSIcz is able to discriminate between neuropathic and nociceptive pain, to identify different pain profiles, and has acceptable test‑ retest reliability. It can, therefore, be recommended as an easy‑ to‑ administer questionnaire suitable for the diagnosis of neuropathic pain, including long‑term follow up.
Key words:
neuropathic pain – nociceptive pain – pain measurement – questionnaire – polyneuropathy – multiple sclerosis – osteoarthritis
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
I. Šrotová 1,2; E. Vlčková 1,2; J. Straková 1; S. Kincová 1,2; L. Ryba 3; L. Dušek 4; B. Adamová 1,2; J. Bednařík 1,2
Působiště autorů:
Neurologická klinika LF MU a FN Brno
1; CEITEC – Středoevropský technologický institut MU Brno
2; Ortopedická klinika LF MU a FN Brno
3; Institut biostatistiky a analýz MU, Brno
4
Vyšlo v časopise:
Cesk Slov Neurol N 2015; 78/111(1): 45-56
Kategorie:
Původní práce
Souhrn
Úvod:
Důležitou součástí diagnostického algoritmu neuropatické bolesti jsou jednoduché dotazníkové nástroje založené na přítomnosti typických popisných charakteristik (tzv. deskriptorů). V českém jazykovém prostředí však není k dispozici validovaná verze žádného z mezinárodně akceptovaných dotazníků.
Cíl:
Cílem práce bylo vytvoření české jazykové verze jednoho z nejpoužívanějších dotazníků zaměřených na diagnostiku neuropatické bolesti a charakteristiku jednotlivých jejích subtypů, a to tzv. NPSI (Neuropathic Pain Symptom Inventory) a její validace.
Soubory a metodika:
Dotazník byl přeložen metodou „forward‑ backward translation“. Pro potřeby validace byla touto českou jazykovou verzí následně vyšetřena skupina pacientů s neuropatickou bolestí periferního (n = 66) nebo centrálního (n = 30) původu (v rámci polyneuropatie či roztroušené sklerózy) a skupina nemocných s bolestí nociceptivní v důsledku pokročilé artrózy kyčelního nebo kolenního kloubu (n = 70). Za účelem hodnocení opakovatelnosti testu byl u části pacientů (n = 19) dotazník administrován dvakrát s odstupem přibližně tří hod.
Výsledky:
Srovnání jednotlivých hodnocených položek, dílčích škál i celkového NPSI skóre pomocí ROC analýzy prokázalo vysokou schopnost diskriminace mezi neuropatickou a nociceptivní bolestí (p < 0,001), ale nízkou schopnost odlišení neuropatické bolesti centrálního a periferního původu (p > 0,05). Opakovaná administrace testu potvrdila vysokou opakovatelnost testu (ICC, Intraclass Correlation Coefficient = 0,86 pro sumární skóre). Pomocí clusterové analýzy bylo identifikováno šest odlišných symptomových profilů.
Závěr:
Vytvořená česká verze dotazníku NPSI je schopna spolehlivě diskriminovat neuropatickou a nociceptivní bolest a identifikovat odlišné symptomové profily bolesti při akceptovatelné opakovatelnosti testu. Dotazník lze tedy doporučit jako vhodný a snadno použitelný nástroj v diagnostickém algoritmu neuropatické bolesti, využitelný i pro longitudinální sledování.
Klíčová slova:
neuropatická bolest – nociceptivní bolest – kvantifikace bolesti – dotazník – polyneuropatie – roztroušená skleróza – artróza
Úvod
Neuropatická bolest je součást klinického obrazu řady onemocnění periferního i centrálního nervového systému. Podle aktuální definice vzniká důsledkem léze nebo nemoci postihující somatosenzitivní nervový systém [1].
Ve vyspělém světě se její prevalence odhaduje na 6– 8 % populace [2,3]. Nejčastěji se vyskytuje u diabetické polyneuropatie, po traumatech periferních nervů, toxických (alkoholových, polékových) a ischemických poškozeních periferního nervového systému, při neuroinfekcích (borelióze, herpetických infekcích, HIV), neuralgii trigeminu, míšních lézích, po iktech či při roztroušené skleróze. Neuropatická složka je také významnou součástí bolesti vertebrogenního původu.
Neuropatická bolest je spojována s typickými deskriptory (popisnými charakteristikami), jako např. pálení, bodání, svědění, pocit elektrických výbojů či bolestivého chladu, a často bývá provázena dalšími senzitivními vjemy, jako jsou mravenčení anebo brnění apod. Stanovení přítomnosti těchto deskriptorů je klíčovou součástí diagnostického algoritmu neuropatické bolesti, a to jak v rámci anamnézy, tak i při použití v rámci specializovaných dotazníků zaměřených na diagnostiku neuropatické bolesti. Tyto dotazníky umožňují detailní deskripci bolesti, většinou v kombinaci s hodnocením intenzity celkové bolesti a/ nebo jejích jednotlivých charakteristik a v některých případech i se specifikací její anatomické distribuce [4– 15]. V klinické praxi je k dispozici velké množství takových dotazníků, jejich validita v diagnostice neuropatické bolesti však není ve všech případech stejná a většina dotazníků není cíleně zaměřena na neuropatickou bolest jako takovou, což snižuje senzitivitu i specificitu příslušného dotazníku v její diagnostice [5]. Výjimku tvoří několik dotazníků, které byly v posledních letech cíleně vyvinuty právě jako skríningové testy za účelem rychlé a objektivní identifikace neuropatické bolesti na podkladě přítomnosti jejích typických deskriptorů (v některých případech v kombinaci s jednoduchým klinickým testováním). Jedná se především o následující dotazníky: „The LANSS Pain Scale: the Leeds Assessment of Neuropathic Symptoms and Signs“ [9,10], „Neuropathic Pain Questionnaire“ [11], a jejich zkrácená verze [12], „Neuropathic Pain Symptom Inventory“ [13], „DN 4“ [14], „ID Pain“ [15] či „PainDETECT“ [4]. Tyto dotazníky vykazují vysokou a vzájemně srovnatelnou validitu v diskriminaci neuropatické a nociceptivní bolesti [5] a jsou podle aktuálních doporučení klíčovou součástí diagnostického procesu neuropatické bolesti, zejm. pro nespecialisty [16,17]. Vedle diagnostiky neuropatické bolesti jsou využívány pro analýzu jednotlivých symptomových profilů testovaných pacientů. Dotazníky tak poskytují např. podklad pro stratifikaci pacientů v rámci lékových či intervenčních studií nebo hodnocení cíleného efektu léčby na jednotlivé komponenty neuropatické bolesti. Z longitudinálního hlediska je účelné jejich využití pro monitorace terapeutického efektu preparátů využívaných v léčbě neuropatické bolesti, stejně jako pro potřeby monitorování klinického vývoje v rámci dlouhodobého sledování pacientů. Žádný z těchto dotazníků nebyl nicméně dosud validován v českém jazyce.
Dotazník NPSI (Neuropathic Pain Symptom Inventory) [13], na jehož validaci je zaměřena prezentovaná studie, je jedním z výše jmenovaných specifických diagnostických nástrojů vyvinutých cíleně za účelem diagnostiky neuropatické bolesti a analýzy jednotlivých jejích subtypů. Dotazník obsahuje 12 položek a je zaměřen na popis pacientových bolestí v posledních 24 hod (Příloha 1). Deset otázek je zaměřeno na typické deskriptory neuropatické bolesti a její časté doprovodné symptomy (bolest pálivá (Q1), svíravá (Q2), tlaková (Q3), krátká záchvatovitá bolest charakteru elektrického šoku (Q5) či bodání (Q6), bolest evokovaná vnějším podnětem, tj. dotekem (Q8), tlakem (Q9) anebo chladem (Q10), a přítomnost abnormálních pocitů v distribuci bolesti charakteru mravenčení (Q11) či brnění (Q12)). Intenzita každého z těchto deskriptorů je hodnocena pomocí numerické škály bolesti (Numeric Rating Scale, NRS) (Příloha 1). Celkové NPSI skóre je pak vypočteno jako průměr hodnot NRS z těchto 10 otázek (Příloha 2). Jedna otázka testu (Q4) je zaměřena na počet hodin, po které pacient v posledním dni trpěl samovolnou bolestí, a jeden dotaz (Q7) je cílen na počet krátkých záchvatů bolesti podobných elektrickému šoku či bodání. U obou otázek jsou odpovědi hodnoceny semikvantitativně (Příloha 1) a v originální verzi testu se do celkového NPSI skóre ani do jednotlivých dílčích škál (viz níže) nezapočítávají (Příloha 2). Podle některých novějších prací zaměřených na validaci NPSI dotazníku, resp. jeho jazykových verzí mohou být tyto otázky při výpočtu celkového skóre také zohledněny, případně může být jednotlivým otázkám dotazníku přikládána různá váha (s ohledem na jejich poněkud odlišnou validitu v diagnostice neuropatické bolesti). Mohou tak být vypočtena modifikovaná NPSI skóre (např. NPSI‑ G skóre [18]). Autoři originální verze dále doporučují výpočet dílčích škál hodnotících specificky intenzitu jednotlivých typů neuropatické bolesti (tj. povrchové a hluboké spontánní bolesti, krátké záchvatovité bolesti, bolesti vyvolané či zhoršené vnějším podnětem) a doprovodných abnormálních senzitivních pocitů (Příloha 2).


Cílem prezentované studie bylo vytvoření české jazykové verze dotazníku Neuropathic Pain Symptom Inventory tak, aby byla akceptovatelná tvůrci původní jazykové verze a co nejsrozumitelnější pro české pacienty, a validace jejího použití v klinické praxi.
Soubor
Do studie byly zařazeny dvě skupiny pacientů:
- a) pacienti s periferní či centrální neuropatickou bolestí (jako klinickým projevem polyneuropatie či roztroušené sklerózy), vyšetřovaní v příslušném období (viz metodika) na Neurologické klinice LF MU a FN Brno a
- b) pacienti s nociceptivní bolestí při artróze kyčelního nebo kolenního kloubu, bezprostředně před implantací endoprotézy (TEP), hospitalizovaní či ambulantně vyšetření na Ortopedické klinice stejné nemocnice. Vstupním kritériem pro oba soubory byla dobrá spolupráce pacienta, ochota k zařazení do studie a absence kognitivního deficitu. Všichni zařazení jedinci byli informováni o účelu vyšetření a podepsali informovaný souhlas. Protokol vyšetření byl schválen etickou komisí FN Brno.
Soubor A – pacienti s neuropatickou bolestí
Do souboru pacientů s neuropatickou bolestí bylo zařazeno 96 jedinců (32 mužů a 64 žen, průměrný věk 56,4 ± 14,7 let) (tab. 1a, b). Diagnóza neuropatické bolesti byla u nich expertně stanovena na základě podrobného rozboru anamnestických dat. Léze nebo dysfunkce somatosenzitivního nervového systému (jejíž přítomnost je dle současných doporučení vyžadována pro stanovení diagnózy neuropatické bolesti) byla konfirmována pomocí klinického a EMG vyšetření u pacientů s periferní neuropatickou bolestí při polyneuropatii (soubor A1, 66 pacientů) a/ nebo pomocí klinického vyšetření, somatosenzitivních evokovaných potenciálů a MR vyšetření mozku a/ nebo C či Th míchy u pacientů s centrální neuropatickou bolestí při roztroušené skleróze (soubor A2, 33 pacientů). Základní diagnóza (polyneuropatie a/ nebo roztroušená skleróza) byla stanovena v souladu s aktuálními diagnostickými kritérii [19,20].
Soubor B – pacienti s nociceptivní bolestí
Skupinu pacientů s nociceptivní bolestí při artróze velkých kloubů tvořilo 70 pacientů (25 mužů a 45 žen, průměrný věk 66,2 ± 9,9 let) (tab. 1a,b), z toho u 33 pacientů se jednalo o postižení kyčelního kloubu a u 37 jedinců o artrózu kloubu kolenního. Ve všech případech se jednalo o pacienty s pokročilým stupněm artrotického postižení, tedy se III. nebo IV. stupněm artrózy dle RTG vyšetření příslušného kloubu při hodnocení dle Kellgren a Lawrence [21]. Pacienti byli většinou vyšetřováni bezprostředně před implantací TEP nebo byli k takovému výkonu indikováni. Vylučujícími kritérii pro zařazení do studie byly:
- známá přítomnost polyneuropatie, onemocnění centrálního nervového systému či bolesti radikulárního původu;
- anamnestická přítomnost rizikových faktorů periferních neuropatií (zejm. diabetu mellitu, chronického abúzu alkoholu či stavu po aplikaci chemoterapie v anamnéze), a/ nebo
- abnormální nález při klinickém neurologickém vyšetření (korelující s postižením periferních nervů na DKK, radikulopatií L3– S1 bilat. nebo s postižením centrálního nervového systému).
V rámci statistického zpracování byl soubor vyhodnocen jako celek a současně bylo provedeno srovnání výsledků u pacientů s klidovými bolestmi při artróze (soubor B1, 31 pacientů) a pacientů bez klidových bolestí (tedy s bolestmi vázanými pouze na pohyb, resp. zátěž příslušného kloubu, soubor B2, 39 pacientů) (tab. 1b).
Metodika
Validace dotazníku probíhala od října 2012 do února 2014 ve FN Brno.
Všichni zařazení pacienti podstoupili detailní anamnestické a klinické neurologické vyšetření: u pacientů s neuropatickou bolestí bylo toto vyšetření součástí diagnostického procesu základního onemocnění a neuropatické bolesti jako takové a bylo zaměřeno také na konfirmaci léze somatosenzitivního nervového systému. U pacientů s bolestí nociceptivní bylo vyšetření zaměřeno na potvrzení absence vylučujících kritérií pro zařazení do studie. Následně byl každý pacient vyšetřen pomocí české verze dotazníku NPSI (NPSIcz).
Česká verze dotazníku NPSI (NPSIcz) byla vytvořena metodou forward‑ backward translation. Vyplnění dotazníku pacientem proběhlo ve všech případech v návaznosti na anamnestické a klinické neurologické vyšetření, a to v přítomnosti vyšetřujícího lékaře. V souladu s metodikou použití originální verze NPSI byly jednotlivé položky dotazníku zaměřené na popis intenzity jednotlivých deskriptorů neuropatické bolesti (otázky Q1, Q2, Q3, Q5, Q6, Q8, Q9, Q10, Q11, Q12) hodnoceny pomocí numerické škály bolesti (Numeric Rating Scale; NRS) v rozsahu 0– 10. „0“ na této škále znamená absenci bolesti příslušného charakteru a „10“ představuje nejhorší představitelnou intenzitu bolesti daného typu. Celkové základní NPSIcz skóre bylo vypočteno jako průměr hodnot NRS v těchto 10 otázkách (Příloha 2),tedy stejně jako v originální verzi bez zohlednění otázek Q4 a Q7 zaměřených na dobu trvání a frekvenci symptomů. Vytvořena byla dále modifikovaná verze NPSIcz skóre (NPSIcz‑ 12 skóre), započítávající i položky Q4 a Q7 NPSIcz dotazníku (blíže viz Statistická metodologie). Hodnoceny byly i dílčí škály, reflektující specificky intenzitu některých subtypů neuropatické bolesti, tj. povrchové spontánní bolesti (otázka Q1), hluboké spontánní bolesti (průměrná hodnota NRS z otázek Q2 + Q3), krátké záchvatovité bolesti (průměr NRS z otázek Q5 + Q6), bolesti vyvolané či zhoršené vnějším podnětem (průměrné NRS z otázek Q8 + Q9 + Q10) a přítomnost abnormálních senzitivních pocitů (průměrná hodnota NRS v otázkách Q11 + Q12) (Příloha 2). Výsledky byly srovnány mezi skupinami pacientů s neuropatickou a nociceptivní bolestí (soubor A vs soubor B) a dále mezi pacienty s klidovou (spontánní) nociceptivní bolestí (B1) a pacienty s neuropatickou bolestí jako celkem (A). Srovnání bylo provedeno i mezi souborem B1 (pacienti s klidovou nociceptivní bolestí) a jednotlivými podskupinami souboru A, tedy pacienty s neuropatickou bolestí periferní (A1) a centrální (A2). Obě podskupiny souboru A byly srovnány také vzájemně (soubory A1 vs. A2).
Příloha ke stažení zde [PDF].
Sledován byl rovněž čas potřebný k vyplnění dotazníku. Současně byla hodnocena náročnost jeho vyplnění (semikvantitativně na stupnici 1– 5, kde 1 = zcela nenáročný a 5 = velmi náročný), a to jak pacientem, tak i vyšetřujícím lékařem.
U 19 pacientů byl test administrován dvakrát s odstupem tří hod za účelem ověření reprodukovatelnosti vyšetření.
Statistické zpracování
Statistické zpracování bylo provedeno pomocí software SPSS 22 (IBM Corporation, 2013), Statistica 12 (Statsoft Inc., 2013) a MedCalc verze 14.10.02 (MedCalc Software, 1993– 2014). Ke zviditelnění rozdělení primárních hodnot jednotlivých testovaných parametrů byla použita standardní deskriptivní statistika (průměry a směrodatné odchylky pro spojité proměnné a absolutní a relativní četnosti pro data kategoriální). Srovnání hodnocených parametrů mezi jednotlivými skupinami pacientů bylo provedeno pomocí exaktního Fisherova testu pro kategoriální proměnné a pomocí t‑testu pro srovnání nezávislých vzorků a ANOVA modelu pro spojitá data, s následnými dílčími post‑hoc testy (Tukeyho test).
Následně byla provedena diskriminační analýza a na základě koeficientů tohoto modelu byl vážením jednotlivých otázek vytvořen třetí možný způsob výpočtu NPSI skóre (diskriminační skóre – NPSIcz‑ D skóre).
ROC (Receiver Operating Characteristic curve) analýza byla použita pro identifikaci cut‑off hodnot u otázek Q4 a Q7 NPSI skóre (před jejich začleněním do modifikovaného NPSIcz-12 skóre a před diskriminační analýzou s výpočtem NPSIcz‑ D skóre, pro jejichž účel byly tyto položky na základě výsledků ROC analýzy binárně kódovány) a současně pro zhodnocení diagnostické validity originálního NPSI skóre a jeho modifikovaných verzí (NPSIcz-12 skóre po začlenění binárně kódovaných položek Q4 a Q7 NPSI dotazníku a NPSIcz‑ D skóre vytvořeného na podkladě diskriminační analýzy).
Analýza subtypů neuropatické bolesti byla provedena pomocí clusterové (shlukové) analýzy s použitím Euklidovských distancí a Wardových algoritmů.
Intraclass korelační koeficient (Intraclass Correlation Coefficient; ICC) byl využit pro hodnocení opakovatelnosti testu při jeho opakovaných administracích.
Výsledky
Vyplnění dotazníku NPSIcz bylo většinou pacientů i vyšetřujícím personálem hodnoceno jako nenáročné či mírně náročné a trvalo v průměru 2,23 ± 0,47 min. Rozdíly těchto parametrů mezi jednotlivými skupinami pacientů nebyly statisticky významné s výjimkou kratšího trvání testu a trendu k nižší subjektivní náročnosti jeho použití u pacientů s centrální neuropatickou bolestí při roztroušené skleróze (data neuvedena). Test byl pro pacienty dobře srozumitelný. Problémem byl pro část zařazených jedinců pouze termín „spontánní“, ke kterému několik pacientů vyžadovalo doplňující vysvětlení. U některých pacientů bylo problematické také specifické cílení odpovědí na posledních 24 hod, protože se u nich toto období vymykalo jejich dlouhodobému stavu. Oba problémy byly zohledněny při tvorbě finální verze dotazníku (Příloha 1). Doporučené změny reflektující řešení potíží zjištěných během procesu validace jsou v této verzi vyznačeny kurzivou.
Pro část pacientů bylo poněkud obtížné využití NRS škály pro hodnocení intenzity symptomů a jevili tendenci nahradit numerické hodnocení slovním popisem. Tato skutečnost poukázala na nutnost podrobného iniciálního vysvětlení před zahájením vlastního testování včetně zácviku použití NRS škály.
Hodnoty celkového NPSIcz skóre (základního i tzv. NPSIcz‑ 12 skóre, modifikovaného zařazením položek Q4 a Q7), hodnocených dílčích škál i NRS v jednotlivých testovaných položkách byly statisticky vysoce významně vyšší ve skupině pacientů s neuropatickou bolestí ve srovnání s pacienty s bolestí nociceptivní (tab. 1a). Nejméně vyjádřený (i když stále statisticky významný) byl rozdíl v otázce Q9 (zhoršení bolesti tlakem). Pacienti s neuropatickou bolestí udávali také delší trvání spontánní bolesti v průběhu dne (Q4) a vyšší počet krátkých záchvatů bolesti (Q7) ve srovnání s pacienty s bolestí nociceptivní.
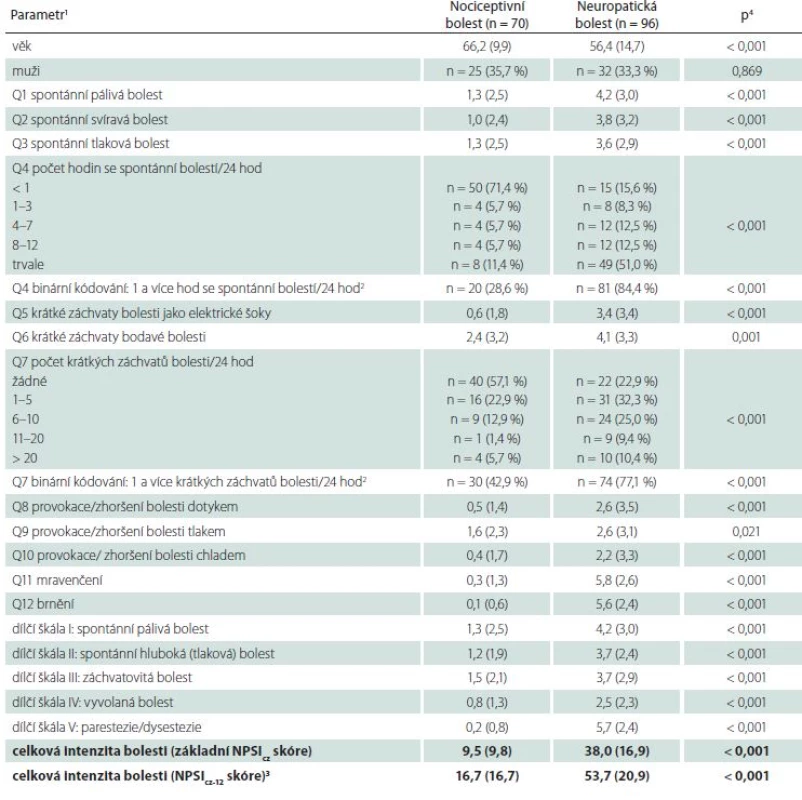
Mezi pacienty s neuropatickou bolestí centrálního a periferního typu se hodnoty celkového NPSIcz skóre (základního ani NPScz‑ 12) ani dílčích škál statisticky významně nelišily (tab. 1b). V každé z obou podskupin pacientů s neuropatickou bolestí byly tyto hodnoty signifikantně odlišné od pacientů s bolestí nociceptivní, a to zejm. při srovnání s jedinci s nociceptivní bolestí bez klidových obtíží. Méně významné byly rozdíly každé z podskupin jedinců s neuropatickou bolestí oproti pacientům s klidovou (spontánní) nociceptivní bolestí (tab. 1b). Při srovnání jednotlivých položek NPSIcz skóre mezi oběma skupinami pacientů s neuropatickou bolestí byl prokázán významně častější výskyt spontánní pálivé a svíravé bolesti u pacientů s centrální etiologií a celkově menší počet hodin se spontánní bolestí u těchto pacientů ve srovnání s pacienty s bolestí periferního typu (tab. 1b).

Pacienti s klidovými bolestmi při artróze kolenního či kyčelního kloubu vykazovali obecně signifikantně vyšší hodnoty celkového NPSIcz skóre, dílčích škál i jednotlivých hodnocených položek ve srovnání s pacienty, u nichž byla bolest v rámci kloubního postižení vázána pouze na pohyb, resp. zátěž příslušného kloubu (tab. 1b). Hodnoty celkového NPSIcz skóre (základního i NPSIcz‑ 12) i jednotlivých dílčích škál byly v obou nociceptivních skupinách signifikantně nižší oproti pacientům s neuropatickou bolestí (tab. 1b).
Provedená diskriminační analýza zaměřená na odlišení neuropatické a nociceptivní bolesti (k dispozici jako Supplementary data v on‑line verzi článku) byla využita pro koncept třetího způsobu výpočtu NPSIcz skóre, tzv. NPSIcz‑ D skóre.
Následná ROC analýza prokázala velmi dobrou diagnostickou validitu NPSIcz skóre v odlišení neuropatické bolesti (i jejích jednotlivých typů) od bolesti nociceptivní (včetně klidové nociceptivní bolesti), a to při použití různých způsobů výpočtu NPSIcz skóre (grafy 1a–d, tab. 2). Diagnostická validita byla ve všech případech velmi dobrá již pro základní NPSIcz skóre, obdobná (ale nikoli vyšší) pro NPSIcz‑ 12 skóre a jednoznačně nejvyšší byla u diskriminačního NPSIcz‑ D skóre, kde se blížila dokonalosti (grafy 1a––d, tab. 2). Validita testu v odlišení pacientů s neuropatickou bolestí (či jejích jednotlivých podskupin) od jedinců s bolestmi nociceptivními byla obecně vyšší při zohlednění nociceptivní skupiny jako celku (tedy současně pacientů bez spontánních bolestí i s nimi) než v případě, kdy bylo srovnání provedeno pouze vůči pacientům s klidovou nociceptivní bolestí (grafy 1a– d, tab. 2). I v případě srovnání s pacienty se spontánní nociceptivní bolestí byla však validita testu v diagnostice neuropatické bolesti uspokojivá (grafy 1a– d, tab. 2).
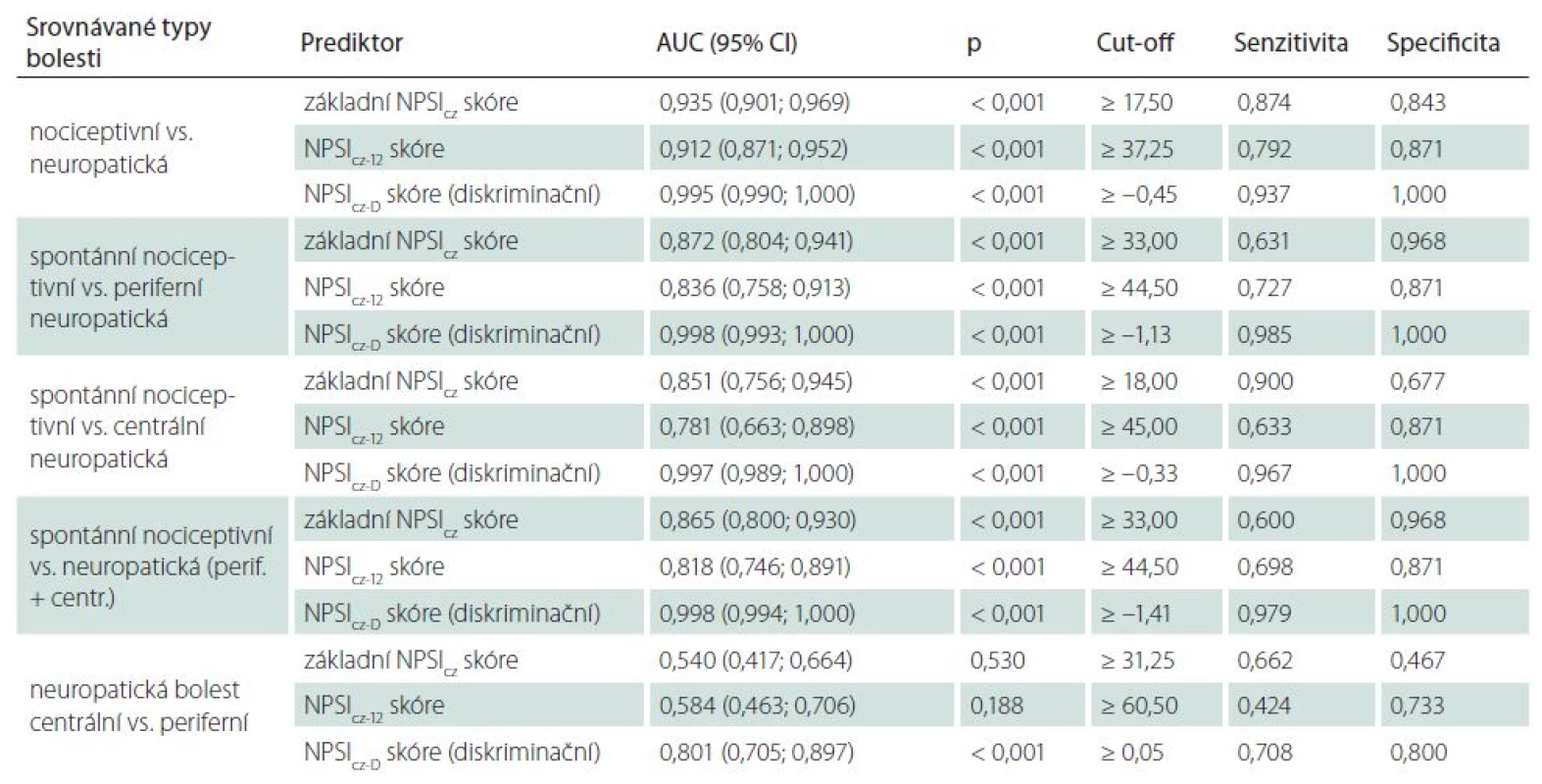

Základní NPSIcz skóre ani modifikovaná verze NPSIcz‑ 12 neumožňovaly spolehlivé odlišení centrální a periferní neuropatické bolesti. Toto rozlišení bylo možné pouze pomocí diskriminačního NPSIcz‑ D skóre (tab. 2, graf 1e). Diagnostická validita testu v diskriminaci centrální a periferní neuropatické bolesti byla však i v tomto případě nižší než spolehlivost testu v odlišení neuropatické bolesti od bolesti nociceptivní (tab. 2).
Clusterová analýza umožnila identifikaci šesti symptomových profilů, lišících se přítomností jednotlivých hodnocených deskriptorů neuropatické bolesti a jejich intenzitou (graf 2). V každé z těchto šesti podskupin byli zastoupeni pacienti s centrální i periferní neuropatickou bolestí.
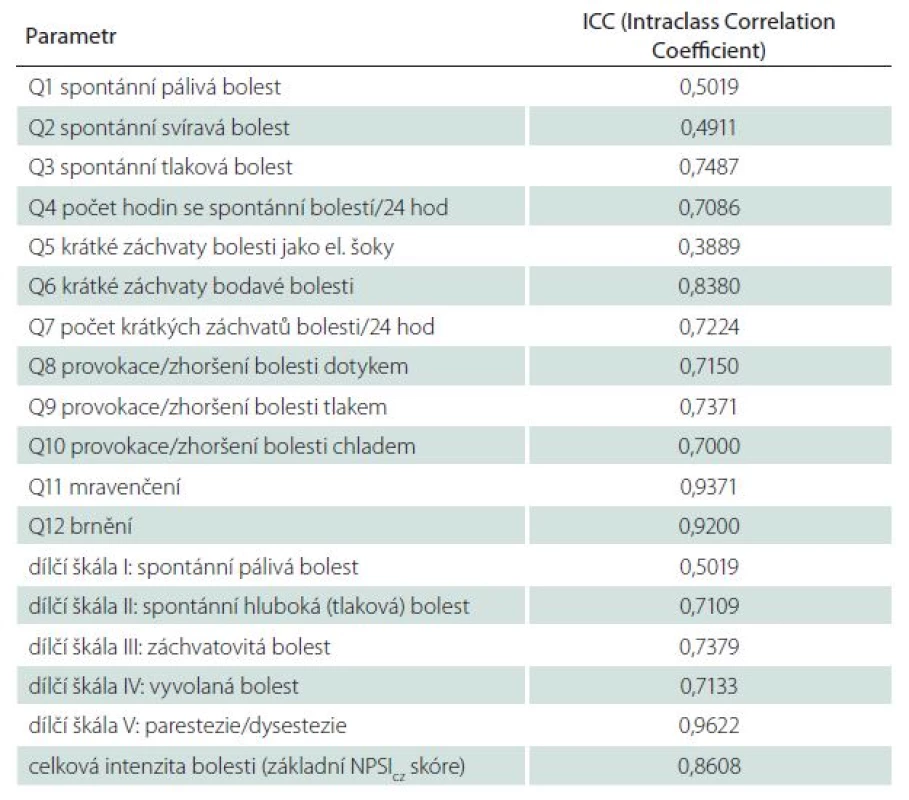
Opakovaná administrace NPSI dotazníku prokázala uspokojivou opakovatelnost sumárního NPSIcz skóre i většiny položek testu a dílčích škál, hodnocenou pomocí intraclass korelačních koeficientů (tab. 3).

Diskuze
Provedená studie ověřila snadnou použitelnost dotazníku NPSIcz v diagnostice neuropatické bolesti, jeho vynikající diskriminační schopnost oproti bolesti nociceptivní a schopnost identifikace jednotlivých symptomových profilů neuropatické bolesti. Zařazení testu do diagnostického algoritmu pacientů s neuropatickou bolestí je vzhledem k nízké časové náročnosti, vysoké diagnostické validitě a uspokojivé opakovatelnosti možné jak pro potřeby rutinního klinického testování, tak pro účely klinických či výzkumných studií včetně longitudinálního sledování pacientů.
Náročnost testování, potřeba asistence při vyplnění dotazníku
Test byl většinou pacientů i vyšetřujících hodnocen jako nenáročný či málo náročný a jeho vyplnění trvalo pouze několik minut. Nižší časová náročnost testu u pacientů s centrální neuropatickou bolestí je zřejmě podmíněna nižším věkem jedinců v této skupině a také jejich obecně větší zkušeností s vyplňováním dotazníků různého druhu pro potřeby lékových i jiných studií. I v ostatních skupinách pacientů však bylo trvání testu i jeho subjektivně hodnocená náročnost zcela přijatelné.
Autoři originální verze koncipovali test tak, že jej pacient vyplňuje sám, bez pomoci lékaře. Při procesu validace české verze byl ve většině případů vyplnění dotazníku přítomen lékař, což se ukázalo jako účelné s ohledem na možnost bezprostředního vysvětlení některých termínů v původně vytvořeném českém překladu originální verze, které nebyly pro část pacientů dobře srozumitelné (viz níže). Přítomnost lékaře (či jiné zacvičené osoby) byla přínosná i pro možnost ověření konzistence odpovědí pacienta s jeho dlouhodobými klinickými obtížemi (rovněž viz níže). Několik pacientů vyžadovalo asistenci vyšetřujícího také za účelem pomoci s využitím NRS škály, které bylo pro některé z nich navzdory úvodnímu vysvětlení principu hodnocení poněkud problematické. Část pacientů jevila tendenci nahradit číselný údaj NRS škály slovním popisem intenzity. Použití dotazníku u nich proto vyžadovalo opakované detailní vysvětlení. Z uvedených skutečností vyplývá, že v případě, kdy pacient vyplňuje dotazník samostatně, je nezbytné detailní úvodní vysvětlení principu testování včetně zácviku využití NRS škály. Optimální je ověřit porozumění pacienta principům testování vyplněním alespoň jedné otázky dotazníku v přítomnosti vyšetřujícího. Účelná je i následná konfirmace výsledků dotazem objektivizujícím soulad uvedeného číselného údaje např. se slovním popisem intenzity daného deskriptoru pacientem pro verifikaci správného použití NRS škály a konzistence odpovědí se skutečnými obtížemi pacienta. Je proto vhodné, aby byl pacientovi během vyšetření k dispozici zaučený asistent (kterým může být zdravotní sestra či dokonce nezdravotnický personál obeznámený s principy testování), na kterého se může pacient obrátit v případě potřeby.
Jazyková stránka tvorby české verze NPSIcz dotazníku
Česká verze dotazníku byla vytvořena metodou „forward‑ backward translation“, tedy metodou zpětného překladu, kdy je původní jazyková verze přeložena do češtiny a tato česká verze následně jiným překladatelem převedena do angličtiny. Poté jsou posuzovány rozdíly takto vytvořené verze v původním jazyce s originální verzí dotazníku a hledán konsenzus v neshodujících se termínech. Tento způsob tvorby jazykových mutací dotazníků je obvyklou součástí validačního procesu a je většinou vyžadován autory originálních dotazníků pro uznání nové jazykové verze.
Původní česká jazyková verze vytvořená zmíněnou metodou forward‑ backward translation obsahuje v úvodním odstavci výraz „spontánní bolest, tj. objevující se bez jakékoli provokace“ (Příloha 1). Pro řadu pacientů však nebyl výraz „spontánní“ dobře srozumitelný. Autoři práce proto doporučují zpřesnění termínu doplněním výrazu „samovolná“, které bylo použito při ústním vysvětlení v případě dotazu pacienta na slovo „spontánní“ a které bylo pro testované pacienty lépe srozumitelné. Tento zpřesňující termín jsme zařadili i do finální verze českého NPSIcz dotazníku.
Dotazník je v originální verzi koncipován tak, aby reflektoval obtíže pacienta za posledních 24 hod. V provedené studii se tato okolnost ukázala jako poněkud problematická, a to především u souboru pacientů před implantací TEP. Tito pacienti byli v době vyplňování dotazníku většinou krátkodobě hospitalizováni před plánovaným ortopedickým zákrokem. Hodnocené období posledních 24 hod se vymykalo jejich dlouhodobému stavu, protože v důsledku omezení fyzické aktivity při hospitalizaci u nich došlo k poklesu intenzity bolestí vázaných na pohyb či pohybem akcentovaných. Diskrepance s běžnou intenzitou obtíží byla zjištěna v rámci rozhovoru s vyšetřujícím lékařem, který mj. cíleně ověřoval konzistenci odpovědí s dlouhodobým stavem pacienta. Z tohoto důvodu byla v rámci validačního procesu do textu původní české jazykové verze dotazníku za údaj o zohlednění obtíží za posledních 24 hod dodatečně doplněna věta: „pokud se toto časové období zásadně neliší od vašeho běžného průměru např. v posledním měsíci“. Tato věta podle zkušeností autorů zvýší pravděpodobnost souladu odpovědí pacienta s jeho dlouhodobými potížemi v případě, že pacient vyplňuje dotazník sám, bez asistence vyšetřujícího lékaře či jiného zaučeného zdravotního personálu.
Diagnostická validita dotazníku
Dotazník NPSI je v originální verzi zaměřen na diagnostiku neuropatické bolesti, resp. její odlišení od bolesti nociceptivní [13]. Většina položek dotazníku je tedy zaměřena na tzv. deskriptory charakteristické pro neuropatickou bolest. Podle očekávání byly proto hodnoty celkového NPSIcz skóre, dílčích škál i NRS skóre v jednotlivých položkách dotazníku signifikantně vyšší ve skupině pacientů s neuropatickou bolestí oproti jedincům s bolestí nociceptivní.
Nejméně výrazné rozdíly mezi pacienty s nociceptivní a neuropatickou bolestí byly prokázány v otázce Q9 (Zhoršení bolesti tlakem). Tento příznak byl často přítomen u pacientů s bolestí neuropatického i nociceptivního původu, což není překvapivé, protože tlak je známý provokační faktor bolesti při artrotickém postižení kloubů stejně jako u pacientů s bolestí neuropatického typu.
Diagnostická validita testu je kromě jiných faktorů významně ovlivněna výběrem srovnávaných vzorků pacientů. U jedinců s neuropatickou bolestí jsou kritéria pro zařazení do studií poměrně jednoznačná. V publikovaných studiích jde prakticky bezvýhradně o jedince s bolestí odpovídající současné definici [1], a to s intenzitou odpovídající NRS ≥ 4, resp. 3 [2,4,13,18]. U souboru pacientů s bolestí nociceptivní je však definice souboru významně ovlivněna skutečností, že klidová bolest není uniformně přítomným symptomem artrózy velkých kloubů DKK, a to ani v pokročilých stadiích kloubních změn [22]. V úvodní fázi validačního procesu byli do skupiny pacientů s nociceptivní bolestí zařazováni konsekutivně téměř všichni pacienti přicházející na Ortopedickou kliniku FN Brno k implantaci TEP. V tomto souboru bylo proto zařazeno velké množství jedinců, u nichž byla bolest vázána výhradně na pohyb či zátěž příslušného kloubu, a tedy bez bolestí klidových, což vedlo k velmi vysoké diskriminační schopnosti NPSIcz. V klinické praxi je však problém spíše odlišení neuropatické bolesti od spontánní klidové nociceptivní bolesti. Proto byl soubor pacientů s nociceptivní bolestí v dalším období rozšířen zejména o pacienty s klidovými bolestmi při artróze velkých kloubů a následné statistické zpracování bylo zaměřeno mj. na zhodnocení diagnostické validity dotazníku v odlišení neuropatické bolesti izolovaně od pacientů s klidovými bolestmi nociceptivními a bez nich. Výsledky statistické analýzy prokázaly, že diskriminace pacientů s neuropatickou bolestí od pacientů s klidovou nociceptivní bolestí je poněkud nižší než při zohlednění nociceptivních pacientů bez klidových bolestí, stále ale velmi uspokojivá.
Nastavení vstupních kritérií je také pravděpodobným důvodem poněkud vyšší diagnostické validity základního NPSIcz skóre v naší studii oproti obdobné validační studii německé verze dotazníku [18]. V této studii nebylo základní NPSI skóre schopno diskriminovat spolehlivě pacienty s neuropatickou bolestí od pacientů s bolestí neneuropatickou. Tuto schopnost vykázala až modifikovaná verze, tzv. NPSI‑ G (German) skóre vytvořená na základě diskriminační analýzy, podobně jako NPSIcz‑ D skóre v naší studii. Skupina pacientů s neneuropatickou bolestí však byla tvořena jednak pacienty s osteoartrózou (bez bližší specifikace stupně pokročilosti postižení či případného výskytu klidových bolestí) a dále pacienty s bolestí hlavy (kteří v naší studii nefigurovali).
Diagnostická validita NPSIcz skóre byla v prezentované studii, stejně jako např. v práci Sommera et al [18], hodnocena pomocí ROC křivky. ROC křivka je statistický parametr kombinující senzitivitu a specificitu testu pro jednotlivé hodnoty (cut‑offs), které může test nabývat. Čím vyšší je pro daný test plocha pod křivkou (tzv. Area Under Curve; AUC), tím vyšší je jeho diagnostická validita. Z křivky lze odečíst senzitivitu a specificitu pro každou hodnotu cut‑off testu, a stanovit tak hodnotu s optimální kombinací obou parametrů jako limitní pro dané vyšetření. Ze statistického hlediska jde o optimální statistický test umožňující hodnocení diagnostické validity vyšetření. Výsledky prezentované studie (stejně jako validace německé verze NPSI) proto lépe reflektují problematiku diagnostické validity testu než originální verze testu [13], v níž je validita hodnocena bez použití ROC analýz.
V prezentované studii byla diagnostická validita NPSIcz dotazníku hodnocena jednak pro základní NPSIcz skóre (vypočítané podle doporučení autorů originální verze dotazníku [13]), jednak pro dvě modifikovaná skóre: NPSIcz‑ 12 (zohledňující i položky Q4 a Q7) a NPSIcz‑ D (vytvořené na základě diskriminační analýzy). Diagnostická validita NPSIcz‑ 12 skóre byla obdobná jako validita základní NPSIcz verze, NPSIcz‑ D skóre však při ROC analýze vykázalo signifikantně lepší validitu a představuje ze statistického hlediska funkci s maximální prediktivní silou. Pro potřeby exaktního odlišení pacientů s neuropatickou a nociceptivní bolestí je tak použití modifikovaných verzí (a to především skóre NPSIcz‑ D) vhodnější nástroj než základní NPSIcz skóre.
Dotazník NPSI není primárně zaměřen na odlišení centrální a periferní neuropatické bolesti. Oba typy neuropatické bolesti vykazují řadu podobných charakteristik a deskriptory používané v jejich popisu jsou obdobné [1,4,5]. V souladu s touto skutečností nebyly prokázány významné rozdíly základního NPSI mezi pacienty s centrální a periferní neuropatickou bolestí a rozdíly jednotlivých dílčích položek NPSI skóre mezi těmito skupinami byly jen ojedinělé. Obě skupiny bylo možno částečně diskriminovat pomocí NPSIcz‑ D skóre, ale s obecně nižší validitou oproti odlišení neuropatické bolesti od bolesti nociceptivní. Dotazník tedy obecně není spolehlivě využitelný pro odlišení centrální a periferní neuropatické bolesti.
Analýza subtypů neuropatické bolesti
Provedená clusterová analýza umožnila v prezentované studii identifikovat šest odlišných symptomových profilů. Zmíněné profily jsou podobné jako ve srovnatelné studii zaměřené na validaci německé jazykové verze stejného dotazníku [18]. Zastoupení pacientů s centrální i periferní neuropatickou bolestí v každé z takto definovaných podskupin pacientů poukazuje na skutečnost, že patologický proces zodpovědný za rozvoj neuropatické bolesti není klíčovým faktorem v rozvoji příslušného symptomového profilu. Definované profily však mohou být podkladem např. pro odlišnou odpovídavost pacientů na terapii neuropatické bolesti či rozdílný přirozený vývoj onemocnění u jedinců s odlišným symptomovým profilem. Tuto hypotézu bude nutno potvrdit následnými studiemi.
Opakovatelnost vyšetření
Provedená intraclass korelační analýza na základě opakovaných administrací dotazníku prokázala uspokojivou opakovatelnost testu, a to zejm. při hodnocení sumárního skóre (ICC = 0,86). Srovnatelná opakovatelnost byla prokázána i pro originální francouzskou (ICC = 0,94) [13] a recentně validovanou německou jazykovou verzi NPSI dotazníku (ICC = 0,89) [18]. Opakovatelnost některých položek testu byla v naší studii horší než v případě německé a francouzské verze, což je nejspíše podmíněno omezeným rozsahem testovaného vzorku v našem souboru, kde byla opakovatelnost hodnocena jen u 19 pacientů. Důsledkem hodnocení opakovatelnosti v menším souboru pacientů může být větší vliv eventuálních odlehlých hodnot na výsledný ICC u některých dílčích položek naší studie.
Uspokojivá opakovatelnost celkového NPSI skóre prokázaná ve všech provedených studiích včetně naší opravňuje použití dotazníku pro longitudinální sledování pacientů a hodnocení změn klinických symptomů, a to jak v souvislosti s přirozeným průběhem onemocnění a vývojem základního patologického procesu vedoucího k rozvoji neuropatické bolesti, tak při sledování vlivu terapeutických intervencí zaměřených na ovlivnění neuropatické bolesti a souvisejících symptomů.
Závěr
Prezentovaná studie prokázala vysokou diagnostickou validitu nově vytvořené české jazykové verze dotazníku NPSI (NPSIcz) v diskriminaci neuropatické a nociceptivní bolesti a analýze symptomových profilů umožňující hodnocení jednotlivých subtypů neuropatické bolesti. Prokázána byla i nízká časová náročnost, uspokojivá opakovatelnost a snadná použitelnost testu. Dotazník lze využít v podmínkách ambulantní neurologické praxe i pro potřeby klinických či vědeckých studií. Administraci dotazníku musí předcházet detailní vysvětlení způsobu testování a principu použití NRS škály, následně mohou pacienti vyplnit dotazník samostatně, ale je vhodné, aby byl v dosahu zaškolený personál, který může odpovědět na případné dotazy. Během procesu validace bylo zjištěno několik drobných problémů s původně vytvořenou českou jazykovou verzí. Ty byly zohledněny při tvorbě finální verze dotazníku vhodné pro účely použití v českém jazykovém prostředí. Provedená studie prokázala velmi uspokojivou diagnostickou validitu dotazníku v odlišení neuropatické a nociceptivní bolesti. Tato validita je dostačující již při základním způsobu výpočtu NPSIcz skóre (dle doporučení autorů originální verze) a dále stoupá použitím jeho modifikovaných verzí (zejména NPSIcz‑ D skóre). Test v základní verzi naopak není schopen spolehlivě odlišit pacienty s centrální a periferní neuropatickou bolestí. Vedle detekce neuropatické bolesti umožňuje dotazník také analýzu jednotlivých symptomových profilů. Jejich klinická relevance však bude muset být ověřena následnými studiemi.
Seznam použitých zkratek
AUC Area Under Curve (plocha pod ROC křivkou)
ICC Intraclass Correlation Coefficient
NPSI Neuropathic Pain Symptom Inventory (dotazník pro diagnostiku neuropatické bolesti)
NPSIcz česká verze dotazníku Neuropathic Pain Symptom Inventory (a jeho originálního skóre)
NPSIcz-12 skóre modifikovaná verze originálního NPSIcz skóre, která zohledňuje i výsledky otázek Q4 a Q7 (nezapočítávané do NPSI skóre v originální verzi testu)
NPSIcz-D skóre modifikovaná verze originálního NPSIcz skóre, vytvořená na základě výsledků diskriminační analýzy
NRS Numeric Rating Scale (numerická škála bolesti)
ROC křivka Receiver Operating Characteristic curve
TEP totální endoprotéza (kyčelního nebo kolenního) kloubu
Práce byla podpořena grantem IGA MZ ČR NT 13523-4 a MZ ČR – RVO (FNBr, 65269705), interními zdroji CEITEC MUNI a 7. rámcovým programem Evropské unie v rámci projektu No. 602133 (Non- -coding RNAs for personalised pain medicine).
Autoři práce děkují paní Janě Novohradské za pomoc při sběru dat a vyšetřování pacientů.
MUDr. Eva Vlčková
Neurologická klinika
LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: evlckova@email.cz
Přijato k recenzi: 1. 8. 2014
Přijato do tisku: 28. 8. 2014
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Zdroje
1. Treede RD, Jensen TS, Campbell JN, Cruccu G, Ostrovsky JO, Griffin JW et al. Neuropathic pain: redefinition and a grading system for clinical and research purposes. Brain 2008; 70(18): 1630– 1635.
2. Bouhassira D, Lantéri‑ Minet M, Attal N, Laurent B, Touboul C. Prevalence of chronic pain with neuropathic characteristics in the general population. Pain 2008; 136(3): 380– 387.
3. Torrance N, Smith BH, Bennett MI, Lee AJ. The epidemiology of chronic pain of predominantly neuropathic origin. Results from a general population survey. J Pain 2006; 7(4): 281– 289.
4. Freynhagen R, Baron R, Gockel U, Tölle TR. PainDETECT: a new screening questionnaire to identify neuropathic components in patients with back pain. Curr Med Res Opin 2006; 22(10): 1911– 1120.
5. Bennett MI, Attal N, Backonja MM, Baron R, Bouhassira D, Freynhagen R et al. Using screening tools to identify neuropathic pain. Pain 2007; 127(3): 199– 203.
6. Melzack R. The McGill Pain Questionnaire: major properties and scoring. Pain 1975; 1(3): 277– 299.
7. Gracely RH, Dubner R, McGrath P, Heft H. New methods of pain measurement and their application to pain control. Int Dent J 1978; 28(1): 52– 65.
8. Cleeland CS. Pain assessment in cancer. In: Osoba D (ed). Effect of cancer on quality of life. Boca Raton: CRC Press, Inc: 1991: 293– 305.
9. Bennett M. The LANSS Pain Scale: the Leeds assessment of neuropathic symptoms and signs. Pain 2001; 92(1– 2): 147– 157.
10. Bennett MI, Smith BH, Torrance N, Potter J. The S‑ LANSS score for identifying pain of predominantly neuropathic origin: validation for use in clinical and postal research. J Pain 2005; 6(3): 149– 158.
11. Krause SJ, Backonja MM. Development of a neuropathic pain questionnaire. Clin J Pain 2003; 19(5): 306– 314.
12. Backonja MM, Krause SJ. Neuropathic pain questionnaire – short form. Clin J Pain 2003; 19(5): 315– 316.
13. Bouhassira D, Attal N, Fermanian J, Alchaar H, Gautron M, Masquelier E et al. Development and validation of the Neuropathic Pain Symptom Inventory. Pain 2004; 108(3): 248– 257.
14. Bouhassira D, Attal N, Alchaar H, Boureau F, Brochet B, Bruxelle J et al. Comparison of pain syndromes associated with nervous or somatic lesions and development of a new neuropathic pain diagnostic questionnaire (DN4). Pain 2005; 114(1– 2): 29– 36.
15. Portenoy R. Development and testing of a neuropathic pain screening questionnaire: ID pain. Curr Med Res Opin 2006; 22(8): 1555– 1565.
16. Cruccu G, Sommer C, Anand P, Attal N, Baron R, Garcia‑ Larrea L et al. EFNS guidelines on neuropathic pain assessment: revised 2009. Eur J Neurol 2010; 17(8): 1010– 1018. doi: 10.1111/ j.1468‑ 1331.2010.02969.x.
17. Haanpää M, Attal N, Backonja M, Baron R, Bennett M, Bouhassira et al. NeuPSIG guidelines on neuropathic pain assessment. Pain 2011; 152(1): 14– 27. doi: 10.1016/ j.pain.2010.07.031.
18. Sommer C, Richter H, Rogausch JP, Frettlöh J, Lungenhausen M, Maier C. A modified score to identify and discriminate neuropathic pain: a study on the German version of the Neuropathic Pain Symptom Inventory (NPSI). BMC Neurol 2011; 11: 104. doi: 10.1186/ 1471‑ 2377‑ 11‑ 104.
19. England JD, Gronseth GS, Franklin G, Miller RG, Asbury AK, Carter GT et al. Distal symmetric polyneuropathy: a definition for clinical research: report of the American Academy of Neurology, the American Association of Electrodiagnostic Medicine, and the American Academy of Physical Medicine and Rehabilitation. Neurology 2005; 64(2): 199– 207.
20. Polman CH, Reingold SC, Banwell B, Clanet M, Cohen JA, Filippi M et al. Diagnostic criteria for multiple sclerosis: 2010 revisions to the McDonald criteria. Ann Neurol 2011; 69(2): 292– 302. doi: 10.1002/ ana.22366.
21. Kellgren JH, Lawrence JS. Radiological assessment of osteo‑ arthrosis. Ann Rheum Dis 1957; 16(4): 494– 502.
22. Haverkamp D, Brokelman RB, van Loon CJ, van Kampen A. Timing of arthroplasty, what is the influence of nocturnal pain and pain at rest on the outcome? Knee Surg Traumatol Arthrosc 2013; 21(11): 2590– 2594. doi: 10.1007/ s00167‑ 012‑ 2071‑ x.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2015 Číslo 1
Nejčtenější v tomto čísle
- Protokol diagnostiky a léčby hyponatremie a hypernatremie v neurointenzivní péči
- Mini‑Mental State Examination – česká normativní studie
- Autoimunitní encefalitidy
- Asymptomatická spondylogenní komprese krční míchy
