Koincidence roztroušené sklerózy a myasthenia gravis
Autoři:
P. Hemerková 1; H. Matulová 1; J. Jandura 2
Působiště autorů:
Neurologická klinika LF UK a FN Hradec Králové
1; Radiologická klinika LF UK a FN Hradec Králové
2
Vyšlo v časopise:
Cesk Slov Neurol N 2020; 83/116(6): 649-651
Kategorie:
Dopis redakci
doi:
https://doi.org/10.48095/cccsnn2020649
Vážená redakce,
prezentujeme případ vzácné koincidence RS a myastenia gravis (MG) u našeho nyní 70letého pacienta.
Roztroušená skleróza je chronické autoimunitní onemocnění mozku a míchy, které má s destrukcí myelinu spojenou nejen složku zánětlivou, ale i neurodegenerativní, přičemž dochází ke ztrátě axonů. Přibližná prevalence nemoci v ČR převyšuje 160/100 000 obyvatel a incidence se pohybuje okolo 11,7/100 000 [1]. Stanovení diagnózy závisí na klinickém obrazu a nálezu na MR mozku. Vyšetření mozkomíšního moku a eventuálně průkaz intrathekální syntézy (ITS) imunoglobulinů IgG má spíše doplňkový charakter a vyloučí diagnózy jiné.
Myastenia gravis je také autoimunitní onemocnění, u kterého dochází k poruše nervosvalového přenosu.
Incidence se v jednotlivých epidemiologických studiích liší. Piťha v roce 2010 odhadoval prevalenci nemoci v ČR na 240/1 000 000 a incidenci na 21/1 000 000 [2].
První příznaky onemocnění se mohou objevit v jakémkoliv věku, ale lze pozorovat dva vrcholy incidence, a to kolem 30. roku, kdy jsou postiženy spíše ženy, a kolem 60. roku, kdy je choroba častěji pozorována u mužů [3]. Dochází zde k produkci autoprotilátek B-lymfocyty proti nikotinovému acetylcholinovému receptoru (anti-AChR), svalově specifické tyrozinkináze (anti-MuSK) či nízkodenzitnímu lipoproteinovému receptoru (anti-Lrp4). Kromě produkce protilátek hraje v imunopatogenezi nemoci roli dysregulace na úrovni T lymfocytů (a to jak pomocných CD4+ T lymfocytů, tak cytotoxických CD8+ T lymfocytů) [4].
Referovaný pacient se narodil v roce 1949 a do svých 56 let vážněji nestonal. V roce 2003 havaroval při sáňkování, došlo k ruptuře pouzdra kolenního kloubu vpravo a poranění nervus peroneus communis s následnou těžkou pravostrannou peroneální parézou. Léky trvale neužíval. Rodinná anamnéza byla neurologicky negativní, až na syna trpícího dětskou mozkovou obrnou. Pracoval jako dělník a žil s nemocným synem v bytě. První příznaky možného neurologického onemocnění se u pacienta objevily v roce 2005, kdy byl neurologem vyšetřen pro vestibulocerebelární symptomatiku. Na naše pracoviště se nemocný dostavil v roce 2006 s vertiginózními potížemi. V neurostatu byl přítomen disociovaný horizontální nystagmus oboustranně v temporálních pohledech, na horních končetinách byla dystaxe, pozitivní Trömnerův jev vlevo, na dolních končetinách byla poúrazová peroneální paréza vpravo a byla přítomna také sfinkterová dysfunkce. Pociťoval zvýšenou únavu, s oporou jedné hole ušel 1 km. Byla vyslovena suspekce na demyelinizační onemocnění. Kritéria na MR pro RS byla splněna (obr. 1). V likvoru byla pozitivní ITS IgG (16 pásů). Byla stanovena diagnóza relaps-remitentní formy RS typu „late onset“. Do medikace byly nasazeny prednison 5 mg, azathioprin 50 mg/d a pacient byl odeslán k přeléčení 5 g metylprednisolonu intravenózně. V roce 2009 nemocný ušel s oporou 50 m, v neurostatu dominovala těžká spastická paraparéza dolních končetin, přidávala se slabost končetin horních. Hodnota Expanded Disability Status Scale byla 6 bodů. Nesplňoval tehdejší kritéria pro podání chorobu modifikujícího léčiva (DMD). Byla zahájena terapie dle Harvardského protokolu (každé 4 týdny 1 g Solumedrolu s následnou aplikací 800 mg cyklofosfamidu, postupně se interval prodlužoval na každých 8 týdnů). Tuto léčbu nemocný dobře toleroval. V roce 2017 byl stav stacionární. Poté však pacient z neznámých důvodů přerušil léčbu a ke kontrole se dostavil až v listopadu 2019 pro celkové zhoršení stavu. Nejvíce si stěžoval na rozmazané vidění a v neurostatu byla navíc přítomná léze nervus oculomotorius vpravo. Pacienta jsme přijali k přešetření v průběhu hospitalizace. Na MR mozku se zobrazily známé ložiskové změny bílé hmoty kompatibilní s RS, avšak nebyla popsána progrese či aktivita onemocnění. Hodnoty glykovaného hemoglobinu a hormonů štítné žlázy byly v normě. Likvorologické vyšetření bylo bez průkazu neuroinfektu. Při vyšetření EMG byla detekována porucha nervosvalového přenosu postsynaptického typu (obr. 2). CT mediastina byla bez průkazu expanze. Byla odebrána hladina protilátek, anti-AChR a anti-MuSK. Zahájili jsme medikaci pyridostigminem (Mestinon 60 mg tbl. p. o. 1–1–1) a pacienta jsme ve zlepšeném stavu propustili domů s plánem ambulantní kontroly. Za 6 dní po dimisi se pacient znovu do naší ambulance. Stěžoval si na rozmazané vidění, celkovou slabost a potíže s polykáním. Při neurologickém vyšetření byla pozorována ptóza pravého a semiptóza levého horního víčka, byl pozitivní Simpsonův i Gorelickův test. Byla již k dispozici hladina protilátek anti-AChR, které byly pozitivní (více než 8 nmol/l). Byla stanovena diagnóza generalizované séropozitivní MG. Do medikace byly přidány distigmin, prednison (v úvodu s postupnou titrací na 60 mg/d) a azathioprin. Při této terapii došlo k výraznému zlepšení. Zprvu byla s pacientem horší spolupráce – štípal doma dříví, věnoval se cyklistice a často se vracel do poradny pro nervosvalová onemocnění s epizodami dekompenzace onemocnění. Později pochopil důležitost režimových opatření a přibližně posledních 10 měsíců, při medikaci prednisonu (10 mg/d), pyridostigminu (60 mg 1–1–1 tbl.) a azathioprinu (25 mg/d), je bez příznaků MG. Stran RS je stav také stabilní. Poslední měsíce ho trápily bolesti zad při kompresivních frakturách obratlů, které vznikly následkem pádů a v terénu osteoporózy při chronické kortikoterapii. Byl dlouho hospitalizován v léčebně dlouhodobě nemocných. Nakonec se mu podařilo zrekonstruovat byt na bezbariérový a pobývá doma.
Fig. 1. MRI examination.
(A) Brain, T2 FLAIR sequence, sagittal scan – multiple hyperintensive lesions in the periventricular white matter of the brain beside the
lateral ventricle – „Dawson fi ngers“ (a typical picture of the distribution of demyelinating lesions in MS).
(B) Cervical spine, T2 STIR sequence, sagittal scan – focal spinal cord hyperintensive lesions at the level of vertebrae C3–4 and at the level
of the intervertebral space Th1–2 – lesions correspond to demyelinating involvement in MS.
(C) Brain, T2 FLAIR sequence, axial scan – hyperintensive focal lesions of the white matter of the brain; one small lesion is frontally on
the right in the juxtacortical localization, several other lesions are bilaterally periventricular, and one lesion is frontally on the left in the
paraventricular white matter of the brain.
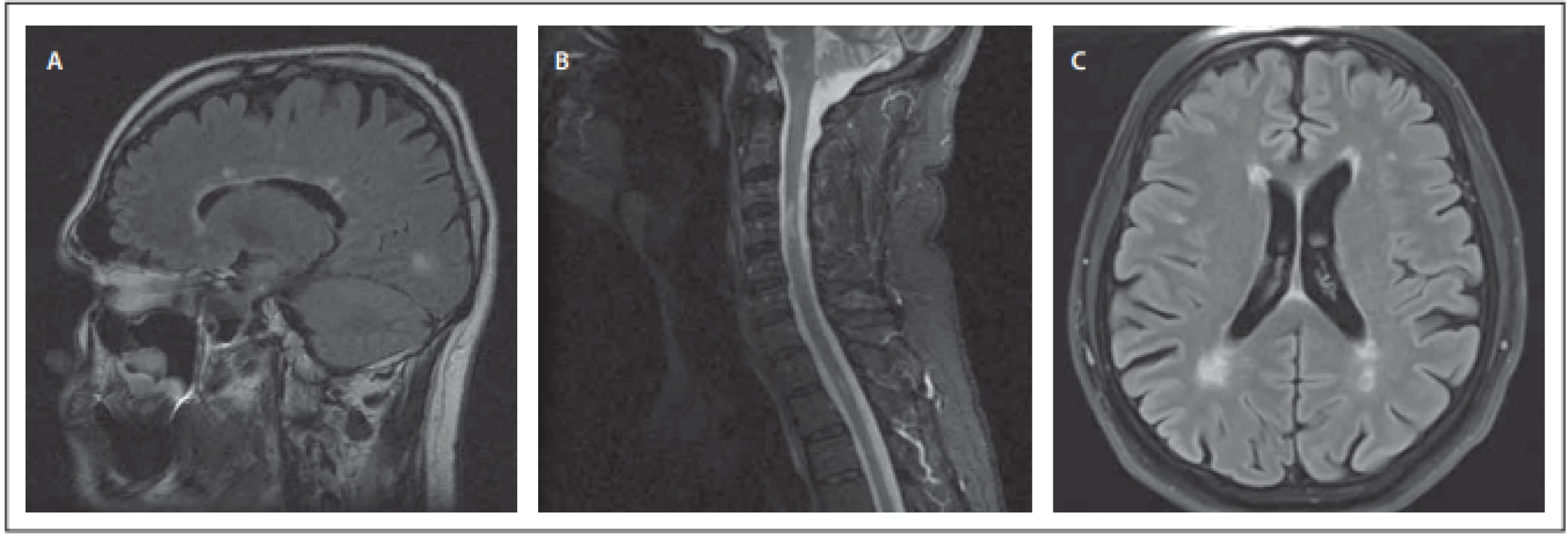
FLAIR – fl uid attenuated inversion recovery; STIR – short tau inversion recovery
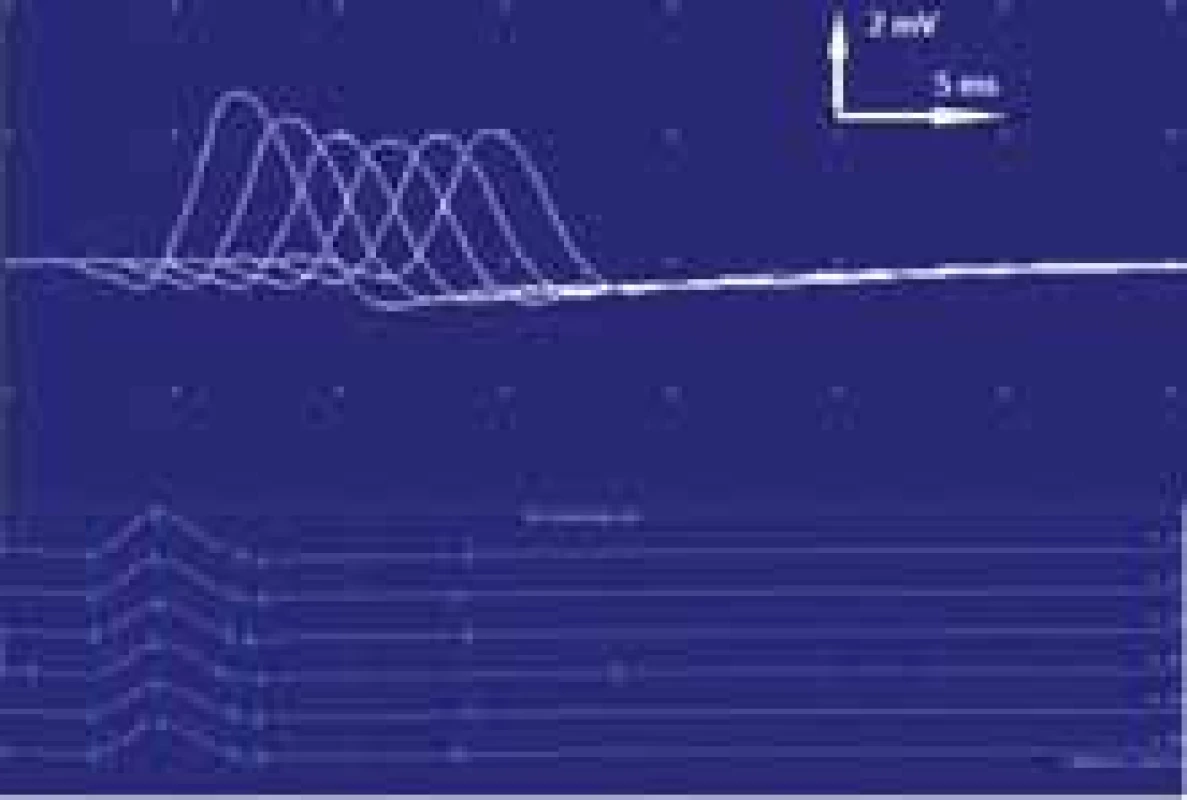
Fig. 2. EMG examination. At repetitive
stimulation (3 Hz), 37% decrement of
the amplitude of the cumulative muscle
action potential from the nasalis muscle,
indicating a transmission disorder on
the postsynaptic neuromuscular disc
and thus supporting the diagnosis of
myasthenia gravis.
Koincidence RS a MG je vzácná, nicméně vyskytuje se častěji, než pokud by se jednalo pouze o náhodnou asociaci. Základním společným rysem je autoimunitní pato geneze obou onemocnění. Z toho vyplývají i obdobné etiopatogenetické mechanizmy. Mezi predispozice obou onemocnění patří faktory genetické i hormonální či nedostatek vitamínu D. Možným spouštěčem pak může být např. infekce či chronický stres interagující s imunitním systémem. MG se může objevit před nebo až po onemocnění RS. Američtí autoři Dehbashi et al v roce 2019 zpracovali rešerši, ve které v literatuře publikované od roku 1980 nalezli 29 kazuistik popisujících koincidenci těchto dvou onemocnění. Ve 26 případech se jednalo o ženy mající mírný průběh obou onemocnění, jaký je pozorován i u našeho nemocného. U třech pacientů došlo k rozvoji MG po léčbě RS interferonem beta, u jednoho nemocného po léčbě glatirameracetátem a alemtuzumabem. Není jisté, zda tyto léky zafungovaly přímo jako spouštěče onemocnění anebo byly u predisponovaných nemocných jen jakýmsi trigger faktorem [5]. Autoři Danikowski et al přikládají zásadní vliv v patogenezi autoimunitních nemocí dysfunkci tzv. Treg lymfocytů, které normálně tlumí funkci CD4+T lymfocytů schopných autoimunitních reakcí, detaily ale přesahují rámec tohoto sdělení [6].
Chtěli jsme upozornit na možnost opomíjené diagnostiky koincidence těchto dvou jednotek při překrytí zvláště bulbární symptomatiky a okulárních příznaků u obou onemocnění.
Mějme tento možný souběh na paměti a neváhejme doplnit příslušná pomocná vyšetření u nemocných s atypickým průběhem MG či RS.
Grantová podpora
Podpořeno MZ ČR – RVO (FNHK, 00179906) a UK (PROGRES Q40). Financováno z projektu IT4Neuro (degeneration), reg. č. CZ.02.1.01/0.0/0.0/18_069/0010054.
MUDr. Pavlína Hemerková
Neurologická klinika LF UK a FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
e-mail: pavlinahemerkova@seznam.cz
Přijato k recenzi: 23. 4. 2020
Přijato do tisku: 25. 11. 2020
Zdroje
1. Vachová M. Současná epidemiologická data roztroušené sklerózy v ČR. Cesk Slov Neurol N 2010; 73/106 (Suppl 2): S124.
2. Piťha J. Klinický obraz myasthenia gravis. In: Piťha J (ed). Myasthenia gravis a ostatní poruchy nervosvalového přenosu. Praha: Maxdorf 2010: 96–114.
3. Špalek P. Myasténia gravis. Cesk Slov Neurol 2008; 71/104 (1): 7–24.
4. Jakubíková M., Piťha J. Současný pohled na imunopatogenezi myasthenia gravis. Cesk Slov Neurol N 2015; 78/111 (6): 649–654.
5. Dehbashi S, Hamouda D, Shanina E. Co-occurrence of multiple sclerosis and myasthenia gravis: a case report and review of immunological theories. Mult Scler Relat Disord 2019; 34: 135–136. doi: 10.1016/j.msard.2019.06.027.
6. Danikowski KM, Jayaraman S, Prabhakar BS. RegulatoryT cells in multiple sclerosis and myasthenia gravis. J Neuroinflammation 2017; 14 (1): 117. doi: 10.1186/s12974-017-0892-8.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2020 Číslo 6
Nejčtenější v tomto čísle
- Progresivní supranukleární obrna
- Supraskapulární neuropatie
- Endoskopické vs. skríninkové vyšetření polykání a jejich vliv na výsledný stav u pacientů po akutní cévní mozkové příhodě
- Encefalopatie při infekci COVID-19 s odezvou na léčbu intravenózními imunoglobuliny
