Časná komplikace ošetření disekujícího intrakraniálního aneuryzmatu ve vertebrobazilárním povodí flow-diverterem
Early complication after treatment of dissecting intracranial aneurysm in vertebrobasilar circulation with a flow-diverter
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study. The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
L. Smetanová 1; D. Krajíčková 2; A. Krajina 3
Působiště autorů:
Rehabilitační klinika FN Hradec Králové
1; Neurologická klinika LF UK a FN, KCC, Hradec Králové
2; Radiologická klinika LF UK a FN, KCC, Hradec Králové
3
Vyšlo v časopise:
Cesk Slov Neurol N 2018; 81(5): 599-601
Kategorie:
Dopis redakci
doi:
https://doi.org/10.14735/amcsnn2018599
Souhrn
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study. The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Vážená redakce,
flow-divertery jsou relativně novou generací stentů k endovaskulárnímu ošetření intrakraniálních aneuryzmat [1,2]. Původně byly určeny k ošetření velkých neprasklých aneuryzmat na arteria carotis interna (ACI) nebo na bazilárních a vertebrálních arteriích, pro fuziformní a disekující aneuryzmata a pro sakulární aneuryzmata se širokým krčkem a s nízkým poměrem vak aneuryzmatu/ krček. Postupně začaly být využívány i pro malá aneuryzmata, aneuryzmata na arteria cerebri anterior a na úsecích M3–M4 arteria cerebri media, rekurentní a prasklá aneuryzmata [1,3]. Existuje řada typů flow-diverterů jako např. PED (Pipeline Embolization Device, Covidien, Mansfield, USA), FRED (Flow Re-direction Endoluminal Device, MicroVention, Tustin, USA), Silk (Balt Extrusion, Montmorency, Francie), p64 (Phoenix, USA) nebo Surpass (Stryker Neurovascular, Fremont, USA). Na rozdíl od embolizace, použití flow-diverteru nevede k okamžité okluzi na konci ošetření, ale dochází k ní až během několika měsíců. Mezi rizika spojená se zavedením flow-diverterů patří in-stent trombóza nebo stenóza (časná i pozdní), okluze vedlejších kortikálních větví nebo perforátorů, perforace cévy, perianeuryzmální edém, klinicky němý nebo symptomatický mozkový infarkt a opožděné intracerebrální nebo subarachnoidální krvácení [1,4,5]. V prevenci in-stent trombózy po zavedení flow-diverteru hraje významnou roli duální protidestičková terapie (klopidogrel v kombinaci s kyselinou acetylsalicylovou), která je zahajována několik dní před plánovaným zavedením stentu a doporučuje se v ní pokračovat 6 týdnů až několik měsíců [6].
Prezentujeme případ 61leté ženy s negativní rodinnou anamnézou, nekuřačku, dispenzarizovanou pro membranózní glomerulonefritidu, arteriální hypertenzi a hypercholesterolemii, která byla ve spádu vyšetřována pro asi měsíc trvající ostrou bolest hlavy na levém temeni a za levým okem narušující její každodenní aktivity i spánek. Vyvolávající příčiny si nebyla vědoma. Praktický lékař a ortoped nezjistili příčinnou patologii, rentgen vedlejších nosních dutin byl s normálním nálezem, úlevu nepřineslo ani ošetření chrupu. MR mozku však detekovala zčásti trombózované aneuryzma velikosti 23 × 16 × 11 mm v blízkosti úseku P1 arteria cerebri posterior (ACP) vlevo, které neurolog pro absenci neurodeficitu hodnotil jako incidentální (obr. 1A). Doplněná DSA mozkových tepen vč. 3D zobrazení potvrdila disekující, nepravidelné, parciálně trombózované aneuryzma úseku P1 ACP vlevo s úzkým krčkem a mírným zúžením P1 v místě krčku (obr. 1B). Po 2denní přípravě duální protidestičkovou léčbou byl do levých segmentů P1– P2 úspěšně zaveden flow-diverter FRED (3 × 19 mm), který byl pro stenózu po zavedení dilatován 2,5mm balonkem (Gateway, Stryker, Fremont, USA) (obr. 1C). Po výkonu byla pacientka standardně zajištěna 72 h Fraxiparinem (Aspen Pharma Trading Limited, Dublin, Irsko). Celkově byla v dobrém stavu s normálními hodnotami krevního tlaku a bez známek cerebrální komplikace. Pátý den po ošetření, v den plánovaného ukončení hospitalizace, se v dopoledních hodinách u pacientky objevila celková slabost s postupným rozvojem centrální parézy n. VII. vpravo a parézy pravé horní končetiny. Navzdory tomu, že urgentně provedené CT a CTA mozku neprokázaly relevantní patologii, začala být nemocná somnolentní a k faciobrachiální pravostranné paréze se přidalo i velmi lehké oslabení pravé dolní končetiny. Po domluvě s intervenčním radiologem byl podán intravenózně Integrilin (Glaxo Operations UK Ltd., Brentford, Velká Británie) a do medikace byl vrácen Fraxiparin v preventivní dávce. Další vývoj byl příznivý, ve večerních hodinách se zlepšilo vědomí i pravostranná hemiparéza. Třetí den od vzniku komplikace byla pacientka při soustavné rehabilitační péči schopna samostatné chůze, avšak přetrvávalo zpomalené psychomotorické tempo. Kontrolní CT mozku sedmý den od komplikace (obr. 2A) zobrazila novou neexpandující hypodenzitu v oblasti levého talamu v průměru cca 20 mm odpovídající subakutní ischemii a zvětšení ztrombózovaného vaku aneuryzmatu v důsledku jeho postupného dotrombózování. Následující den byla pacientka bez neurodeficitu propuštěna domů s doporučením klidového režimu po dobu 2 měsíců, s duální protidestičkovou medikací na 6 týdnů a s doporučením na udržení spíše nižšího krevního tlaku. Kontrolní MRA za 2 měsíce po intervenci potvrdila plnou obliteraci aneuryzmatu (obr. 2B). Šest měsíců po výkonu byla pacientka bez nové neurologické symptomatiky.
Fig. 1. Partially thrombosed aneurysm (size 23 × 16 × 11 mm) near the P1 section of the cerebral posterior artery before treatment
(A – MRI, B – DSA). C – control DSA of aneurysm after successful endovascular treatment with a flow-diverter.
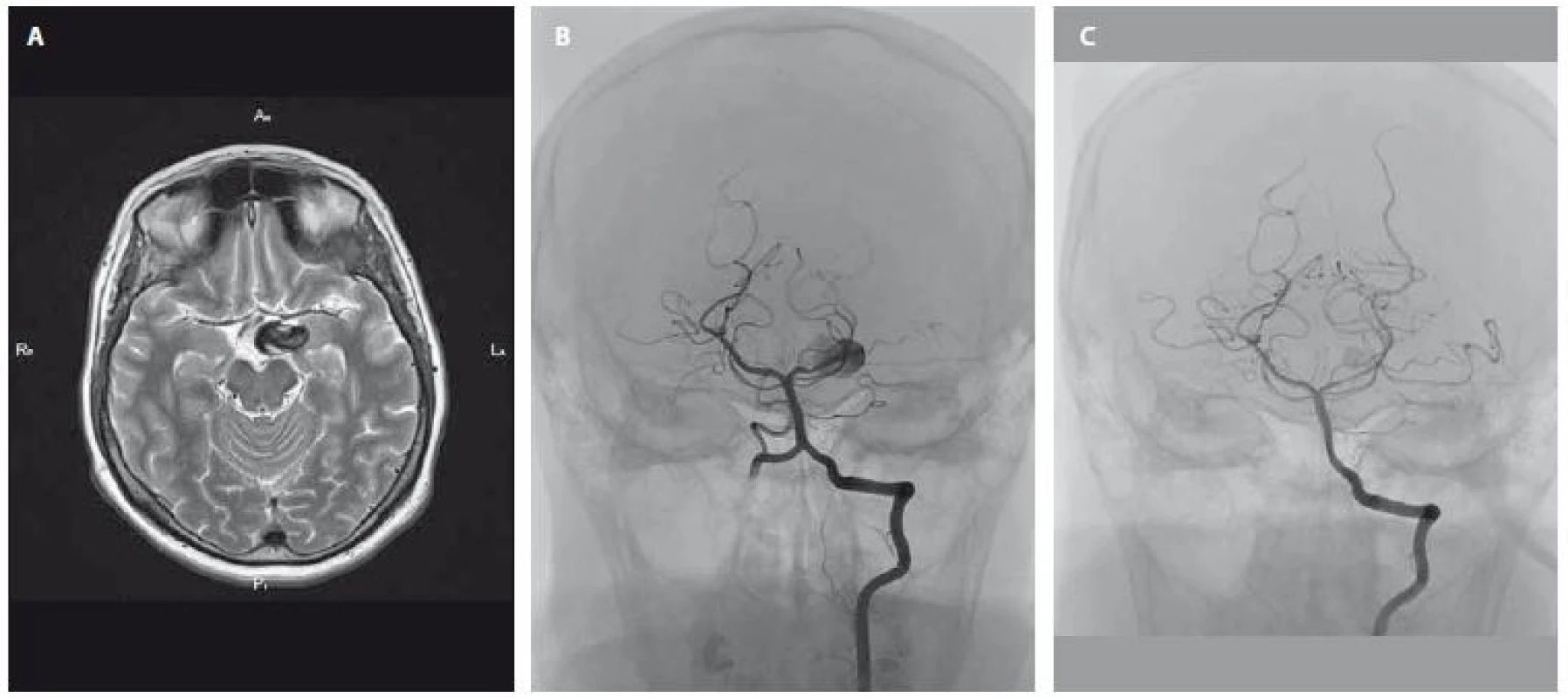
Fig. 2. A – Control brain CT on the 7th day from a complication with a new non-expanding hypodensity in the left thalamic area, approximately 20 mm in diameter, corresponding with subacute ischaemia. B – Control MRA 2 months after intervention with full aneurysm obliteration.
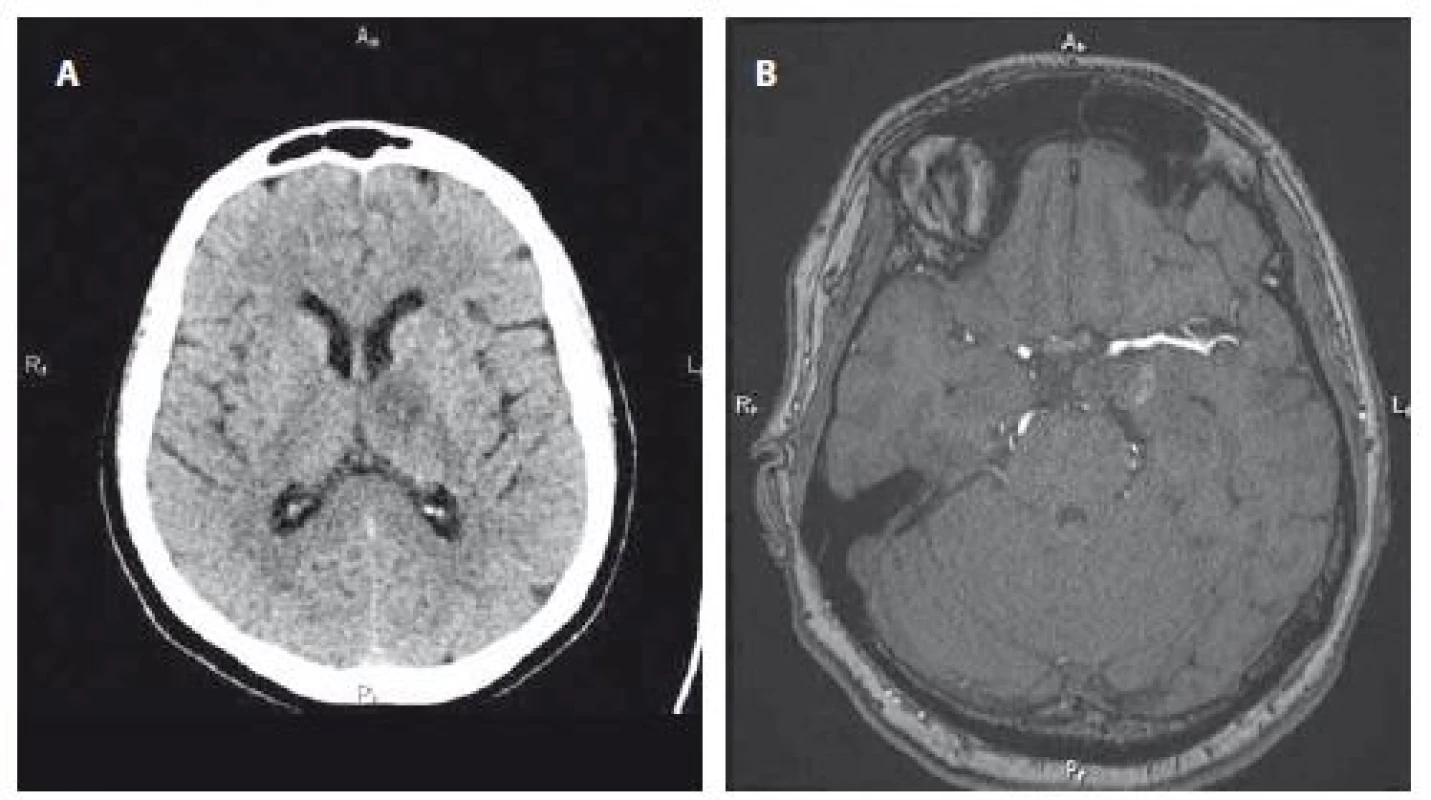
Léčba aneuryzmat v přední cirkulaci s použitím flow-diverterů, především aneuryzmat na ACI, se v komplexních cerebrovaskulárních centrech stala běžnou praxí. Použití flow-diverterů pro léčbu aneuryzmat v zadní cirkulaci však stále zůstává více rizikové pro signifikantně vyšší procento komplikujících mozkových ischemií. Zavedením flow-diverteru (speciálního hustě pleteného stentu) do místa přechodu mateřské cévy a aneuryzmatu dochází k „odklonění toku“ krve z aneuryzmatu, což následně vede k trombóze aneuryzmatu v čase. Zároveň flow-divertery poskytují kostru pro přerůstání endotelu a tím k hojení a rekonstrukci mateřské cévy, ve většině případů se zachováním perforátorů a vedlejších kortikálních větví [2,5]. Po zavedení flow-diverteru FRED bylo kompletní okluze dosaženo po 3 měsících u 42 %, po 6 měsících u 88 % a po 12 měsících u 96 % aneuryzmat [7]. Statisticky významnými rizikovými faktory jsou gigantická, fuziformní a disekující aneuryzmata, periferní lokalizace aneuryzmat a aneuryzmata v zadní cirkulaci [1,5,8]. Posledně jmenovaná aneuryzmata mají mnohem vyšší riziko mortality, ischemické příhody a infarktů v povodí perforátorů [5]. Ischemické komplikace vznikají jako následek tvorby trombu na stěně stentu, který vede k okluzi mateřské cévy, vedlejších větví, perforátorů nebo vzdálené trombembolické příhodě.
U námi prezentované pacientky šlo o ošetření disekujícího, poměrně velkého aneuryzmatu v zadní cirkulaci (úseku P1 ACP), tj. o rizikové aneuryzma. Příčinou talamického infarktu, který vznikl 5. den po zavedení flow-diverteru, byl pravděpodobně uzávěr ipsilaterálních paramediánních perforátorů odstupujících z proximálního úseku ACP. V literatuře jsou popsány případy mozkových ischemií při uzávěru těchto paramediánních arterií [9]. Percheron popsal několik typů odstupů těchto paramediánních arterií, přičemž u nejčastějšího typu 1 odstupuje z každé ACP jedna paramediánní talamická arterie zásobující ipsilaterální talamus [10].
Závěrem lze shrnout, že popsaný endoluminální přístup, kdy vak aneuryzmatu nemusí být ošetřen, eliminuje riziko intraprocedurálního prasknutí aneuryzmatu. V zadní cirkulaci je však spojen s vyšším rizikem ischemických komplikací. Tento přístup také zcela neeliminuje možnost opakovaného krvácení z aneuryzmatu. K prevenci in-stent trombózy je zásadní podávání duální protidestičkové terapie před výkonem a po něm [6].
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Libuše Smetanová, Ph.D.
Rehabilitační klinika FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
e-mail: libuse.smetanova@fnhk.cz
Přijato k recenzi: 16. 5. 2018
Přijato do tisku: 14. 8. 2018
Zdroje
1. Briganti F, Leone G, Marseglia M et al. Endovascular treatment of cerebral aneurysms using flow-diverter devices: a systematic review. Neuroradiol J 2015; 28(4): 365– 375. doi: 10.1177/ 1971400915602803.
2. Jiang B, Paff M, Colby GP et al. Cerebral aneurysm treatment: modern neurovascular techniques. Stroke Vasc Neurol 2016; 1(3): 93– 100. doi: 10.1136/ svn-2016-000027.
3. Kocer N, Islak C, Kizilkilic O et al. Giant intracranial aneurysm: a case-based atlas of imaging and treatment. Istanbul: Springer 2016.
4. Patzig M, Forbrig R, Ertl L et al. Intracranial aneurysms treated by flow-diverting stents: long-term follow-up with contrast-enhanced magnetic resonance angiography. Cardiovasc Intervent Radiol 2017; 40(11): 1713– 1722. doi: 10.1007/ s00270-017-1732-z.
5. Wang CB, Shi WW, Zhang GX et al. Flow diverter treatment of posterior circulation aneurysms. A meta-analysis. Neuroradiology 2016; 58(4): 391– 400. doi: 10.1007/ s00234-016-1649-2.
6. Prabhakaran S, Wells KR, Lee VH et al. Prevalence and risk factors for aspirin and clopidogrel resistance in cerebrovascular stenting. AJNR Am J Neuroradiol 2008; 29(2): 281– 285. doi: 10.3174/ ajnr.A0818.
7. Briganti F, Leone G, Cirillo L et al. Postprocedural, midterm, and long-term results of cerebral aneurysms treated with flow-diverter devices: 7-year experience at a single center. Neurosurg Focus 2017; 42(6): E3. doi: 10.3171/ 2017.3.FOCUS1732.
8. Lv X, Yang H, Liu P et al. Flow-diverter devices in the treatment of intracranial aneurysms: a meta-analysis and systematic review. Neuroradiol J 2016; 29(1): 66– 71. doi: 10.1177/ 1971400915621321.
9. Šustrová Z, Černík D, Beneš J et al. Oboustranná ischemie paramediálního thalamu a Percheronova arterie. Ces Radiol 2018; 72(2): 90– 95.
10. Percheron G. The anatomy of the arterial supply of the human thalamus and its use for the interpretation of the thalamic vascular pathology. Z Neurol 1973; 205(1): 1– 13.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2018 Číslo 5
Nejčtenější v tomto čísle
- Nové poznatky v diagnostice a léčbě amyotrofické laterální sklerózy
- Přehled onemocnění s obrazem restrikce difuze na magnetické rezonanci mozku
- Cervikální vertigo – fikce či realita?
- Anestezie a nervosvalová onemocnění
