Stanovení prognostických faktorů trombolytické léčby u pacientů s akutním mozkovým infarktem – analýza registru SITS
Identification of Prognostic Factors for Thrombolytic Therapy in Patients with Acute Stroke – Analysis of the SITS Registry
Determination of predictors of a favourable outcome in patients treated with thrombolytic therapy for acute stroke, analysis of the SITS (Safe Implementation of Treatments in Stroke) Registry.
Background:
Identification of predictors of a favourable outcome in stroke patients treated with thrombolysis might help in determining their prognosis and individualizing treatment. The aim of our study was to identify predictors of a favourable outcome in stroke patients treated with systemic thrombolysis.
Method:
We analyzed data entered in the SITS Registry (Safe Implementation of Treatments in Stroke) in the Czech Republic between February 2003 and February 2010. Univariate and multivariate regressive analyses were used to identify predictors of a favourable outcome as defined by the modified Rankin scale 0–1 at 3 months.
Results:
Overall in the Czech Republic, 3,053 patients were treated with intravenous thrombolysis. A total of 462 (15%) patients died and 1,308 (43%) achieved a favourable outcome. Symptomatic intracerebral haemorrhages (as per the SITS definition) were observed in 62 (2%) patients. Multivariate analyses identified the following characteristics to be significantly associated with a favourable outcome: age (10-year increments) – OR 0.90, 95% CI (0.83–0.97); systolic blood pressure (10 mmHg increments) – OR 0.92, 95% CI (0.88–0.97); stroke severity at baseline measured by NIHSS score (5-point increments) – OR 0.52, 95% CI (0.47–0.56); glucose (5 mmol/L increments) – OR 0.61, 95% CI (0.51–0.73) and diagnosis of embolic etiology of stroke (I63.4 according to the International Classification of Diseases) – OR 0.75, 95% CI (0.62–0.90).
Conclusion:
In our study, we identified several important prognostic predictors determining a clinical outcome of stroke patients treated with intravenous thrombolysis in the Czech Republic. Knowledge of these predictors allows clinicians to predict patient prognosis and manage risk factors.
Key words:
ischemic stroke – intravenous thrombolysis – predictors – outcome
Autoři:
M. Bar 1; P. Kadlecová 2; D. Václavík 3; J. Neumann 4; O. Škoda 5; R. Mikulík 6
Působiště autorů:
Neurologická klinika LF OU a Fakultní nemocnice Ostrava
1; Mezinárodní centrum klinického výzkumu (ICRC), FN u sv. Anny v Brně
2; Neurologické oddělení, Iktové centrum Vítkovické nemocnice a. s., Ostrava
3; Neurologické oddělení, Krajská zdravotní, a. s. – Nemocnice Chomutov, o. z.
4; Neurologické oddělení, Nemocnice Jihlava a Neurologická klinika 3. LF UK a FN Královské Vinohrady, Praha
5; Mezinárodní centrum klinického výzkumu (ICRC), Neurologická klinika LF MU a FN u sv. Anny v Brně
6
Vyšlo v časopise:
Cesk Slov Neurol N 2012; 75/108(4): 426-431
Kategorie:
Původní práce
Souhrn
Úvod:
Identifikace faktorů ovlivňujících výsledný stav pacientů po trombolýze umožňuje stanovit prognózu v časné fázi cévní mozkové příhody a ovlivnit léčbu. Cílem naší práce proto bylo zjištění prognostických ukazatelů příznivého výsledného klinického stavu pacientů s mozkovým infarktem léčených pomocí systémové trombolýzy.
Metodologie:
Byly zpracovany údaje vložené do SITS registru (Safe Implementation of Treatments in Stroke) z České republiky v období 2/2003–2/2010 s cílem určit pomocí uni- a multivariabilní regresní analýzy ukazatele příznivého výsledného klinického stavu, definovaného v modifikované Rankinově škále 0–1 bodem.
Výsledky:
V letech 2003 až 2010 bylo v České republice dle registru SITS léčeno systémovou trombolýzou celkem 3 053 pacientů. Celkově 462 (15 %) pacientů zemřelo a dobrého klinického stavu bylo dosaženo u 1 308 (43 %) pacientů. Symptomatické intracerebrální krvácení podle definice SITS proběhlo u 62 (2 %) pacientů. Při multivariabilní analýze byly významně asociovány s příznivým výsledným stavem pacientů následující faktory: věk (zvyšující se po 10 letech) – OR 0,90; 95% CI (0,83–0,97); systolický krevní tlak (zvyšující se po 10 mmHg) – OR 0,92; 95% CI (0,88–0,97); vstupní klinický stav pacienta měřený dle NIHSS (zvyšující se po 5 bodech škály) – OR 0,52; 95% CI (0,47–0,56); hladina glykemie (zvyšující se o 5 mmol/L) – OR 0,61, 95% CI (0,51–0,73) a diagnóza embolické mozkové ischemie (I63.4 dle Mezinárodní klasifikace nemocí) – OR 0,75; 95% CI (0,62–0,90).
Závěr:
V naší práci jsme identifikovali několik významných prognostických faktorů ovlivňujících výsledný klinický stav pacientů léčených systémovou trombolýzou v ČR. Znalost těchto prediktorů umožňuje klinikovi určit prognózu pacienta léčeného systémovou trombolýzou a ovlivnit léčbu rizikových faktorů.
Klíčová slova:
mozková ischemie – trombolytická lečba – prognostické faktory – výsledný stav
Poděkování
Poděkování patří všem lékařům a dalším pracovníkům, kteří mnoho let a bez nároku na odměnu ukládají údaje do SITS registru. Tato publikace je věnována především jim. Pro možnosti další analýzy a případné publikace z registru SITS kontaktujte národního koordinátora registru SITS Roberta Mikulíka (mikulik@hotmail.com).
Seznam spolupracovníků SITS Česká republika (v abecedním pořadí): Zdena Bajková, Ludmila Bláhová, Kateřina Blejchařová, Henryk Brzeżański, Helena Dvořáková, Jan Fajstauer, Jan Fiksa, Petr Geier, Emanuela Habrovanská, Lenka Hajduková, Monika Holíková, Pavel Houška, Květa Chotětovská, Jana Jankových, Jan Kábrt, Jana Kadlčíková, Lukáš Klečka, Sylva Klimešová, Ondřej Kočí, Stanislav Kopecký, Vladislav Kopecký, Lenka Kouřilová, Martin Koutný, Martin Kovář, Martin Krobot, Barbora Křiváková, Marian Kuchár, Ctirad Lakomý, Alena Lapáčková, Jiří Loučka, Aleš Novák, Jiří Neumann, Tomáš Peisker, Marek Pernička, Stanislav Peška, František Pfeifer, Richard Plný, Petr Procházka, Martin Roubec, Jaroslav Říman, Daniel Šaňák, Petr Ševčík, Vladimir Šigut, David Školoudík, Stanislav Slavík, Jiří Stehlík, Petr Štěpán, Martin Vančura, Helena Vančurová, Peter Vaško, Květoslava Večeřová, Milada Urbančíková.
Úvod
Rekanalizační terapie pomocí systémové trombolýzy (IVT) do 4,5 hodiny snižuje počet hendikepovaných pacientů až o 30 % [1–4]. Nebylo prokázáno, že by IVT v časovém okně do 4,5 hodiny byla u některých pacientů neúčinná. Na druhé straně byla identifikována řada faktorů ovlivňujících prognózu, např. čas od vzniku onemocnění k léčbě, vstupní stav pacientů, věk, přítomnost mozkové ischemie na CT mozku, vysoký systolický tlak, hladina glykemie, zlepšující se klinický stav v průběhu akutní léčby a rekanalizace cévy [5–8].
Identifikovat faktory ovlivňující výsledný stav pacientů po trombolýze je důležité, protože jejich znalost umožňuje stanovit prognózu v časné fázi iktu, pomůže určit patofyziologické mechanizmy průběhu mozkového infarktu a ovlivnit léčbu. Kromě analýzy vlivu velikosti objemu ischemie měřené pomocí magnetická rezonance (MR), difuzně vážených obrazů nebo vlivu prodloužení terapeutického okna na klinický stav [9,10] údaje o prediktorech výsledného stavu po trombolýze v ČR nejsou dostupné. Cílem naší práce bylo zjištění prognostických ukazatelů příznivého výsledného klinického stavu pacientů s mozkovým infarktem léčených pomocí systémové trombolýzy v období mezi 2/2003 a 2/2010 v České republice.
Soubor a metodika
Klinická a demografická data pacientů léčených systémovou trombolýzou v České republice jsou ukládána dle jednotného protokolu do registru SITS. Registr SITS je prospektivní mezinárodní internetový registr, který shromažďuje data pacientů léčených systémovou trombolýzou [11].
Všichni pacienti vložení do registru prodělali akutní mozkový infarkt a byli léčeni IVT – tkáňovým plazminogenem (tPA) alteplázou (Actilyse, Boehringer Ingelheim, Germany) v dávce 0,9 mg/kg. Terapeutické okno bylo na základě výsledku studie ECAS III (The European Cooperative Acute Stroke Study) prodlouženo z původních 3 hodin od vzniku mozkové ischemie na 4,5 hodiny v září 2008 [4]. Závažnost neurologického deficitu při přijetí byla hodnocena podle National Institute of Health Stroke Scale (NIHSS) škály. Konečný výsledný klinický stav pacientů byl měřen pomocí modifikované Rankinovy škály (mRS) za 90 dní od počátku onemocnění. Příznivý výsledek léčby byl definován jako mRS skóre v rozmezí 0–1. Všichni pacienti podstoupili vstupní vyšetření CT mozku k potvrzení diagnózy a kontrolní CT za 24–48 hodin po IVT k vyloučení intracerebrální hemoragie.
Následující proměnné charakteristiky byly dokumentovány a použity pro analýzu prognostických faktorů dobrého výsledného klinického stavu: věk, pohlaví, anamnéza rizikových faktorů (hypertenze, diabetes mellitus, hyperlipidemie, kouření, prodělaná CMP v minulosti, fibrilace síní, městnavé srdeční selhání), užívání protidestičkové terapie, mRS skóre před CMP, výchozí skóre NIHSS, hodnota systolického krevního tlaku, hladina krevního cukru, hmotnost pacientů, celková dávka tPA, čas do zahájení léčby od nástupu příznaků, čas od přijetí pacienta do nemocnice k zahájení léčby, přítomnost časných ischemických změn na CT nebo MR mozku. Dále byla posuzována etiologická diagnóza mozkové ischemie, skutečnost, jestli léčba proběhla v pracovní době (8–16 hodin, po–pá) a léčba po prvním říjnu 2008, kdy došlo k prodloužení terapeutického okna na 4,5 hodiny.
Hlavními klinickými sledovanými ukazateli jsou v registru SITS přítomnost symptomatického intracerebrálního krvácení (SICH) podle tří definicí (dle definice SITS, dle definice NINDS a dle definice ECASS II) [6], mortalita a konečný výsledný klinický stav pacienta hodnocený dle mRS ve třech měsících od mozkového infarktu. Symptomatické intracerebrální krvácení podle SITS je definováno jako lokální nebo vzdálené parenchymové krvácení typu 2 na CT mozku, zjištěné mezi 22–36 hod po léčbě v kombinaci se zhoršením neurologického deficitu ≥ 4 body NIHSS ve srovnání s výchozím stavem, nebo intracerebrální krvácení vedoucí ke smrti.
Statistická analýza
Deskriptivní statistika posloužila pro charakteristiku všech pacientů. Následující parametry byly použity pro zjištění ukazatelů úspěšnosti příznivého výsledného klinického stavu (mRS za 3 měsíce 0–1):
- a) demografická a klinická data: věk, pohlaví, přítomnost rizikových faktorů, užívání antiagregační terapie, skóre mRS před CMP, výchozí skóre NIHSS, hodnota systolického krevního tlaku, hladina krevního cukru, hmotnost pacientů, celková dávka tPA, přítomnost časných ischemických změn na CT/MR mozku a konečná etiologická diagnóza mozkové ischemie.
- b) organizační parametry: čas do zahájení léčby od nástupu příznaků, čas od přijetí pacienta do nemocnice k zahájení léčby, skutečnost, že léčba proběhla v pracovní době (8–16 hodin, po–pá) a léčba po prvním říjnu 2008.
Statistická významnost jednotlivých ukazatelů úspěšnosti výsledného klinického stavu byla testována pomocí uni- a multivariabilní logistické regresní analýzy. Proměnné, které dosáhly hladiny významnosti p < 0,1 v univariabilní analýze, byly následně použity pro testování v multivariabilní analýze. Hladina statistické významnosti v konečném modelu byla určena jako p < 0,05.
Výsledky
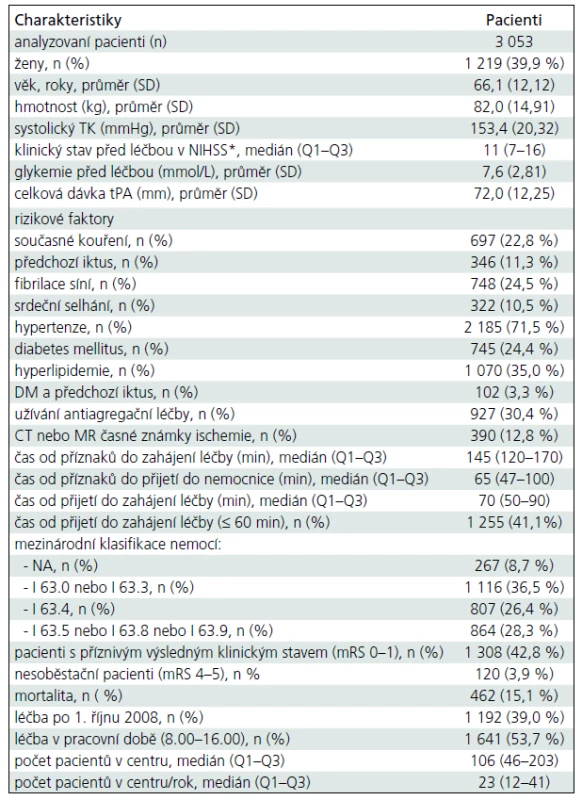
V letech 2003–2010 bylo v České republice dle registru SITS léčeno systémovou trombolýzou celkem 3 053 pacientů. V terapeutickém okně do 3 hodin od vzniku příznaků 1 861 (61 %) pacientů a od 1. 10. 2008, po prodloužení terapeutického okna na 4,5 hodiny, 1 192 (39 %). Mimo pracovní dobu bylo léčeno 1 412 (47 %) pacientů. Demografická a vstupní klinická data pacientů ukazuje tab. 1. Dobrého klinického stavu hodnoceného v modifikované škále mRankin 0–1 bylo dosaženo u 1 308 (43 %) pacientů. Celkem 120 (4 %) pacientů zůstalo nesoběstačných (mRS 4–5) a 462 (15 %) pacientů zemřelo. K symptomatickému intracerebrálnímu krvácení dle definice SITS došlo u 62 (2 %) pacientů.
Tab. 2 ukazuje vliv jednotlivých sledovaných ukazatelů na příznivý výsledný stav (mRS ≤ 1) hodnocený pomocí uni- a multivariabilní logistické regresní analýzy. Při multivariabilní analýze byly významně asociovány s příznivým výsledným stavem pacientů následující faktory: věk (zvyšující se po 10 letech) – OR 0,90; 95% CI (0,83–0,97); systolický krevní tlak (zvyšující se po 10 mmHg) – OR 0,92; 95% CI (0,88–0,97); vstupní klinický stav pacienta měřený dle NIHSS (zvyšující se po 5 bodech škály) – OR 0,52; 95% CI (0,47–0,56); hladina glykemie (zvyšující se o 5 mmol/L) – OR 0,61; 95% CI (0,51–0,73) a diagnóza embolické mozkové ischemie (I63.4 dle Mezinárodní klasifikace nemocí) – OR 0,75; 95% CI (0,62–0,90).
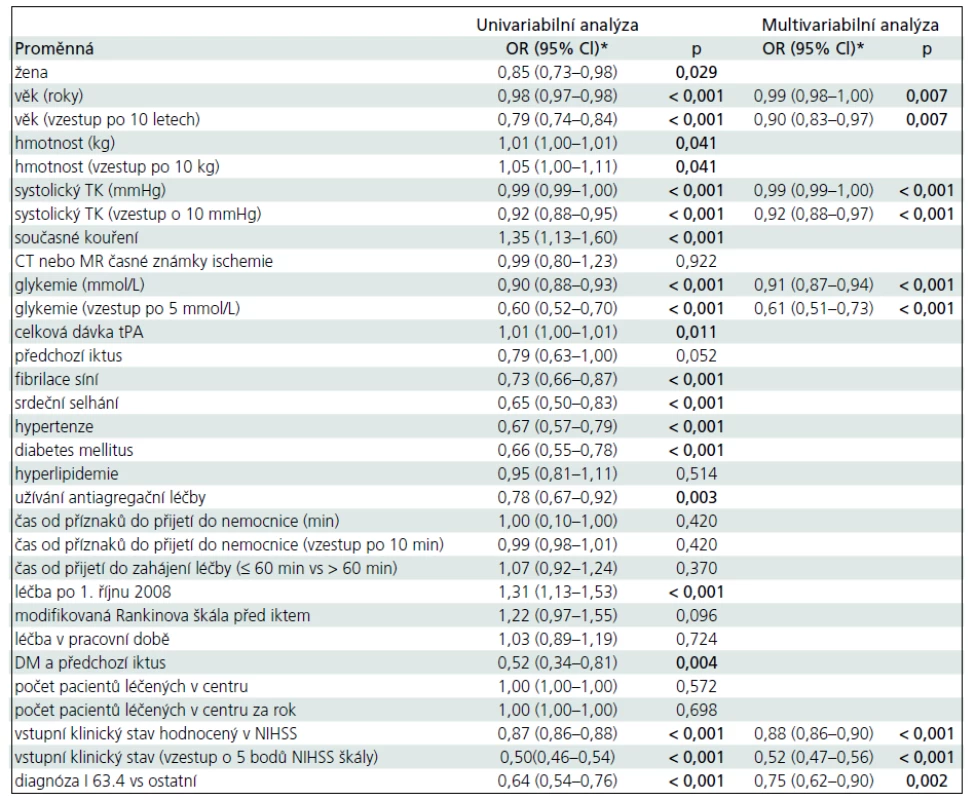
Diskuze
V naší práci jsme identifikovali následující nezávislé faktory, které ovlivňují prognózu pacientů léčených trombolýzou v ČR pro akutní mozkový ischemický infarkt: věk, vstupní systolický krevní tlak a hladina glykemie, vstupní klinický stav pacienta hodnocený v škále NIHSS a embolická etiologie mozkové ischemie. Naše výsledky podporují již dříve publikované prognostické faktory léčby IVT, z nichž nejvýznamnější prací byla analýza všech dat mezinárodního registru SITS. V této analýze věk, vysoká hladina glukózy, vstupní klinický stav pacienta měřený v škále NIHSS a přítomnost mozkového infarktu na vstupním CT byly nezávisle asociovány s nepříznivým výsledným klinickým stavem [6,11].
Zatímco výše uvedená data potvrzují výsledky studií z jiných zemí, naše analýza poskytuje některé zajímavé údaje specifické pro ČR. Zajímavé je např. zjištění, že pouze 13 % pacientů, kteří měli jasné známky časné ischemie na CT mozku, bylo indikováno k IVT v ČR ve srovnání s 24 % pacientů v mezinárodním registru SITS. Tento údaj svědčí o opatrném přístupu k indikaci k IVT u pacientů s časnými známkami mozkové ischemie na CT v ČR. Tento postoj lékařů není správný, protože přítomnost časných ischemických změn na CT neovlivňuje účinnost trombolýzy. Jinými slovy, nepodání trombolýzy těmto pacientům ještě zhorší jejich prognózu, která je v důsledku přítomnosti časných známek ischemie nepříznivá. Argumentem proti jednoznačnému doporučení podat IVT je, že přítomnost časných známek ischemie zvyšuje riziko symptomatického krvácení dle definice RCT (Randomized Control Trial) [6].
V ČR též celkový počet registrovaných pacientů a počet pacientů léčených mimo pracovní dobu svědčí o kvalitní organizaci péče o CMP v naší zemi. Celkem bylo léčeno mimo pracovní dobu 47 % pacientů a tento počet výrazně převyšuje počty léčených pacientů v mezinárodním registru SITS nebo v registrech jednotlivých zemí [6,11–13].
Například ve Velké Británii pouze necelá 4 % pacientů byla léčena mimo pracovní dobu [14]. Navíc skutečnost, že pacienti byli léčeni mimo pracovní dobu, neovlivnila v našem souboru negativně výsledný klinický stav.
Faktor, který vedle vstupního klinického stavu nejvíce ovlivňoval prognózu pacientů v našem souboru, byla hladina glykemie. Každé zvýšení glykemie o 5 mmol/l snižovalo šanci na dosažení příznivého výsledného stavu o 39 %. Hladina glykemie byla i nezávislým prediktorem výsledného stavu v publikovaných studiích, ale nedosáhla tak významných prediktivních hodnot [6,15]. Ribo et al prokázali, že hyperglykemie ovlivňuje nejenom výsledný klinický stav pacientů, ale také růst ischemie v průběhu akutní fáze CMP měřený pomocí difuzně vážených MR snímků a rekanalizační čas [16,17]. Existuje několik vysvětlení účinků hyperglykemie na ischemický mozek. Teorie hyperosmolární se opírá o fakt, že hyperglykemie zvyšuje osmolalitu krve, a tím způsobuje zhoršení prokrvení postižené tkáně. Teorie metabolická se opírá o aktivaci N-metyl--d-aspartát (NMDA) receptorů, která je následována vstupem kalcia do buněk a vznikem lokálního edému [18]. Zánětlivá teorie argumentuje aktivací oxidativního stresu a zánětu při hyperglykemii [19,20]. Bylo prokázáno, že 30–50 % pacientů před zahájením a v průběhu IVT má hyperglykemii, která snižuje účinnost tPA [20,21]. European Stroke Organization doporučuje snížit hladinu glykemie do hodnoty 140 mg/dL (7,7 mmol/l) před zahájením IVT [22]. Data z randomizovaných studií s inzulinem aplikovaným před IVT a v jejím průběhu jsou potřebná k jasnému doporučení léčby hyperglykemie [20,21,23].
Vysoký věk je nezávislý prediktor mortality a invalidity u pacientů se všemi typy CMP [24]. Z naší analýzy vyplývá, že každá dekáda zvyšuje riziko následné invalidity po mozkovém infarktu o 10 %. To ovšem neznamená, že by starší pacienti měli být z IVT vyloučeni. I přes obecně nepříznivý vliv vyššího věku na výsledný klinický stav byla prokázána vyšší účinnost trombolytické léčby starších pacientů ve srovnání se stejně starými pacienty neléčenými IVT [8,24,25].
Průměrný naměřený systolický tlak před aplikací IVT dosáhl u našich pacientů hodnoty 153 mmHg. Naše práce prokázala, že pacienti s hodnotou systolického TK o 10 mmHg nižší měli o 7 % vyšší šanci na dosažení mRS 0–1. Tento nález odpovídá analýze pacientů z mezinárodního registru SITS, kde optimální hodnoty systolického TK v období prvních 24 hodin po IVT byly v rozmezí 141–150 mmHg [5]. Zda by měl být systolický TK vyšší než 150 mmHg snižován do hodnot 141–150 mmHg není jasné. Studie u pacientů neléčených trombolýzou ukázaly, že takové snížení krevního tlaku pacientům nepřináší prospěch [26]. Do doby provedení randomizovaných klinických studií proto platí, že u pacientů léčených IVT snižujeme krevní tlak pod hodnoty 185/110 mmHg [27].
Vstupní klinický stav je ve všech publikovaných studiích uváděn jako silný prediktor nepříznivého výsledného klinického stavu [6,9,12–15]. Vstupní hodnota NIHSS pacientů léčených v ČR byla identická s pacienty v mezinárodním registru (medián NIHSS 11, IQR 8–17). Z naší analýzy vyplývá, že pacienti s hodnotou ve škále NIHSS o 5 bodů vyšší měli o 48 % nižší šanci dosáhnout příznivého klinického stavu!
Posledním významným prognostickým faktorem byla embolická diagnóza mozkové ischemie, která zvyšovala šanci na nepříznivý výsledný stav o 25 % ve srovnání s ostatní etiologií CMP.
Limitací této práce je skutečnost, že údaje z registru mohou podléhat selekčnímu bias. Protože je ale v ČR do registru zařazováno velké množství pacientů a na registru participuje naprostá většina trombolytických center, je přítomnost selekčního bias krajně nepravděpodobná a určitě nižší než na úrovni celého SITS registru. Druhou potenciální limitací je, že údaje z České republiky nebylo možné validně srovnat s údaji z jiných zemí, protože rozdíly ve vstupních parametrech by vyžadovaly adjustaci na tyto parametry. SITS Česká republika ale není vlastníkem údajů z jiných zemí (a naopak), takže taková adjustace se nedala provést.
Hlavní předností této práce je, že existuje pouze velmi málo zemí na světě, které by měly tak systematickým způsobem a v takovém rozsahu jako Česká republika zmapovánu trombolytickou terapii pacientů s akutním mozkovým infarktem.
Závěr
V naší práci jsme identifikovali několik významných prognostických faktorů ovlivňujících výsledný klinický stav pacientů léčených systémovou trombolýzou v České republice. Jsou jimi: hladina glykemie a hodnota systolického tlaku před zahájením léčby, věk, vstupní klinický stav hodnocený v škále NIHSS a embolická etiologie mozkové ischemie. Znalost prediktorů výsledného klinického stavu pomůže klinikovi určit prognózu pacienta léčeného systémovou trombolýzou v časné fázi mozkového infarktu a ovlivnit rozhodování o léčbě rizikových faktorů.
Zdroje podpory formou grantů, přístrojového vybavení nebo léků: R. Mikulík a P. Kadlecová jsou podporováni z Evropského fondu regionální rozvoje – Projekt FNUSA-ICRC (No. CZ.1.05/1.1.00/02.0123).
MUDr. Michal Bar, Ph.D.
Neurologická klinika LF OU a Fakultní nemocnice
Třída 17. listopadu 1790
708 52 Ostrava
e-mail: michal.bar@fno.cz
Přijato k recenzi: 28. 11. 2011
Přijato do tisku: 20. 1. 2012
Zdroje
1. Goldemund D, Mikulik R. Reperfusion therapies for acute ischemic stroke. Curr Treat Options Neurol 2010; 12(2): 155–166.
2. Bar M, Sandercock P, Skoloudik D, Prochazka V. Should mechanical embolectomy devices be used in routine clinical practice? J Neural Transm 2011; 118(8): 1131–1138.
3. Wahlgren N, Ahmed N, Dávalos A, Hacke W, Millán M, Muir K et al. Thrombolysis with alteplase 3–4.5 h after acute ischaemic stroke (SITS-ISTR): an observational study. Lancet 2008; 372(9646):
1303–1309.
4. Hacke W, Kaste M, Bluhmki E, Brozman M, Dávalos A, Guidetti D et al. Thrombolysis with alteplase 3 to 4.5 hours after acute ischemic stroke. N Engl J Med 2008; 359(13): 1317–1329.
5. Ahmed N, Wahlgren N, Brainin M, Castillo J, Ford GA, Kaste M et al. Relationship of blood pressure, antihypertensive therapy, and outcome in ischemic stroke treated with intravenous thrombolysis: retrospective analysis from Safe Implementation of Thrombolysis in Stroke-International Stroke Thrombolysis Register (SITS-ISTR). Stroke 2009; 40(7): 2442–2449.
6. Wahlgren N, Ahmed N, Eriksson N, Aichner F, Bluhmki E, Dávalos A et al. Multivariable analysis of outcome predictors and adjustment of main outcome results to baseline data profile in randomized controlled trials: Safe Implementation of Thrombolysis in Stroke-MOnitoring STudy (SITS-MOST). Stroke 2008; 39(12): 3316–3322.
7. Kharitonova T, Mikulik R, Roine RO, Soinne L, Ahmed N, Wahlgren N et al. Association of early National Institutes of Health Stroke Scale improvement with vessel recanalization and functional outcome after intravenous thrombolysis in ischemic stroke. Stroke 2011; 42(6): 1638–1643.
8. Mishra NK, Ahmed N, Andersen G, Egido JA, Lindsberg PJ, Ringleb PA et al. Thrombolysis in very elderly people: controlled comparison of SITS International Stroke Thrombolysis Registry and Virtual International Stroke Trials Archive. BMJ 2010; 341: c6046.
9. Sanak D, Herzig R, Zapletalova J, Horak D, Kral M, Skoloudik D et al. Predictors of good clinical outcome in acute stroke patients treated with intravenous thrombolysis. Acta Neurol Scand 2011; 123(5): 339–344.
10. Sanak D, Herzig R, Hubacek R, Kral M, Veverka T, Zapletalova J et al. Rozšíření terapeutického časového okna pro intravenózní trombolýzu by nemělo vést k prodloužení „door-to-needle time“ intervalu. Cesk Slov Neurol N 2011; 74/107(6): 685–688.
11. Wahlgren N, Ahmed N, Dávalos A, Ford GA, Grond M, Hacke W et al. Thrombolysis with alteplase for acute ischaemic stroke in the Safe Implementation of Thrombolysis in Stroke-Monitoring Study (SITS-MOST): an observational study. Lancet 2007; 369(9558): 275–282.
12. Kobayashi A, Czlonkowska A, Ahmed N, Romanowicz S, Glonek M, Nyka WM et al. Intravenous recombinant tissue plasminogen activator for acute stroke in Poland: an analysis based on the Safe Implementation of Thrombolysis in Stroke (SITS) Registry. Acta Neurol Scand 2010; 122(4): 229–236.
13. Topakian R, Brainin M, Eckhardt R, Kiechl S, Ahmed N, Ferrari J et al. Thrombolytic therapy for acute stroke in Austria: data from the Safe Implementation of Thrombolysis in Stroke (SITS) register. Eur J Neurol 2011; 18(2): 306–311.
14. Lees KR, Ford GA, Muir KW, Ahmed N, Dyker AG, Atula S et al. Thrombolytic therapy for acute stroke in the United Kingdom: experience from the safe implementation of thrombolysis in stroke (SITS) register. QJM 2008; 101(11): 863–869.
15. Vanacker P, Thijs V, Peeters A, Bruneel B, Laloux P, Druwé P et al. The Belgian experience with intravenous thrombolysis for acute ischemic stroke. Acta Neurol Belg 2010; 110(2): 157–162.
16. Alvarez-Sabín J, Molina CA, Rubiera M, Montaner J, Arenillas JF, Santamarina E et al. Impact of admission hyperglycemia on stroke outcome after thrombolysis: risk stratification in relation to time to reperfusion. Stroke 2004; 35(11): 2493–2498.
17. Ribo M, Molina CA, Delgado P, Rubiera M, Delgado-Mederos R, Rovira A et al. Hyperglycemia during ischemia rapidly accelerates brain damage in stroke patients treated with tPA. J Cereb Blood Flow Metab 2007; 27(9): 1616–1622.
18. Li PA, Shuaib A, Miyashita H, He QP, Siesjo BK, Warner DS. Hyperglycemia enhances extracellular glutamate accumulation in rats subjected to forebrain ischemia. Stroke 2000; 31(1): 183–192.
19. Fukuoka S, Yeh H, Mandybur TI, Tew JM Jr. Effect of insulin on acute experimental cerebral ischemia in gerbils. Stroke 1989; 20(3): 396–399.
20. Ribo M, Molina C, Montaner J, Rubiera M, Delgado-Mederos R, Arenillas JF et al. Acute hyperglycemia state is associated with lower tPA-induced recanalization rates in stroke patients. Stroke 2005; 36(8): 1705–1709.
21. Garg R, Chaudhuri A, Munschauer F, Dandona P. Hyperglycemia, insulin, and acute ischemic stroke: a mechanistic justification for a trial of insulin infusion therapy. Stroke 2006; 371: 267–273.
22. Executive Committee and the European Stroke Organization Writing Committee: ESO Guidelines for Management of Ischaemic Stroke Update 2009: 55–56 [online]. Dostupné z URL: www.eso-stroke.org.
23. Ahmed N, Dávalos A, Eriksson N, Ford GA, Glahn J, Hennerici M et al. Association of admission blood glucose and outcome in patients treated with intravenous thrombolysis: results from the Safe Implementation of Treatments in Stroke International Stroke Thrombolysis Register (SITS-ISTR). Arch Neurol 2010; 67(9): 1123–1130.
24. Engelter ST, Bonati LH, Lyrer PA. Intravenous thrombolysis in stroke patients of > or = 80 versus < 80 years of age – a systematic review across cohort studies. Age Ageing 2006; 35(6): 572–580.
25. Petrovicsová M, Kadlecová P, Václavík D, Šaňák D, Ševčík P, Mikulík R et al. Bezpečnost a účinnost intravenózní trombolytické terapie mozkového infarktu u pacientů nad 80 let. Cesk Slov Neurol N 2011; 74/ 107 (Suppl): S27.
26. Sandset EC, Bath PM, Boysen G, Jatuzis D, Kõrv J, Lüders S et al. The angiotensin-receptor blocker candesartan for treatment of acute stroke (SCAST): a randomised, placebo-controlled, double-blind trial. Lancet 2011; 377(9767): 741–750.
27. Executive Committee and the European Stroke Organization Writing Committee: ESO Guidelines for Management of Ischaemic Stroke Update 2009: 51–52 [online]. Dostupné z URL: www.eso-stroke.org.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2012 Číslo 4
Nejčtenější v tomto čísle
- Mozkové arachnoidální cysty u dospělých – retrospektivní analýza výsledků chirurgické terapie
- Porucha spánku s rytmickými pohyby
- Izolovaná sfenoidální sinusitida – možná příčina bolestí hlavy a závažných komplikací
- Oswestry dotazník, verze 2.1a – výsledky u pacientů s lumbální spinální stenózou, srovnání se starší verzí dotazníku
