Kognitivní rehabilitace pacientů s Parkinsonovou nemocí
Cognitive rehabilitation in patients with Parkinson’s disease
Cognitive impairment is recognized as an important non-motor symptom of Parkinson´s disease (PD) and it can be particularly characterized by disruption of executive functions, memory, visuospatial functions and attention. Cognitive decline may already occur in early stages of the PD and it can progress from mild cognitive impairment in PD up to dementia in PD. Cognitive rehabilitation (CR) represents one of non-pharmacological approaches to remediation of cognitive impairment in PD patients. At present, we have individual and group non-computerized and computerized approaches to CR. Currently, CR is not an evidence-based approach in PD patients, because of a limited number of studies. The report compares the research of efficiency of non-computerized CR in comparison with efficiency of computerized CR and combined approach. For this purpose, we searched for the research published between 2004 -2018. The aims of the report are to analyze current research of CR in PD patients and to compare the efficiency and benefits of computerized, non-computerized CR and combined approach for PD patients. The purpose of the report is to point out the new approaches and innovations in the field of CR in patients with neurodegenerative disorders.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Keywords:
Parkinson´s disease – cognitive rehabilitation – computerized cognitive rehabilitation – non-computerized cognitive rehabilitation – combined rehabilitation – cognitive dysfunction
Authors:
V. Plzáková 1,2; T. Nikolai 1
Authors‘ workplace:
Laboratoř neuropsychologie, Neurologická klinika 1. LF UK a VFN v Praze
1; Rehabilitační ústav Kladruby
2
Published in:
Cesk Slov Neurol N 2020; 83(1): 14-20
Category:
Review Article
doi:
https://doi.org/10.14735/amcsnn202014
Overview
Kognitivní deficit patří mezi signifikantní nemotorické symptomy Parkinsonovy nemoci (PN). U pacientů s PN bývá přítomen deficit exekutivních funkcí, paměti, vizuospaciálních funkcí a pozornosti. Deficity se mohou projevit již v časných fázích PN a mohou nabývat různých stupňů závažnosti: od mírné kognitivní poruchy u PN až po syndrom demence u PN. Kognitivní rehabilitace (KR) představuje jeden z nefarmakologických přístupů k intervenci kognitivního deficitu u PN. V současné době se kromě individuální a skupinové nepočítačové KR stále více v klinické praxi uplatňuje počítačová KR. Vzhledem k limitovanému počtu studií KR u pacientů s PN nelze prozatím tento přístup považovat za evidence-based. Příspěvek komparuje současné výzkumy efektivity nepočítačové KR ve srovnání se studiemi počítačové KR a kombinované rehabilitace u PN. Za tímto účelem byly vyhledávány výzkumy publikované v rozmezí od roku 2004 do roku 2018. Příspěvek si dává za cíl analyzovat současné výzkumy KR u pacientů s PN, porovnat efektivitu a přínos počítačové, nepočítačové KR a kombinované rehabilitace pro pacienty s PN. Záměrem příspěvku je poukázat na možné postupy a inovace v oblasti KR pacientů s neurodegenerativními onemocněními.
Klíčová slova:
kognitivní rehabilitace – počítačová kognitivní rehabilitace – nepočítačová kognitivní rehabilitace – kombinovaná rehabilitace – kognitivní defi cit – Parkinsonova nemoc
Úvod
Dříve byla Parkinsonova nemoc (PN) charakterizována především jako porucha motorických funkcí [1]. V posledních letech se zvyšuje povědomí o rozsahu klinického spektra symptomů PN, které kromě motorických symptomů zahrnuje i symptomy nemotorické. Mezi nemotorické symptomy PN patří porucha kognitivních funkcí. Kognitivní deficit u PN je heterogenní, ovlivňuje široké spektrum kognitivních domén. Deteriorace kognitivních funkcí u PN byla prokázána především v doménách exekutivních funkcí, vizuospaciálních funkcí, pozornosti a krátkodobé paměti [2,3]. Deficit kognitivních funkcí se u PN může manifestovat také v percepci, paměti, ve schopnosti učení, při utváření a formování konceptů, v plánování a řešení problémů, ve zvládání běžných denních aktivit (activities of daily living; ADL), ve verbálních schopnostech, v sebereflexi a abstraktním uvažování [4].
Neuropsychologická diagnostika pacientů s PN prokázala specifický kognitivní deficit dokonce již v časných fázích nemoci [4]. Kognitivní dysfunkce se může u pacientů manifestovat různým stupněm závažnosti, a to jako mírná kognitivní porucha (mild cognitive impairment; MCI), která může v průběhu nemoci progredovat až v syndrom demence u PN (PN-D) [5,6]. Mírná kognitivní porucha u Parkinsonovy nemoci (PN-MCI) je definována jako pokles aktuální úrovně některých kognitivních domén, který neodpovídá normě daného věku, kognitivní deficity neinterferují se zvládáním běžných denních aktivit [7]. Přesto může následkem PN-MCI dojít ke změnám v dynamice rodinných či ostatních sociálních vztahů. Pacienti s PN i pečující osoby mohou subjektivně prožívat zhoršenou kvalitu života [8].
Mírná kognitivní porucha u PN bývá často považována za rizikový faktor pro rozvoj PN-D [2]. Některé studie uvádí, že 25–50 % pacientů s PN-D v průběhu nemoci konvertuje do PN-MCI a PN-D nebo dojde ke konverzi ze stadia PN-MCI do PN-D do 5 let od diagnostiky PN [9]. PN-D se rozvíjí u většiny pacientů, kteří jsou diagnostikováni déle než 10 let [10]. PN-D se manifestuje symptomy závažné kognitivní deteriorace, která ve svém důsledku může negativně ovlivnit životní očekávání, významně snižuje kvalitu života pacienta i pečujících osob [11,12].
V klinické praxi může kognitivní deficit u PN prodloužit délku hospitalizace a zvýšit náklady na léčbu [11]. Efekt farmakoterapie v léčbě kognitivního deficitu u PN je limitován [13]. Vzhledem k tomu, že majorita pacientů s pokročilou PN trpí nadměrným užíváním medikace, dostávají se do popředí zájmu různé typy nefarmakologických intervencí [13]. Jedním z nefarmakologických přístupů k léčbě kognitivních poruch u PN je kognitivní rehabilitace. Jejím základem bývá některá z forem kognitivního tréninku. Kognitivní trénink poskytuje strukturované procvičování mentálních aktivit za účelem zlepšení kognitivního fungování [14,15]. Ve své praktické podobě bývá často specificky zaměřen na jednotlivé oblasti kognitivních funkcí nebo přímo na rozvíjení komplexních aktivit denního života [16]. Kognitivní rehabilitace představuje individuální přístup k pacientům s kognitivním deficitem a k jejich pečujícím osobám [17]. Cílem kognitivní rehabilitace je stimulovat funkční nezávislost jedince [18]. Důraz je především kladen na fungování v běžných denních aktivitách [19,20] a na využití maximálního potenciálu každého pacienta. Intervence se mohou zaměřovat na obnovení či posílení dřívějších vzorců chování, využívání externích a interních kompenzačních mechanizmů a strategií, adaptaci na změny související s deficitem kognitivních funkcí [21]. Jednotlivé intervence se odvíjí od specifických potřeb pacientů. Častými požadavky a cíli ze strany pacientů jsou např. správné používání různých typů technologií, self-management, strategie pro pravidelné užívání léků, vylepšení či zapojení se do sociálních interakcí a volnočasových aktivit nebo orientace v prostoru a čase [18]. Kognitivní rehabilitace u pacientů s PN přináší dle dostupné literatury pozitivní výsledky [22,23].
Cíle přehledové studie
Cílem této přehledové studie je systematicky ověřit proveditelnost a efektivitu nefarmakologických intervencí u respondentů s PN. Cílem je komparace efektivity počítačové, nepočítačové kognitivní rehabilitace a multimodálního přístupu u respondentů s PN. V rámci studie je analyzován vliv jednotlivých intervenčních přístupů na kognitivní funkce u respondentů s PN-MCI, s PN-D a u respondentů s PN bez kognitivního deficitu.
Metody
Pro vyhledávání článků byly použity databáze EBSCOhost Academic Search Ultimate, Taylor & Francis Online, Springer Standard Collection 2018, Elsevier Science Direct Journals Complete, Oxford University Press Journals, DOAJ Directory of Open Access Journals Free, Wiley Online Library Full Collection 2018, Journals@Ovid Complete. Pro přehledovou studii byly vyhledávány výzkumy publikované v rozmezí od roku 2004 do roku 2018. Do studie byly zahrnuty i výzkumy s nerandomizovaným designem, pokud byly explicitně zaměřeny na kognitivní intervence u PN-MCI, PN-D, u respondentů s PN bez kognitivního deficitu. Do přehledové studie nebyly zahrnuty kazuistiky. Laboratorní experimentální studie byly vyloučeny. Výzkumy byly publikovány výhradně v anglickém jazyce. Pojmy pro vyhledávání výzkumných intervenčních studií byly zvoleny na základě některých již publikovaných přehledových studií [13,24]. Pro vyhledávání byly zvoleny pojmy: cognitive rehabilitation, cognitive rehabilitation in Parkinson’s disease, cognitive training, cognitive training in Parkinson’s disease, cognitive stimulation, cognitive stimulation in Parkinson’s disease, nonpharmacological enhancement in Parkinson’s disease. Pojmy pro vyhledávání byly použity takto: “Parkinson’s disease” AND “cognitive rehabilitation” OR “cognitive training” OR “cognitive stimulation” OR “nonpharmacological enhancement”. Pro zefektivnění postupu byla posouzena vhodnost článku na základě abstraktu a potenciálně relevantní abstrakty byly pročteny jedním autorem (V. P.) a následně supervidovány (T. N.).
Nepočítačová kognitivní rehabilitace
Nepočítačová kognitivní rehabilitace představuje intervence bez využití počítačových softwarů. Převážně jsou v nepočítačové kognitivní rehabilitaci využívány úkoly typu tužka-papír (tab. 1). V současné klinické praxi je nejčastěji aplikován strukturovaný kognitivní trénink jednotlivých domén. Nepočítačová kognitivní rehabilitace může být také zacílena na nácvik a využití různých typů kompenzačních mechanizmů. V praxi se můžeme setkat s nácvikem používání externích kompenzačních mechanizmů, tzn. využívání diáře, kalendáře, upomínek v mobilním telefonu nebo s nácvikem interních kompenzačních mechanizmů, např. mnemotechnik, strategií pro exekutivní funkce a pozornost. Nepočítačová kognitivní rehabilitace může probíhat individuálně nebo skupinově. Frekvence kognitivní intervence se v jednotlivých studiích často liší. Jednotlivé nepočítačové kognitivní intervence se mohou také lišit svou komplexností, tzn. počtem trénovaných domén.
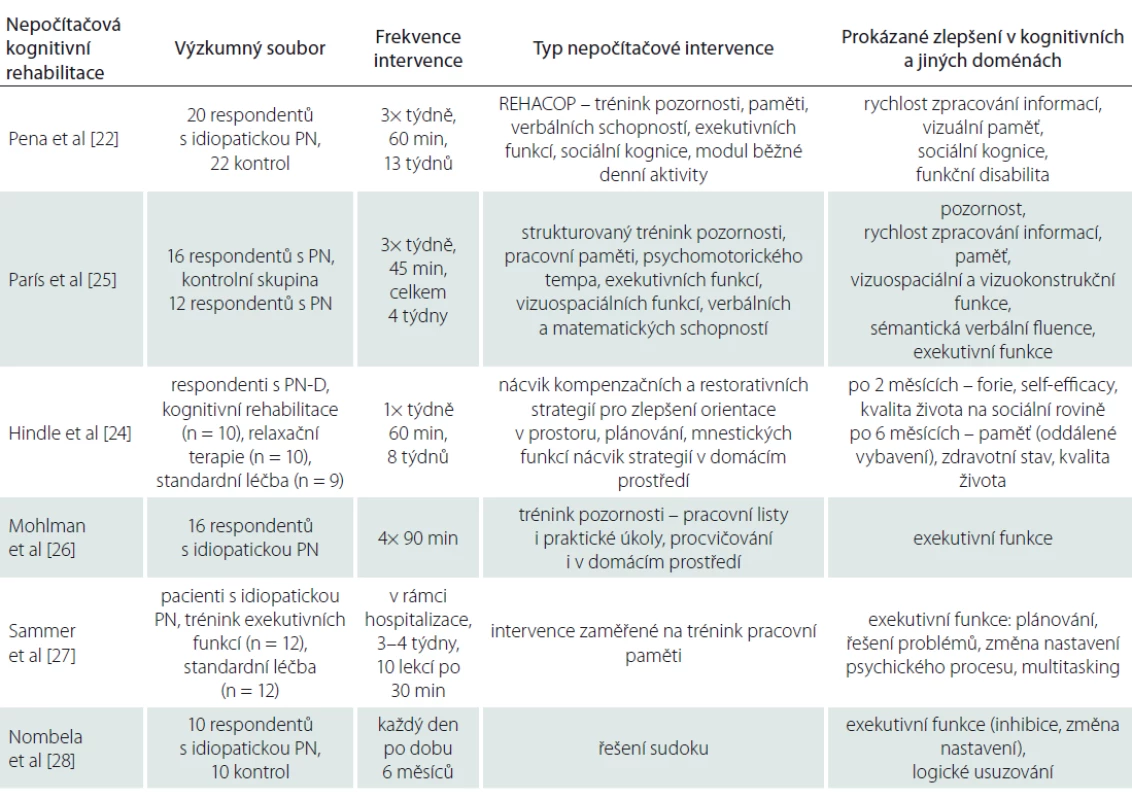
REHACOP je prezentován jako komplexní strukturovaný kognitivně rehabilitační program zacílený na zlepšení kognitivní výkonnosti a funkční disability u respondentů s PN [22]. REHACOP obsahuje 300 úkolů, které jsou hierarchicky organizovány do 3 úrovní. Každá úroveň je komponována z jednotlivých bloků intervenujících vždy jednu kognitivní doménu. Blok pozornost (trénink selektivní, rozdělené a zaměřené pozornosti), blok paměť (vizuální a verbální učení, oddálené vybavení, rekognice), blok verbální schopnosti (gramatika, syntax, slovník, verbální fluence, slovní porozumění, abstrakce), blok exekutivní funkce (plánování, přísloví, analogie, sociální kognice), blok sociální kompetence (teorie mysli, sociální usuzování, dilemata). Efektivita programu REHACOP byla komparována s výkony respondentů zařazených do kontrolní skupiny, kteří podstoupili pracovní terapii. Aktivity kontrolní skupiny byly zacíleny na rukodělné práce s různými typy materiálů a na četbu. Změna v kognitivní výkonnosti respondentů obou skupin byla hodnocena pomocí neuropsychologického vyšetření zacíleného na analýzu rychlosti zpracování, paměti, exekutivních funkcí, Teorie mysli a také na hodnocení přítomnosti neuropsychiatrických symptomů a funkční disability. Respondenti s PN zařazení do komplexního programu REHACOP se signifikantně zlepšili v rychlosti zpracování informací, vizuální paměti, teorii mysli, funkční disabilitě [22]. Respondenti experimentální skupiny v rámci programu REHACOP trénovali strategie pro učení, cílem tréninku byl transfer do ADL [22].
Strukturovaný kognitivní trénink respondentů s PN-MCI zaměřený na nácvik pozornosti, paměti, psychomotorického tempa, exekutivních a vizuospaciálních funkcí, verbálních schopností, matematických a sociálních schopností měl oproti řečové terapii v kontrolní skupině prokazatelně pozitivní efekt v doménách pozornosti, rychlosti zpracování informací, mnestických funkcích, visuospaciálních a visuokonstrukčních schopnostech a v doménách exekutivních funkcí [25]. V experimentální skupině podstupující kognitivní trénink nebyla nalezena signifikantní zlepšení v celkové kognitivní výkonnosti administrovaným testem Mini Mental State Examination (MMSE) a Addenbrooke’s Cognitive Examination. Nebyl prokázán vliv kognitivního tréninku na zlepšení subjektivně hodnocené kvality života a na lepší kompenzaci kognitivního deficitu ADL [25].
Pacienti s PN-D často bývají závislí při vykonávání ADL na dopomoci pečujících osob. Pravidelná strukturovaná 8týdenní kognitivní rehabilitace respondentů s PN-D zacílená na nácvik kompenzačních a restorativních strategií měla vliv na zlepšení emotivity, self-efficacy a sociální participace respondentů experimentální skupiny [24]. Po 6 měsících od ukončení programu byl prokázán efekt kognitivní rehabilitace v oddáleném vybavení z paměti. U respondentů s PN-D se také signifikantně zlepšily kvalita života a celkový zdravotní stav [24]. V kontrolní skupině, která podstoupila relaxační terapii, ani v kontrolní skupině, která dostávala obvyklou léčbu, nebyly prokázány žádné významné rozdíly v kognitivní výkonnosti a kvalitě oproti počáteční úrovni hodnocení skríningovými neuropsychologickými testy a dotazníky kvality života.
Nepočítačová kognitivní rehabilitace může být zacílena na trénink pouze jedné kognitivní domény. V klinické praxi obvykle bývá u respondentů s PN indikován trénink pozornosti, pracovní paměti nebo exekutivních funkcí. Strukturovaný kognitivní trénink respondentů s PN sestavený z praktických úkolů a pracovních listů zaměřených na jednotlivé oblasti pozornosti (tenacita, selektivita pozornosti, rozdělená pozornost) byl efektivní pro domény exekutivních funkcí vyžadující zaměření pozornosti [26]. Pravidelný ambulantní trénink probíhal paralelně s tréninkem v domácím prostředí. Studie hodnotila také proveditelnost kognitivního tréninku u PN. Ta byla posuzována ve čtyřech oblastech – unavitelnost, vytrvalost, progres, radost. Respondenti studie se velmi dobře na intervenci adaptovali, míra zapojení byla vysoká. Výkonnost respondentů korelovala s únavou. Muži během intervence vykazovali větší úsilí než ženy [26].
Respondenti s idiopatickou PN mohou profitovat ze specifického krátkodobého tréninku exekutivních funkcí se zaměřením především na trénink pracovní paměti [27]. Celkový rozsah kognitivní rehabilitace byl 3–4 týdny. Efektivita studie byla hodnocena porovnáním kognitivních výkonů respondentů v experimentální tréninkové skupině a skupině kontrolní (standardní léčba) pomocí neuropsychologické diagnostiky. Administrovaná testová baterie byla zacílena na vyšetření exekutivních funkcí, pracovní paměti, pozornosti, well-beingu, intelektu a posouzení míry deprese. Respondenti s PN v experimentální skupině se oproti kontrole zlepšili ve schopnosti organizace postupu v jednotlivých úkolech, dokázali lépe řešit paralelně více úloh, vylepšila se i doména změny nastavení psychického procesu. V rámci studie nebyl hodnocen efekt transferu do ADL [27].
Některé přístupy nepočítačové kognitivní rehabilitace u PN využívají pro trénink běžné mentální aktivity, jako je např. luštění sudoku. Vyšetřením pacientů s PN a zdravých kontrol funkční MR a modifikovanou verzí Stroopova testu bylo zjištěno, že respondenti s PN, kteří trénovali kognici luštěním sudoku, se signifikantně zlepšili v jednotlivých doménách exekutivních funkcí (schopnost upravit naučenou či automatickou odpověď, změna nastavení psychického procesu) a v logickém usuzování. Kognitivní trénink v podobě luštění sudoku stimuluje kortikální plasticitu respondentů s PN. Po 6měsíční nepočítačové intervenci byly vzorce kortikální aktivace u pacientů s PN srovnatelné s intaktní populací. Kognitivní intervence založená na luštění sudoku má u pacientů s idiopatickou PN střednědobý efekt [28]. Kognitivní rehabilitace může zlepšit kognitivní strategie pacientů s PN v oblasti řešení problémů, flexibilitě myšlení a v rovině kognitivně behaviorální. Zlepšování kognitivních schopností může mít také pozitivní efekt na motorické symptomy. Respondenti, kteří podstoupili kognitivní rehabilitaci, byli i pro další intervence více motivováni, lépe snášeli měnící se úkolové situace. Při některých kognitivních cvičeních dochází k reaktivaci frontálních oblastí mozku, kde je lokalizováno i motorické plánování [28]. Vzhledem k těmto zjištěním lze konstatovat, že standardizovaná kognitivní rehabilitace by měla být součástí managementu péče o pacienty s PN.
Počítačová kognitivní rehabilitace
V současné době dochází k prudkému vývoji softwarů počítačové kognitivní rehabilitace (tab. 2). Různé typy programů, ať už komplexních nebo zaměřených na jednotlivé kognitivní domény, rychle pronikají do klinické praxe i do distanční terapie v domácím prostředí. Počítačový software BrainStim (COGITO Center, Düsseldorf, Německo) je zacílen na kompenzaci deficitu pracovní paměti [29]. Software je sestaven ze tří tréninkových modulů. Modul „Mapa města“ stimuluje paměť pro verbální materiál a vizuospaciální funkce. Modul „Hledání párů“ je zacílen na posílení vizuální prostorové pracovní paměti. Modul „Paměť na čísla“ je zaměřen na procvičování mnestických funkcí. Počítačový software BrainStim je efektivní v tréninku paměti pro verbální materiál a vizuální prostorové pracovní paměti u respondentů s idiopatickou PN [29].
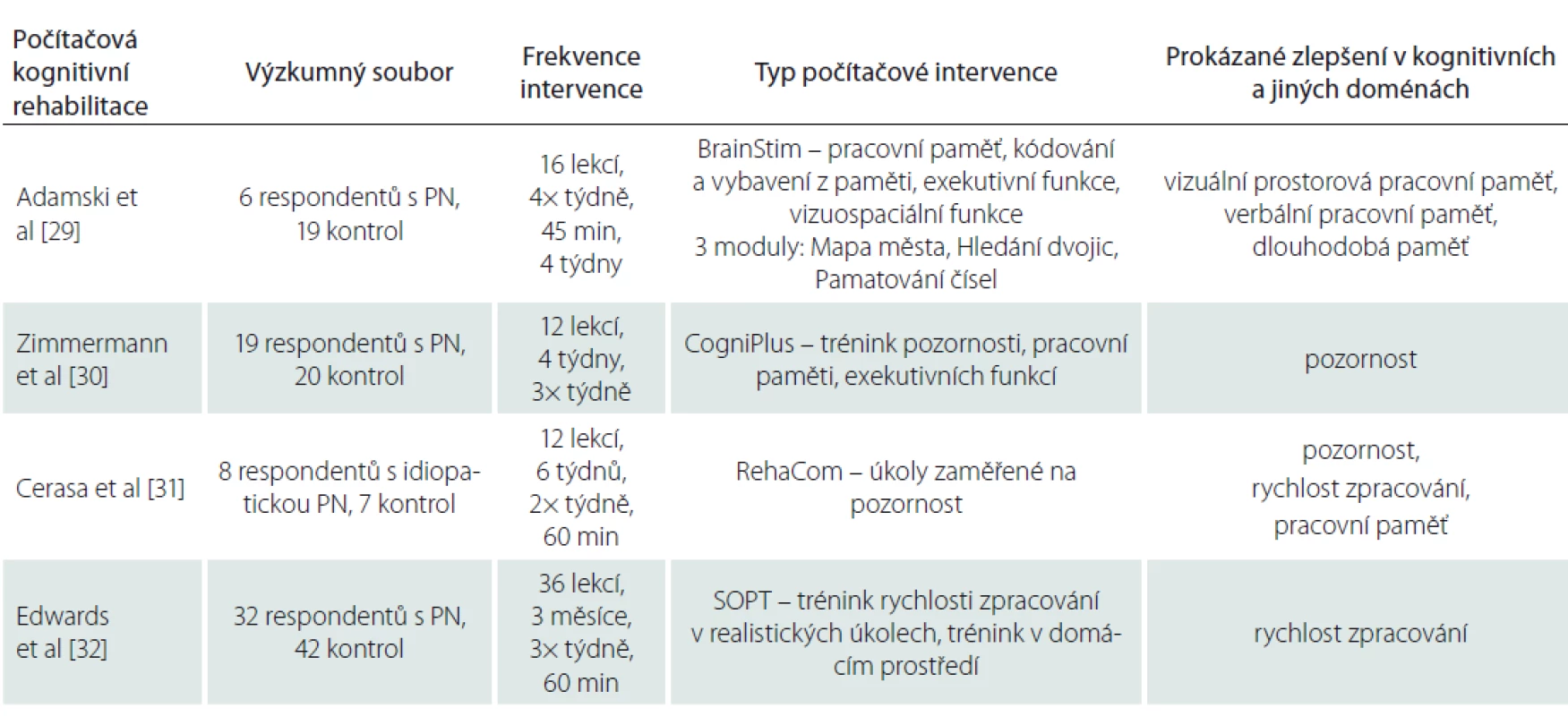
Software Cogniplus (Schuhfried, Mödling, Rakousko) je pokládán za evidence-based tréninkový program kognitivních funkcí [30]. V tomto programu lze konfigurovat různé úkoly dle neuropsychologického profilu pacienta. Některé moduly jsou zacíleny na nácvik mnemotechnik nebo vedení diáře. Respondenti s PN, kteří podstoupili pravidelnou kognitivní rehabilitaci s využitím programu Cogniplus, se signifikantně zlepšili v kvalitách pozornosti. Efektivita programu Cogniplus byla posuzována rozdílem v kognitivní výkonnosti v neuropsychologickém vyšetření před začátkem kognitivní intervence, po jejím skončení a následně po 3 měsících od skončení intervence. Respondentům byly v rámci vstupního psychologického vyšetření i retestu administrovány sebeposuzovací škály zacílené na hodnocení únavy a depresivních symptomů. Kognitivní výkonnost respondentů byla zároveň komparována s kognitivními výkony zdravých kontrol. Efekt tréninku s využitím programu Cogniplus byl u respondentů s PN přítomen i po 3 měsících od skončení intervence. Výsledky studie ukazují, že kognitivní trénink není efektivní pouze pro stimulaci jednotlivých kognitivních domén, ale také zlepšuje self-efficacy a well-being respondentů [30].
Počítačový software Rehacom (Hasomed, Magdeburg, Německo) představuje komplexní program pro rehabilitaci kognitivních funkcí [31]. Trénink je možné nakonfigurovat každému pacientovi individuálně. Bylo prokázáno, že respondenti s PN, kteří pravidelně trénovali v programu Rehacom moduly zaměřené na pozornost a rychlost zpracování informací, se signifikantně v těchto doménách zlepšili. Efekt využitého softwaru byl u respondentů s PN zařazených do experimentální skupiny prokázán vyšetřením funkční MR a změnami v kognitivní výkonnosti v neuropsychologickém vyšetření respondentů před započetím pravidelné intervence a po jejím skončení. Změny v kognitivní výkonnosti respondentů experimentální skupiny byly porovnávány s kognitivními výkony a MR respondentů kontrolní skupiny. Respondentům kontrolní skupiny byla indikována placebo počítačová intervence v domácím prostředí, v níž měli respondenti za úkol plnit jednoduché úkoly zacílené na vizuomotorickou koordinaci. Kognitivní rehabilitace specificky zacílená na jednu kognitivní doménu může mít benefity pro zmírnění poruch pozornosti u pacientů s PN. Doména pozornosti má kontrolní a integrační funkci implikující od ostatních kognitivních domén. Zlepšení této domény může mít vliv na celé spektrum kognitivních domén [31].
Počítačový program SOPT (Speech Processing Training) (Visual Awareness Research Group, Sarasota, Finsko) lze využít pro individuální trénink kognitivních funkcí v domácím prostředí [32]. Respondenti s PN-MCI trénovali úkoly zaměřené na rychlost zpracování informací. Software SOPT má za cíl simulovat trénink jednotlivých kognitivních domén v realistických podmínkách. Trénink rychlosti zpracování byl u respondentů s PN-MCI prokazatelně efektivní. Efektivita tréninku byla prokázána v rozdílných výsledcích vstupního vyšetření a retestu respondentů s PN-MCI zařazených do experimentální a kontrolní skupiny. Hodnoceny byly celková kognitivní výkonnost respondentů, rychlost zpracování informací ve fázi vstupu a výstupu, motorická rychlost, hodnocení závažnosti symptomů PN dle The Unified Parkinson’s Disease Rating Scale (UPDRS), hodnocení míry depresivních symptomů. Respondentům byly ve fázi vstupu i výstupu administrovány sebeposuzovací zdravotní škály a škály na hodnocení zvládání ADL. Počítačový software SOPT může potenciálně snížit zátěž pečujících osob, zdravotnických institucí, časovou a finanční náročnost péče. Současná studie nebyla cílena na analýzu transferu do běžných denních aktivit, budoucí studie budou zaměřeny na hodnocení longitudinálního efektu pro zachování řidičských schopností a bezpečnou jízdu autem u pacientů s PN [32].
Kombinovaný trénink
Dle prezentovaných studií je pravděpodobné, že kognitivní rehabilitace zlepšuje u pacientů s PN kognitivní výkonnost. Nicméně současné studie kognitivní rehabilitace již dále nestudují transfer těchto pokroků do běžných denních aktivit. Někteří autoři předpokládají, že kombinované rehabilitační programy komponované z mentálních a fyzických aktivit jsou efektivnější než samotná kognitivní rehabilitace. Studie, do níž bylo zařazeno celkem 240 respondentů s PN (tab. 3), mapovala efektivitu kombinované rehabilitace [33]. Respondenti byli náhodně rozděleni do tří skupin, každé skupině byly indikovány rozdílné intervence. Skupina A podstoupila kognitivní trénink, skupina B měla pravidelný kognitivní trénink v kombinaci s tréninkem transferu naučených dovedností do běžných denních aktivit, skupina C podstoupila oba typy kognitivních intervencí a fyzický trénink zaměřený na psychomotoriku a fyzickou kondici. Intervence probíhaly po dobu 4 týdnů v rámci hospitalizace, a poté pokračovaly v domácím prostředí.
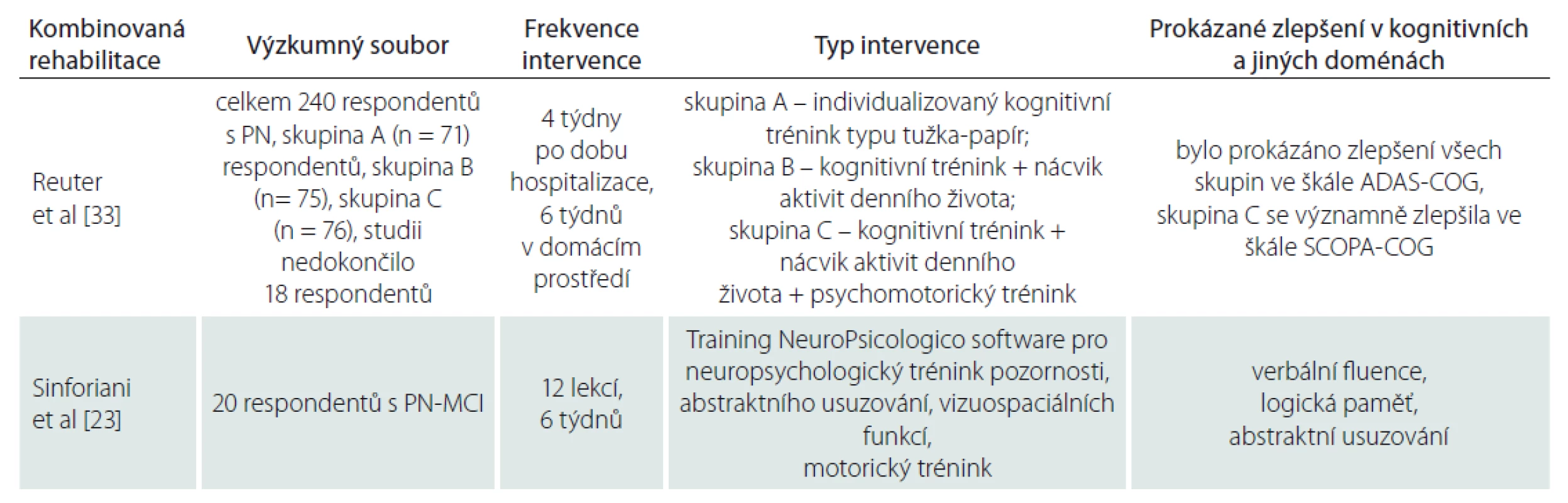
Respondenti s PN zařazení do kombinovaného motorického a mentálního tréninku (skupina C) se oproti respondentům zařazeným do kontrolních skupin zlepšili ve škálách kognitivní výkonnosti Alzheimer Assessment Scale Cognition (ADAS-COG) a Scales for Outcome of Parkinsons Disease Cognition (SCOPA-COG). Respondenti zařazení do kombinovaného tréninku subjektivně lépe hodnotili svůj vlastní zdravotní stav. Kombinovaná kognitivní rehabilitace má vliv na větší zapojení pacientů s PN do vykonávání ADL, čímž může dojít k celkovému zlepšení kvality života. Pečující osoby respondentů zařazených do kombinované kognitivní rehabilitace reflektovaly větší zapojení respondentů do ADL. Bylo prokázáno, že fyzické cvičení může mít benefit pro zmírnění deficitu exekutivních funkcí. Kombinovaný trénink má vliv na exekutivní domény změny nastavení psychického procesu na rozhodování. Tento přístup je efektivní zejména u PN-MCI, velmi omezený efekt tohoto přístupu je patrný u PN-D [33].
U respondentů s PN-MCI, kteří absolvovali komplexní kognitivně rehabilitační program složený jak z mentálních, tak fyzických aktivit, bylo prokázáno signifikantní zlepšení v neuropsychologických testech [23]. Šestitýdenní intervenční program byl sestaven z počítačového tréninku zacíleného na domény pozornosti, vizuospaciálních funkcí, na logické myšlení a abstraktní usuzování a z motorického tréninku. Respondenti s PN-MCI se signifikantně zlepšili v doméně verbální fluence, logické paměti a usuzování. Efekt kognitivní rehabilitace byl prokázán neuropsychologickým vyšetřením i po 6 měsících od skončení intervence. Kombinovaná kognitivní rehabilitace má pozitivní vliv na posilování a upevňování kognitivních strategií, které jsou funkcí frontálního laloku [23].
Diskuze
Současné studie nepočítačové kognitivní rehabilitace u pacientů s PN prokazují, že tento typ intervence je efektivní pro trénink rychlosti zpracování informací [22,25], kvality pozornosti [25] a paměti [22,24,25], některých domén exekutivních funkcí [27,28], vizuospaciálních funkcí a vizuokonstrukčních schopností [25], logického usuzování [28]. Nepočítačová kognitivní rehabilitace v praxi probíhá formou individuální nebo skupinové intervence. Současné výzkumy prokazují, že sociální interakce, které představují nedílnou součást nepočítačových intervencí, jsou efektivní pro zlepšení sociální kognice [22,24], kvality života [24], nálady [24], self-efficacy [24] a funkční disability pacientů s PN [22]. Nepočítačová kognitivní rehabilitace umožňuje pacientům stanovovat si individuální cíle intervence. Rehabilitace by měla být zacílena na běžné denní aktivity pacientů a nácvik kompenzačních mechanizmů pro jejich zvládání. Nevýhodou nepočítačové kognitivní rehabilitace může být její časová, organizační náročnost a nejednotné postupy intervence u jednotlivých klinických populací.
Výzkumy počítačové kognitivní rehabilitace prokázaly pozitivní efekt pravidelného tréninku na pozornost [30,31], pracovní paměť [29,31], rychlost zpracování informací [31,32] a na dlouhodobou paměť [29]. Nespornou výhodou počítačových kognitivních intervencí je časová a organizační nenáročnost. Mnohé tréninkové softwary jsou autoadaptivní. Úrovně obtížnosti v jednotlivých úkolech jsou postupně stanovovány dle výkonnosti pacienta. Software dynamicky reaguje na aktuální výkonnost pacienta, není tedy nutné, aby byl po celou dobu terapeut přítomen u intervence jednoho pacienta. To umožňuje individualizovaný trénink současně několika pacientů. Některé komerční softwary nabízejí možnost jejich využití v distanční terapii. Pacient může samostatně trénovat v domácím prostředí, zároveň však terapeut dostává zpětnou vazbu o dosažených výsledcích či frekvenci tréninku. Terapeut může na základě zpětné vazby upravovat či měnit trénované úkoly. Nevýhodou může být chybějící sociální interakce mezi pacientem a terapeutem nebo ve skupině pacientů. Počítačové programy neumožňují nácvik a aplikaci kompenzačních mechanizmů jako např. mnemotechnik. Počítačové programy systematicky stimulují jednotlivé kognitivní domény, ale nekorelují s běžnými denními činnostmi pacientů.
Efektivní přístup ke stimulaci kognitivního deficitu u PN představuje kombinovaná kognitivní rehabilitace, která je sestavena z fyzických aktivit, kognitivního tréninku [23] a případně nácviku běžných denních aktivit [33]. Kombinovaná kognitivní rehabilitace kompenzuje možné projevy kognitivního deficitu v běžných denních aktivitách. V klinické praxi se např. často setkáváme s poruchami stability u pacientů s PN. Ty jsou zčásti ovlivněny oslabenými exekutivními funkcemi a pozorností. Pacienti mají problémy s multitaskingem, tzn. že každý rušivý stimul může při chůzi narušit pozornost a způsobit pád. Kombinovaná rehabilitace umožňuje komplexně přistupovat ke kompenzaci symptomů PN. V rámci strukturovaného tréninku mohou být stimulovány oslabené domény, současně mohou probíhat transfer do běžných denních aktivit a aplikace do pohybových vzorců pacienta. Kombinovaná rehabilitace by mohla představovat efektivní přístup ke kompenzaci neurodegenerativních procesů u PN. V ambulantní péči je tento koncept pravděpodobně neproveditelný a může se spíše uplatnit během hospitalizace v rehabilitačních ústavech.
V současné době se stále více ukazuje, že PN představuje komplexní problematiku zahrnující kromě motorických symptomů i symptomy nemotorické. I přesto, že mnoho výzkumů prokazuje u PN kognitivní deficit, změny v emotivitě, prožívání a změny na behaviorální rovině, tak v léčbě PN stále dominuje farmakoterapie. Medikace je podstatnou součástí léčby PN, zároveň by však neměla být jedinou. Přístup k léčbě PN by měl být komplexní. Na intervencích by se měli podílet lékaři, fyzioterapeuti, psychologové, logopedi, nutriční terapeuti a další specialisté. Cílem spolupráce jednotlivých specialistů by měl být ucelený intervenční program, ze kterého by pacient mohl profitovat a který by mu pomohl žít kvalitněji vlastní život. Komplexní přístup by měl být aplikován i v kognitivní rehabilitaci. Je třeba kognitivní intervence pro pacienty utvářet tak, aby efektivita transferu do běžných denních činností byla co největší. Počítačová kognitivní rehabilitace je limitována svou strukturou. Pacient trénuje pomocí úkolů na počítači jednotlivé kognitivní domény, ale nemáme důkazy o tom, zda trénink koreluje s efektivnějším vykonáváním běžných denních aktivit. V nepočítačové kognitivní rehabilitaci si osvojuje kompenzační mechanizmy pro paměť a jiné kognitivní domény, ale v klinické praxi není proveditelný každodenní trénink tak, aby si pacient vštípil kompenzační strategie natolik, že je začne spontánně využívat v běžných činnostech. Vzhledem k aktuálním možnostem současné klinické praxe by byla vhodným řešením kombinace počítačové distanční terapie, kterou pacient provádí samostatně v domácím prostředí, a podpůrné skupiny zaměřené na nácvik kompenzačních strategií.
Limity
Limitem současné přehledové studie je absence publikovaného výzkumu kognitivní rehabilitace u pacientů s PN v ČR a jeho možná komparace se zahraničními studiemi. Aktuální přehledová studie uvádí minimální počet výzkumů zaměřených na kombinovanou kognitivní rehabilitaci, která je vnímána jako potenciálně efektivní. V budoucí přehledové studii by bylo třeba explorovat další publikované studie kombinované kognitivní rehabilitace se shodným výzkumným designem a následně porovnat efektivitu použitých intervencí.
Závěr
Kognitivní rehabilitace představuje dynamicky se rozvíjející koncept neinvazivní stimulace mozku u pacientů s kognitivním deficitem. Současné výzkumy neurodegenerativních nemocí se kromě diagnostiky stále více zaměřují na rozvíjení metod kognitivních intervencí, které by doplnily standardní farmakologickou léčbu o nový rozměr péče. Klinická aplikace metod kognitivní rehabilitace u pacientů s PN se zaměřuje na zlepšení soběstačnosti pacientů s různou hloubkou kognitivního deficitu, na zvládání běžných denních aktivit. Předpokládaným druhotným efektem kognitivní rehabilitace je snížení subjektivní zátěže pečujících osob. Současná klinická praxe v ČR se potýká se značnou nejednotností ve standardních postupech kognitivní intervence. Jednotlivé intervence se liší frekvencí, počtem pacientů a zejména použitými metodami. Aktuálně jsou v klinické praxi nejčastěji využívány strukturované úkoly typu tužka-papír nebo komerční tréninkové softwary. Současná přehledová studie mapuje zahraniční trendy v oblasti výzkumu kognitivní rehabilitace u pacientů s PN, porovnává výhody a nevýhody nepočítačové, počítačové a kombinované kognitivní rehabilitace. Výsledky publikovaných studií ukazují, že kognitivní rehabilitace představuje dobře proveditelný a efektivní koncept intervence kognitivního deficitu u pacientů s neurodegenerativním onemocněním. Budoucí intervenční výzkumy by se mohly zaměřovat na efekt transferu do běžných denních aktivit a na udržitelnost efektu kognitivní rehabilitace v čase.
Grantová podpora
Podpořeno granty: GAUK č. 848617, Progres Q27/ LF1.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
PhDr. Vladimíra Plzáková
Neurologická klinika
1. LF UK a VFN v Praze
Viničná 9
128 21 Praha
e-mail: vladimira.plzakova@rehabilitace.cz
Přijato k recenzi: 9. 5. 2019
Přijato do tisku: 29. 10. 2019
Sources
1. Chen L, Yu C, Zhang N et al. Cognitive impairment in patients with Parkinson’s disease: a 30-month follow-up study. Clin Neurol Neurosurg 2016; 151: 65–69. doi: 10.1016/ j.clineuro.2016.09.021.
2. Hurtado Gonzalez CA, Ladera V, Perea MV et al. Mild cognitive impairment in idiopathic Parkinson‘s disease without dementia. Biomed Res 2017; 28(8): 3635–3640.
3. Das D, Biswas A, Roy A et al. Cognitive impairment in idiopathic Parkinson‘s disease. Neurol India 2016; 64(3): 419–427. doi: 10.4103/ 0028-3886.181533.
4. Dubois B, Pillon B. Cognitive deficits in Parkinson’s disease. J Neurol 1996; 244(1): 2–8. doi: 10.1007/ PL00007725.
5. Litvan I, Goldman JG, Tröster AI et al. Diagnostic criteria for mild cognitive impairment in Parkinson‘s disease: Movement Disorder Society Task Force guidelines. Mov Disor 2012; 27(3): 349–356. doi: 10.1002/ mds.24893.
6. Svenningsson P, Westman E, Ballard C et al. Cognitive impairment in patients with Parkinson’s disease: diagnosis, biomarkers, and treatment. Lancet Neurol 2012; 11(8): 697–707. doi: 10.1016/ S1474-4422(12)70152-7.
7. Nikolai T, Bezdíček O, Vyhnálek M et al. Mírná kognitivní porucha: diagnostická jednotka nebo stadium předcházející demenci. Cesk Psychol 2012; 56(4): 374–390.
8. Kim KS, Kim BJ, Kim KH et al. Subjective and objective caregiver burden in Parkinson’s disease. Taehan Kanho Hakhoe Chi 2007; 37(2): 242–248. doi: 10.4040/ jkan.2007.37.2.242.
9. Pedersen KF, Larsen JP, Tysnes OB et al. Prognosis of mild cognitive impairment in early Parkinson disease. JAMA Neurol 2013; 70(5): 580–586. doi: 10.1001/ jamaneurol.2013.2110.
10. Aarsland D. Cognitive impairment in Parkinson‘s disease and dementia with Lewy bodies. Parkinsonism Relat Disord 2016; 22 (Suppl 1): S144–S148. doi: 10.1016/ j.parkreldis.2015.09.034.
11. Yang Y, Tang BS, Guo JF. Parkinson’s disease and cognitive impairment. Parkinsons Dis 2016; 2016: 6734678. doi: 10.1155/ 2016/ 6734678.
12. Hindle JV, Watermeyer TJ, Roberts J et al. Cognitive rehabiliation for Parkinson‘s disease dementia: a study protocol for a pilot randomised controlled trial. Trials 2016; 17(1): 152. doi: 10.1186/ s13063-016-1253-0.
13. Leung IH, Walton CC, Hallock H et al. Cognitive training in Parkinson disease: a systematic review and meta-analysis. Neurology 2015; 85(21): 1843–1851. doi: 10.1212/ WNL.0000000000002145.
14. Clare L, Woods R. Cognitive training and cognitive rehabilitation for people with early-stage Alzheimer‘s disease: a review. Neuropsychol Rehab 2004; 14(4): 385–401. doi: 10.1080/ 09602010443000074.
15. Gates NJ, Sachdev PS, Fiatarone Singh MA et al. Cognitive and memory training in adults at risk of dementia: a systematic review. BMC Geriatr 2011; 11: 55. doi: 10.1186/ 1471-2318-11-55.
16. Kennedy MR, Coelho C, Turkstra L et al. Intervention for executive functions after traumatic brain injury: a systematic review, meta-analysis and clinical recommendations. Neuropsychol Rehabil 2008; 18(3): 257–299. doi: 10.1080/ 09602010701748644.
17. Clare L, Linden DE, Woods RT et al. Goal-oriented cognitive rehabilitation for people with early-stage Alzheimer disease: a single blind randomized controlled trial of clinical efficacy. Am J Geriatr Psychiatry 2010; 18(10): 928–939. doi: 10.1097/ JGP.0b013e3181d5792a.
18. Watermeyer TJ, Hindle JV, Roberts J et al. Goal setting for cognitive rehabilitation in mild to moderate Parkinson’s disease dementia and dementia with Lewy bodies. Parkinsons Disease 2016; 2016: 8285041. doi: 10.1155/ 2016/ 8285041.
19. Simon SS, Yokomizo JE, Bottino CM. Cognitive intervention in amnestic mild cognitive impairment: a systematic review. Neuroscience 2012; 36(4): 1163–1178. doi: 10.1016/ j.neubiorev.2012.01.007.
20. Levine B, Robertson IH, Clare L et al. Rehabilitation of executive functioning: an experimental – clinical validation of goal management training. J Int Neuropsychol Soc 2000; 6(3): 299–312. doi: 10.1017/ S1355617700633052.
21. Cicerone KD, Dahlberg C, Kalmar K et al. Evidence-based cognitive rehabilitation: recommendations for clinical practice. Arch Phys Med Rehabil 2000; 81(12): 1596–1615. doi: 10.1053/ apmr.2000.19240.
22. Pena J, Ibarretxe-Bilbao N, Gacía-Gorostiaga I et al. Improving functional disability and cognition in Parkinson disease: randomized controlled trial. Neurology 2014; 83(23): 2167–2174. doi: 10.1212/ WNL.0000000000001043.
23. Sinforiani E, Banchieri L, Zucchella C et al. Cognitive rehabilitation in Parkinson‘s disease. Arch Gerontol Geriatr Suppl 2004; 9: 387–391. doi: 10.1016/ j.archger.2004.04.049.
24. Hindle JV, Watermayer TJ, Roberts J et al. Goal-orientated cognitive rehabilitation for dementias associated with Parkinson‘s disease pilot randomised controlled trial. Int J Geriatr Psychiatry 2018; 33(5): 718–728. doi: 10.1002/ gps.4845.
25. París AP, Saleta HG, de la Cruz Crespo Maraver M et al.Blind randomized controlled study of the efficacy of cognitive training in Parkinson‘s disease. Mov Disord 2011; 26(7): 1251–1258. doi: 10.1002/ mds.23688.
26. Mohlman J, Chazin D, Georgescu B. Feasibility and acceptance of a nonpharmacological cognitive remediation intervention for patients with Parkinson disease. J Geriatr Psychiatry Neurol 2011; 24(2): 91–97. doi: 10.1177/ 0891988711402350.
27. Sammer G, Reuter I, Hullmann K et al. Training of executive functions in Parkinson‘s disease. J Neurol Sci 2006; 248(1–2): 115–119. doi: 10.1016/ j.jns.2006.05.028.
28. Nombela C, Bustillo PJ, Castell PF et al. Cognitive rehabilitation in Parkinson’s disease: evidence from neuroimaging. Front Neurol 2011; 2: 82. doi: 10.3389/ fneur.2011.00082.
29. Adamski N, Adler M, Opwis K et al. A pilot study on the benefit of cognitive rehabilitation in Parkinson’s disease. Ther Adv Neurol Disord 2016; 9(3): 153–164. doi: 10.1177/ 1756285616628765.
30. Zimmermann R, Gschwandtner U, Benz N et al. Cognitive training in Parkinson disease: cognition-specific vs nonspecific computer training. Neurology 2014; 82(14): 1219–1226. doi: 10.1212/ WNL.0000000000000287.
31. Cerasa A, Gioia MC, Salsone M et al. Neurofunctional correlates of attention rehabilitation in Parkinson’s disease: an explorative study. Neurol Sci 2014; 35(8): 1173–1180. doi: 10.1007/ s10072-014-1666-z.
32. Edwards JD, Hauser RA, O’Connor ML et al. Randomized trial of cognitive speed of processing training in Parkinson disease. Neurology 2013; 81(15): 1284–1290. doi: 10.1212/ WNL.0b013e3182a823ba.
33. Reuter I, Mehnert S, Sammer G et al. Efficacy of a multimodal cognitive rehabilitation including psychomotor and endurance training in Parkinson‘s disease. J Aging Res 2012; 2012: 235765. doi: 10.1155/ 2012/ 235765.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2020 Issue 1
Most read in this issue
- Novorozenecké záchvaty – současný pohled na problematiku
- Možnosti prevence Alzheimerovy choroby
- Primární non-Hodgkinův B-lymfom centrálního nervového systému
- Neuropsychiatrické symptomy jako časná manifestace Alzheimerovy nemoci
