Bolesti hlavy v graviditě
Headaches in pregnancy
The headache during pregnancy represents a specific issue. This complaint is quite common, but the treatment possibilities are limited at that period. In general, the incidence of secondary headaches including serious or life-threatening conditions may increase during pregnancy. Headache may also represent the first symptom of serious systemic complications of pregnancy. This article thus provides an overview of primary and secondary headache disorders, available diagnostic methods and therapeutic options in pregnant women. If the headache occurs for the first time in a pregnant woman, it is necessary to rule out serious secondary types of headache, e.g., pre-eclampsia, cerebral venous sinus thrombosis or intracerebral haemorrhage, which can be life-threatening. In contrast, primary headaches usually improve during pregnancy. About 70% of female patients suffering from primary headache disorders (especially migraine without aura) report improvement or complete remission of migraine attacks during pregnancy. The rest of women requires proper acute or prophylactic therapy, which is rather complicated with regard to teratogenic effect of many drugs.
Keywords:
headache – pregnancy – Migraine – pre-eclampsia – intracranial sinus thrombosis – diagnostic imaging
Autoři:
A. Rajdová 1,2; E. Vlčková 1,2; I. Niedermayerová 1,3; A. Šprláková-Puková 2,4; J. Bednařík 1,2
Působiště autorů:
Neurologická klinika, Centrum pro, diagnostiku a léčbu bolestí hlavy, FN Brno
1; LF MU, Brno
2; Neurologie Brno s. r. o.
3; Klinika radiologie a nukleární, medicíny FN Brno
4
Vyšlo v časopise:
Cesk Slov Neurol N 2020; 83/116(3): 269-276
Kategorie:
Přehledný referát
doi:
https://doi.org/10.14735/amcsnn2020269
Souhrn
Bolesti hlavy v graviditě představují do jisté míry specifickou problematiku: jedná se o poměrně časté obtíže, možnosti jejich farmakoterapeutického ovlivnění jsou však omezené. Navíc je v tomto období zvýšený výskyt některých závažnějších příčin bolestí hlavy a bolest hlavy může být dokonce prvním příznakem závažných systémových komplikací gravidity. Tento článek proto podává přehled o primárních a sekundárních bolestech hlavy, jejich diagnostice a základních možnostech terapie u těhotných žen. Pokud se u těhotné ženy nově objeví bolesti hlavy, je vždy nutné nejdříve vyloučit sekundární příčiny, jako je např. rozvíjející se preeklampsie, trombóza mozkových splavů či intracerebrální krvácení. Tyto jednotky mohou pacientky dokonce ohrozit na životě. Primární bolesti hlavy (zejména migréna bez aury) se během gravidity naopak až u 70 % žen zlepšují, případně dokonce úplně vymizí. U ostatních je pak volba akutní a zejména profylaktické terapie poměrně komplikovaná s ohledem na teratogenní účinky řady preparátů.
Klíčová slova:
bolesti hlavy – gravidita – migréna – preeklampsie – trombóza mozkových žilních splavů – zobrazovací metody
Úvod
Bolesti hlavy patří k častým obtížím gravidních žen. Jejich poměrně frekventní výskyt v těhotenství není překvapivý vzhledem k vysoké prevalenci primárních bolestí hlavy v běžné populaci a jejich výskytu zejména u žen a spíše v mladším věku. Většina bolestí hlavy sama odezní (jsou tzv. self-limited) a má nezávažnou příčinu. Zejména v případě nově se objevujících bolestí hlavy, kterými pacientka dosud netrpěla, je ale nutné vyloučit závažnější etiologické faktory.
Diagnostika bolestí hlavy v graviditě
Klíčovým nástrojem v odlišení potenciálně závažných příčin bolestí hlavy je anamnéza doplněná o klinické a fyzikální vyšetření a případně o vyšetření zobrazovací a/nebo vyšetření mozkomíšního moku z lumbální punkce.
Anamnéza umožní zejména odlišit pacientky s akutní, nově vzniklou bolestí hlavy (nebo s novým odlišným charakterem bolestí oproti dlouhodobé normě pacientky) od žen s chronickými či epizodickými bolestmi hlavy, které byly přítomny již před graviditou a v jejím průběhu významně nemění charakter ani nezvyšují intenzitu. V případě recidivujících či chronických bolestí hlavy jde pravděpodobně o primární bolest hlavy (nejčastěji tenzní typ bolesti hlavy či migrénu), které snižují kvalitu života pacientek, ale jinak je závažněji neohrožují.
Akutní (nově vzniklé) bolesti hlavy u ženy bez předchozí anamnézy podobných obtíží naopak vždy představují potenciální riziko závažné vyvolávající příčiny vyžadující došetření. Závažné jsou zejména určité specifické klinické obrazy (tab. 1).
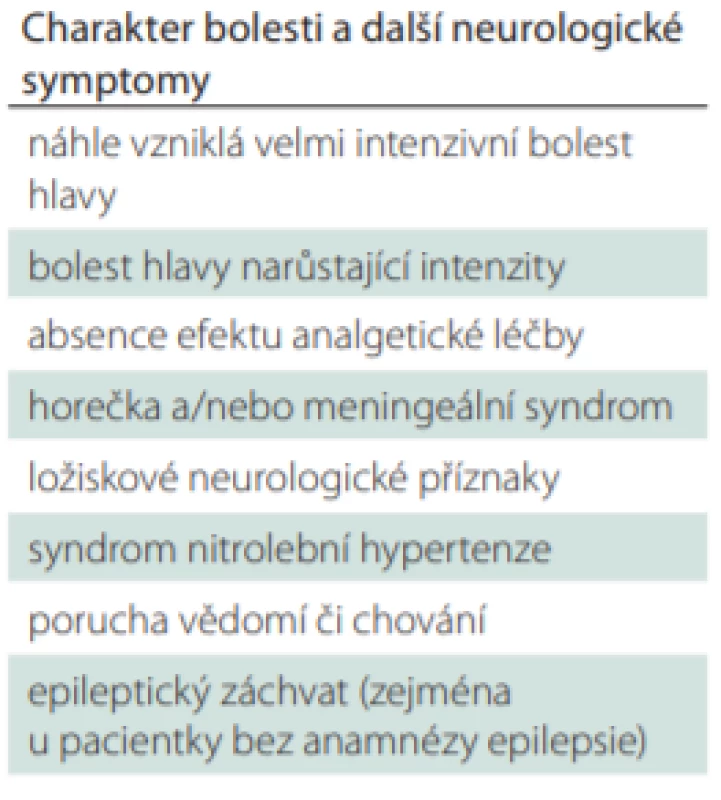
V těchto případech je vždy nutné vyloučit závažnější sekundární příčiny bolesti hlavy, např. preeklampsii, neuroinfekce (meningitidy, encefalitidy), CMP (třeba subarachnoidální krvácení či trombózu splavů) nebo nitrolební expanzivní procesy.
Velmi důležité je správné rozpoznání jiné etiologie bolestí hlavy u pacientek s anamnézou migrenózní či tenzní bolesti hlavy, která byla přítomna již v období před graviditou. I tyto pacientky mohou samozřejmě trpět některou ze závažných příčin bolestí hlavy. Je proto nutné se jich aktivně dotazovat na případnou změnu charakteru bolesti či nárůst intenzity oproti jejich dlouhodobé normě. Taková změna je důležitou varovnou známkou naznačující možnost sekundární potenciálně závažné etiologie bolestí.
V případě výše zmíněných rizikových klinických obrazů je klíčové vyloučit sekundární bolesti hlavy, a to zejména pomocí zobrazovacích vyšetření. Vyšetření CT je rychlé a v detekci akutního krvácení má přednost před MR. Radiační dávka pro matku i plod je při použití současných přístrojů nízká. Množství průkazů o bezpečnosti tohoto vyšetření je však omezené. Nelze proto vyloučit, že vyšetření CT matky v období gravidity poněkud zvyšuje riziko následujících komplikací:
- malformací plodu;
- nádorů ve fetálním období (zejména leukemie) či vyskytujících se později během dětství či dokonce dospělosti;
- katarakty plodu;
- růstové nebo kognitivní retardace plodu [1].
Z těchto důvodů je těhotenství nadále považováno za relativní kontraindikaci vyšetření CT [1]. Jeho indikace by proto měla být vždy uvážlivá a vyšetření by mělo být provedeno pouze v případě, kdy možný diagnostický benefit jednoznačně převažuje potenciální rizika, o nichž musí být pacientka informována (především tedy v případě potenciálního ohrožení života matky). Kromě expoziční dávky a hmotnosti matky je klíčovým faktorem určujícím bezpečnost vyšetření CT gestační věk plodu: riziko je vyšší mezi 8. a 15. týdnem gravidity, tedy v období organogeneze a následně v časném období zrání mozku. V tomto stadiu gravidity je vhodné přistupovat k indikaci vyšetření CT velmi obezřetně [1]. Jednoznačně je v období těhotenství doporučeno omezit použití jódových kontrastních látek pro riziko suprese funkce štítné žlázy u plodu.
Z výše uvedených důvodů je proto u gravidních pacientek obecně preferovaným vyšetřením MR, a to s výjimkou výše uvedené diagnostiky akutní hemoragie, kdy diagnostický benefit pro matku převáží rizika pro plod. V ostatních případech je MR považována za bezpečnější. Žádné závažné nežádoucí účinky vyšetření MR na matku či plod nebyly dosud popsány. Doporučuje se pouze maximální omezení kontrastních vyšetření s použitím gadolinia (které dle animálních modelů prostupuje přes placentu do fetální cirkulace a může vyvolat malformace plodu či spontánní aborty). Nekontrastní zobrazení cévního řečiště – MRA či MR venogram – jsou jednoznačnou metodou volby v indikaci zobrazení cévních struktur v graviditě [1]. Při podezření na disekci či trombotický uzávěr přívodných mozkových tepen je preferováno UZ vyšetření, které je pro matku i plod zcela nezatěžující. Limitem však v některých případech může být dostupnost vyšetření v akutní fázi.
V případě podezření na neuroinfekci jako příčinu bolestí hlavy lze provést vyšetření mozkomíšního moku z lumbální punkce. Toto vyšetření nemá negativní vliv na plod ani na graviditu a jeho indikace není v těhotenství omezena. V pokročilých stadiích gravidity spojených s výraznější hyperlordózou bederního úseku páteře však může být vyšetření obtížněji technicky proveditelné. Podobně jako v období mimo těhotenství lze vyšetření provádět vsedě či vleže na boku. I pro období gravidity platí, že výběr vhodné polohy při lumbální punkci záleží na rozhodnutí lékaře a jeho domluvě s pacientkou a nejsou k dispozici odborná doporučení jednoznačně preferující některou z uvedených poloh.
Primární bolesti hlavy
Jako primární bolesti hlavy je označována skupina onemocnění s recidivujícími či chronickými bolestmi hlavy, které nemají zřejmou vyvolávající příčinu (strukturální, metabolickou apod.). Bolest hlavy zde tedy představuje vlastní onemocnění. K nejčastějším jednotkám v této skupině patří tenzní typ bolesti hlavy (tension type headache; TTH) a migréna [2].
Migréna
Migréna se u žen vyskytuje asi 3× častěji než u mužů. Celoživotní prevalence migrény v ženské populaci je přibližně 25 % [3]. Recentní studie uvádějí prevalenci dokonce až 40 % [4]. Incidence se pak pohybuje kolem 15 % [3]. Bolest hlavy u této jednotky je typicky pulzující a má charakter hemikranie, je střední až vyšší intenzity, zvyšuje se fyzickou aktivitou a je spojena s nevolností, zvracením, foto- a fonofobií. Asi u 20 % pacientek předchází rozvoji bolesti tzv. aura, tedy jakékoli ložiskové neurologické příznaky, objevující se 5–60 min před nástupem bolesti a případně přetrvávající i v jejím průběhu. Nejčastějším příznakem aury jsou zrakové projevy, a to iritační (např. záblesky či barevné obrazce v zorném poli) nebo zánikové (např. skotom či hemianopsie). Relativně časté příznaky jsou senzitivní (parestezie končetin či obličeje), vzácné jsou parézy nebo poruchy řeči [5].
Tenzní typ bolesti hlavy
Tenzní typ bolesti hlavy je nejčastější primární bolestí hlavy vůbec. Celoživotní prevalence těchto bolestí je podle různých zdrojů 60–90 %. Podobně jako u migrén jsou více postiženy ženy zejména produktivního věku (20–50 let). Častým spouštěčem je déletrvající stres. Bolest je obvykle tupá, tlaková, oboustranná či difuzní, pociťovaná zejména v týle s propagací do čela a za oči (popisovaná např. jako pocit „těsné čepice“ či „obruče kolem hlavy“), nižší až střední intenzity. Trvá desítky minut až dny. Nemá pulzující charakter, významně se nemění fyzickou námahou, neinterferuje s běžnými denními aktivitami. Typicky není provázena nevolností a zvracením, může však být přítomna mírná foto- či fonofobie [6].
Pacientky s primárními bolestmi hlavy obecně (tedy jak s migrénou, tak s TTH) většinou zaznamenají v době gravidity snížení frekvence a intenzity obtíží, jež souvisejí s navyšující se hladinou estrogenů a zřejmě i s omezením cyklického kolísání hormonálních hladin v těhotenství [7]. Zmírnění potíží popisuje již od prvního trimestru gravidity více než polovina pacientek, v pozdějších fázích těhotenství dokonce až tři čtvrtiny z nich [8-11]. Vyšší pravděpodobnost zlepšení je u pacientek s migrénou bez aury. U 8–10 % pacientek však dojde naopak ke zhoršení obtíží, a to zejména v prvním trimestru [7,12]. Ke zhoršení mají tendenci zejména pacientky s migrénou s aurou, u nichž se v graviditě mohou objevovat i izolované aury bez migrény [10]. Primární bolesti hlavy se mohou v těhotenství objevit i de novo (u pacientek bez anamnézy podobných obtíží před graviditou). Podle velkých populačních studií se migréna nově objeví až u 16,5 % gravidních pacientek, a to zejména v prvním trimestru [8]. V těchto případech je však nutné vždy zvažovat možnost sekundární (potenciálně závažné) příčiny bolestí. V poporodním období dochází u většiny pacientek k relapsu bolestí hlavy, a to signifikantně častěji u nekojících matek, zatímco kojení (zřejmě v důsledku s ním spojené absence ovulace) jednoznačně prodlužuje období bez bolestí hlavy [9,13].
Pokud se jedná o pacientky s preexistujícími bolestmi (beze změn jejich charakteru), nejsou nutná žádná specifická došetření. Na místě je zklidnění pacientky, doporučení úpravy režimových opatření (dostatek spánku, omezení stresových faktorů, dostatečná hydratace, vynechání dietních spouštěčů záchvatů, pokud jsou pacientce známy). Podobný přístup lze s určitou obezřetností volit v případě nových bolestí hlavy, jejichž klinický obraz je zcela charakteristický pro migrénu, případně TTH. Podmínkou takového přístupu je, že u pacientek nejsou přítomny ložiskové neurologické příznaky, změny vědomí či chování, meningeální jevy, syndrom nitrolební hypertenze, zvýšení krevního tlaku nebo tělesné teploty a bolest hlavy samovolně či po analgetické terapii odeznívá.
Při záchvatech primárních bolestí hlavy lze užít paracetamol, který se v graviditě jeví jako nejbezpečnější a stává se z něj analgetikum první volby, a to zejména při nižší intenzitě bolesti. Metamizol také nemá negativní vliv na plod v časných fázích těhotenství a jeho jednotlivé dávky lze v prvních 6 měsících gravidity užívat [14]. V posledním trimestru však může mít negativní vliv na ledviny a oběhový systém plodu a jeho užívání se nedoporučuje. Salicyláty nejsou v graviditě vhodné, a to zejména ve 3. trimestru, kdy mohou zvyšovat riziko neonatálního krvácení a jsou asociovány s nízkou porodní hmotností. Navíc podobně jako ostatní nesteroidní antirevmatika zvyšují riziko předčasného uzávěru Botalovy dučeje. Ostatní nesteroidní antirevmatika lze v 1. a 2. trimestru s opatrností použít. Dle souhrnu údajů o léčivém přípravku (summary of product characteristics; SPC) je vždy nutné posoudit riziko pro plod a přínos pro matku. Pro terapii migrény či TTH lze při individuálním zvážení rizika během gravidity využít ibuprofen, naproxen, diklofenac, nimesulid, ketoprofen či dexketoprofen. Opioidy obecně pravděpodobně neškodí plodu (pokud nejde o pravidelnou medikaci), ale mohou zhoršovat těhotenskou nevolnost a zvracení a nejsou ani u primárních bolestí hlavy příliš účinné. Při použití v předporodním období navíc mohou způsobit dechovou supresi u novorozence. Při pravidelném užití vedou po porodu k rozvoji abstinenčních příznaků u novorozence. Nejčastěji využívanými opioidy jsou tramadol a kodein. Dle SPC by však tramadol neměl být těhotným ženám podáván, protože není k dispozici dostatek údajů o jeho bezpečnosti. U kodeinu, který je k dispozici v kombinovaných preparátech s paracetamolem, je pak doporučeno zvážit přínos a riziko, a to zejména ve 3. trimestru a předporodním období s ohledem na možný rozvoj dechových potíží u novorozenců.
Metoklopramid může být užíván k omezení nevolnosti a zvracení. Naopak ondansetron pravděpodobně zvyšuje riziko rozštěpů patra a jeho použití v graviditě se spíše nedoporučuje, pokud přínos podání jednoznačně nepřevýší možné riziko pro plod [15]. Existují narůstající důkazy o bezpečnosti triptanů v graviditě [16–18]. V minulosti bylo doporučeno nepodávat triptany zejména ve 3. trimestru gravidity pro riziko spontánních potratů, předčasných porodů a nízké porodní hmotnosti. Recentní studie [18] však zvýšený výskyt těchto komplikací neprokazují, což hovoří proti kontraindikaci triptanů ve 3. trimestru těhotenství.
Podle recentních studií tedy užití sumatriptanu nebylo na velkých souborech pacientek asociováno s vyšším výskytem malformací plodu, negativním vlivem na průběh gravidity ani závažnými nežádoucími účinky a tento lék je možné použít pro léčbu migrény v těhotenství v případech, kdy předpokládaný přínos pro matku převýší možné riziko pro plod [19].
Jednoznačně kontraindikovány jsou naopak ergotaminy, které mohou v důsledku vazokonstrikčního efektu snižovat prokrvení dělohy [20].
Profylaktickou léčbu migrény je v graviditě vhodné (a možné) ve většině případů vysadit [21]. V případě frekventních záchvatů lze však zvážit její ponechání či nové nasazení. Využít můžeme zejména betablokátory (propranolol, metoprolol) [19,21], ev. amitriptylin [19]. Vždy je však nutné zvážit případný benefit ve smyslu zmírnění frekvence a/nebo intenzity bolestí a možná rizika pro plod. Navíc je nutné zohlednit údaje SPC, které připouštějí možnost podávat gravidním ženám betablokátory (metoprolol) i amitriptylin pouze v případě, že je jejich použití nevyhnutelné a po pečlivém zvážení případného pozitivního účinku a možných rizik. Metoprolol pravděpodobně omezuje placentární perfúzi a může vyvolat bradykardii, arteriální hypotenzi a hypoglykémii u plodu. Proto by jeho podávání mělo být ukončeno 48–72 h před porodem a/nebo by novorozenci měli být po porodu pečlivě monitorováni. Amitriptylin může při podávání těhotným ženám vést u novorozence k rozvoji abstinenčních příznaků. Z blokátorů kalciových kanálů není flunarizin v ČR t.č. dostupný ve formě hromadně vyráběného ani individuálně připravovaného léčebného přípravku. U verapamilu nejsou adekvátní studie reflektující podávání přípravku v těhotenství k dispozici. Aktuální doporučení Státního ústavu pro kontrolu léčiv proto udává, že by tento léčivý přípravek neměl být v těhotenství užíván, pokud to není zcela nezbytně nutné.
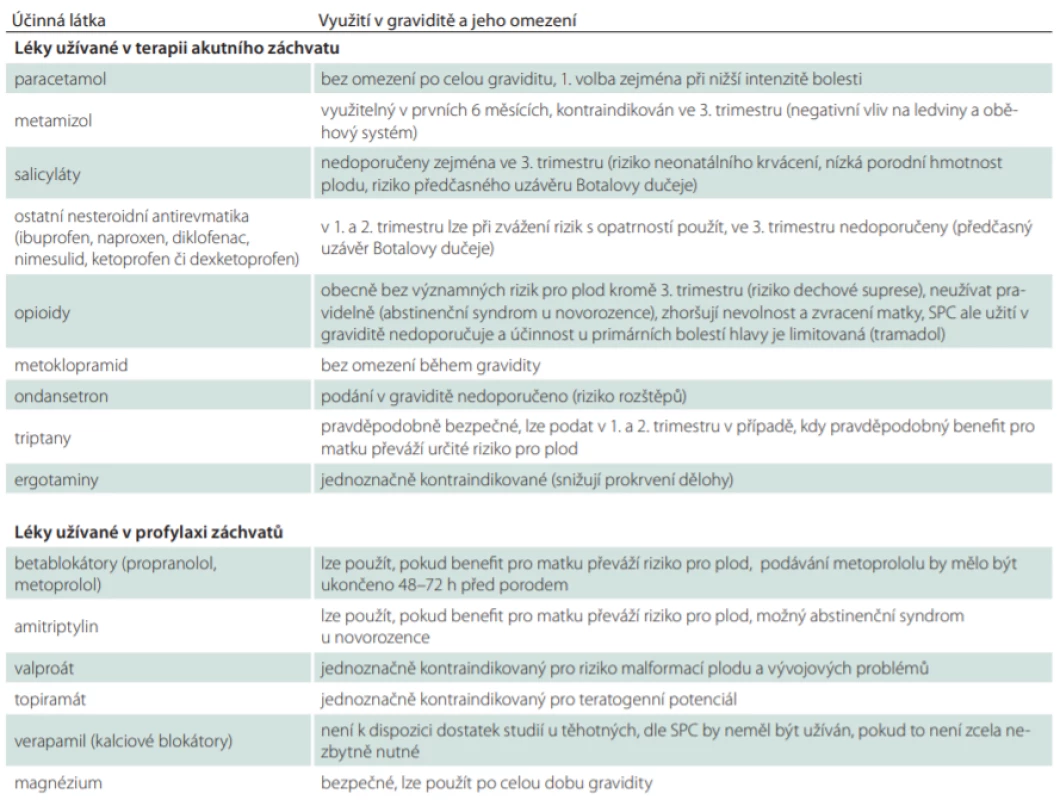
Jednoznačně kontraindikováno je použití valproátu, který zvyšuje riziko vrozených malformací (např. defektů neurální trubice, rozštěpů patra) a vývojových problémů (jako jsou opoždění psychomotorického vývoje či poruchy autistického spektra). Podobně je z důvodu prokázaného teratogenního potenciálu a asociace s výskytem velkých malformací jasně kontraindikováno použití topiramátu u gravidních žen. Z těchto důvodů by valproát ani topiramát neměly být používány pro profylaktickou léčbu migrény dokonce ani u pacientek v riziku gravidity, tedy u žen v plodném věku neužívajících vysoce spolehlivou formu antikoncepce. Naopak nejbezpečnějším lékem, který je využitelný v profylaxi migrény po celou dobu gravidity, je magnézium. Novinkou v profylaktické léčbě migrény je cílená terapie monoklonálními protilátkami proti calcitonin gene-related peptidu (CGRP) nebo jeho receptoru. Schválenou úhradu má erenuman a fremanezumab, registrovaný je galcanezumab, zatím pouze ve studiích je užíván eptinezumab. Údaje o podávání těchto látek těhotným a kojícím ženám jsou stále omezené, proto se z preventivních důvodů jejich užití v klinické praxi nedoporučuje [22] (viz SPC přípravků Aimovig či Ajovy). Souhrnné informace o možnostech léčby akutního záchvatu migrény i její profylaktické terapie v průběhu gravidity jsou uvedeny v tab. 2.
Anamnéza primárních bolestí hlavy před graviditou představuje obecně určitý rizikový faktor naznačující možnou horší prognózu bolestí hlavy u těchto pacientek během těhotenství. Jedním z faktorů je možné zanedbání správné diagnostiky jiných závažnějších vyvolávajících příčin bolestí hlavy (preeklampsie, syndrom přechodné mozkové vazokonstrikce apod.). Kromě toho mají podle kohortových studií na rozsáhlých vzorcích pacientek ženy s migrénou ve srovnání s gravidními ženami bez migrény signifikantně vyšší riziko gestační hypertenze a preeklampsie (odds ratio [OR] dle různých zdrojů až 5,81!) [23], porodu císařským řezem (OR 1,02–1,24), předčasného porodu (OR 1,13–1,39), nízké porodní hmotnosti dítěte (OR 1,03–1,31) [24] a zejména závažných cévních komplikací gravidity, např. ischemických iktů (OR 7,9–30,7) [25], akutního infarktu myokardu a dalších srdečních onemocnění (OR 4,9) a tromboembolických příhod (tedy zejména hluboké žilní trombózy s OR 2,4 a plicní embolie s OR 3,1) [26].
Závažné sekundární příčiny bolestí hlavy v graviditě
U sekundárních bolestí hlavy je bolest příznakem jiného organického (strukturálního, zánětlivého či metabolického) onemocnění (např. infekce, dekompenzované arteriální hypertenze, CMP či nádorového onemocnění mozku). U gravidních žen se samozřejmě mohou vyskytnout jakékoli bolesti hlavy, které postihují obecnou populaci. Následující výčet však zahrnuje nejvýznamnější sekundární bolesti hlavy, jejichž výskyt je vázán na graviditu a/nebo jejichž pravděpodobnost v graviditě narůstá.
Preeklampsie
Preeklampsie (těhotenská gestóza) je závažnou komplikací gravidity. Je definována jako arteriální hypertenze (systolický tlak nad 140 a/nebo diastolický nad 90 mm Hg) a proteinurie (nad 0,3 g/den ve vzorku moči sebraném za 24 h) u pacientky ve 20. a vyšším týdnu gravidity, která byla před těhotenstvím normotenzní. Postihuje asi 2–8 % gravidních žen. Klinicky se může projevovat bolestí hlavy, poruchami vidění, edémy a bolestí v oblasti epigastria. Těžké preeklampsie mohou vést k multiorgánovému selhání (projevujícímu se m.j. plicním edémem, oligurií, trombocytopenií, elevací jaterních enzymů, trvalou bolestí hlavy vysoké intenzity, rozmazaným viděním až slepotou a psychickými změnami). Pokud se objeví generalizovaný tonicko-klonický epileptický záchvat (u pacientky bez anamnézy předchozích epileptických záchvatů), stav se označuje jako eklampsie.
Léčba a sledování pacientek s preeklampsií je v rukou porodníků. Jedná se o monitoraci pacientky i plodu, podávání intravenózního magnézia jako prevence záchvatů a antihypertenziv (doporučován je zejména hydralazin a labetalol). Možným řešením je také indukce porodu, a to zejména pokud je to možné s ohledem na gestační věk plodu. Indukce je doporučována především v případě nekontrolovatelné arteriální hypertenze navzdory maximální léčbě a/nebo v případě ložiskové neurologické symptomatiky, kdy je toto opatření jednoznačně ke zvážení i přes ev. nižší gestační věk plodu [20].
Syndrom reverzibilní encefalopatie v zadní cirkulaci
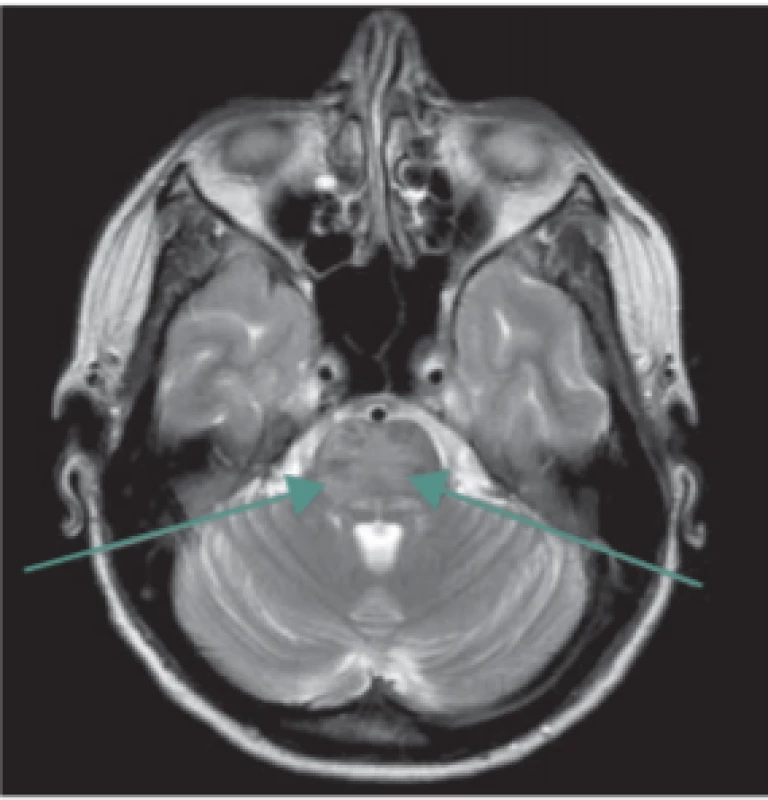
Další vzácnou komplikací, obvykle asociovanou s preeklampsií či eklampsií, je tzv. syndrom reverzibilní encefalopatie v zadní cirkulaci (posterior reversible encephalopathy syndrome; PRES syndrom) [27,28]. Jedná se o relativně novou neurologicko-radiologickou diagnózu, poprvé popsanou v roce 1996, která se může objevit i u netěhotných pacientek (např. v rámci hypertenzní encefalopatie, renálního selhání či toxické nebo imunosupresivní medikace). Klinicky je pro tento syndrom charakteristická kombinace bolesti hlavy s poruchami vidění, kvalitativní či kvantitativní poruchou vědomí, nauzeou, zvracením a generalizovanými epileptickými záchvaty. Klíčovou roli v diagnostice hraje zobrazovací vyšetření mozku (MR, případně CT), které prokáže kortikální a subkortikální edém a symetrické postižení bílé hmoty mozku zejména v zadní jámě lební (obr. 1, 2). Tento radiologický obraz i klinické symptomy jsou obvykle reverzibilní, pokud je diagnostika a léčba dostatečně rychlá, tj. provedená v řádu hodin. Terapeuticky se uplatňuje zejména důsledná a co nejrychlejší kontrola epileptických záchvatů a arteriální hypertenze (využít lze zejména MgSO4, labetalol, urapidil či nicardipin), antiedémová terapie (manitol, dexametazon, furosemid) a korekce vnitřního prostředí.
Fig. 1. Posterior reversible encephalopathy
syndrome. MRI scan, transversal T2-weight -
ed turbospin echo image – bilateral symmetrical T2 hyperintensities suggesting
edema in the occipital lobes and vascular
borderzones of basal ganglia (arrows).
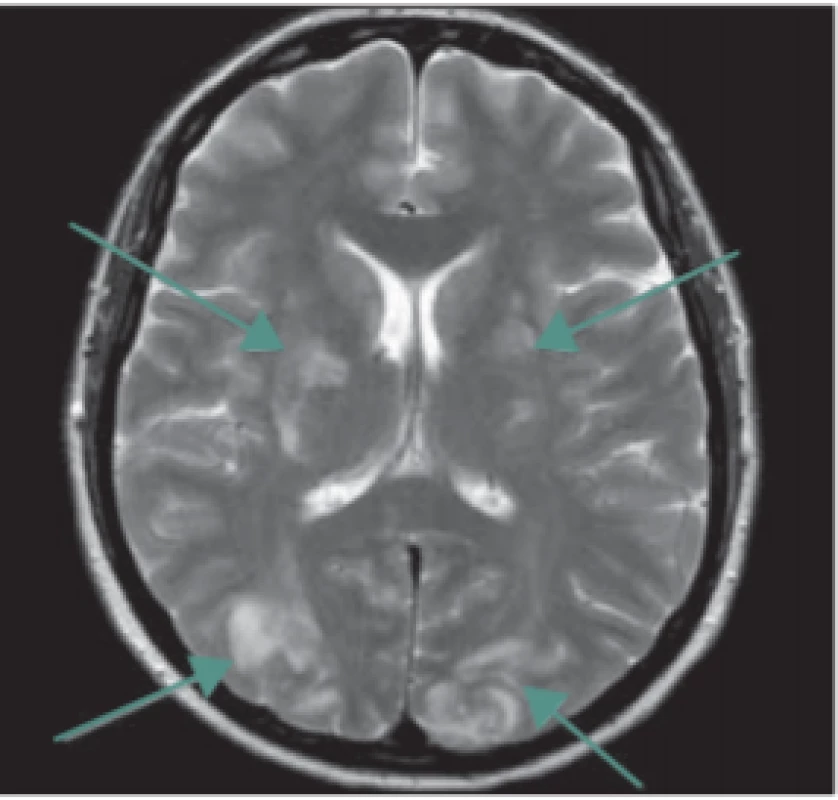
Fig. 2. Posterior reversible encephalopathy syndrome. MRI scan, transversal T2-
-weighted turbospin echo image – arrows
show pathological T2 hyperintensity in
the brainstem.
Trombóza mozkových žilních splavů
Riziko trombózy mozkových žilních splavů v graviditě narůstá, protože těhotenství představuje obecně protrombogenní stav. Nejvyšší výskyt trombóz mozkových splavů je v posledním trimestru. Klinicky se onemocnění projevuje bolestí hlavy (typicky subakutní, většinou tenzního charakteru, někdy pozvolna narůstající intenzity), často spojenou s ložiskovou neurologickou symptomatikou, epileptickými záchvaty, kvalitativní nebo kvantitativní poruchou vědomí a/nebo syndromem intrakraniální hypertenze.
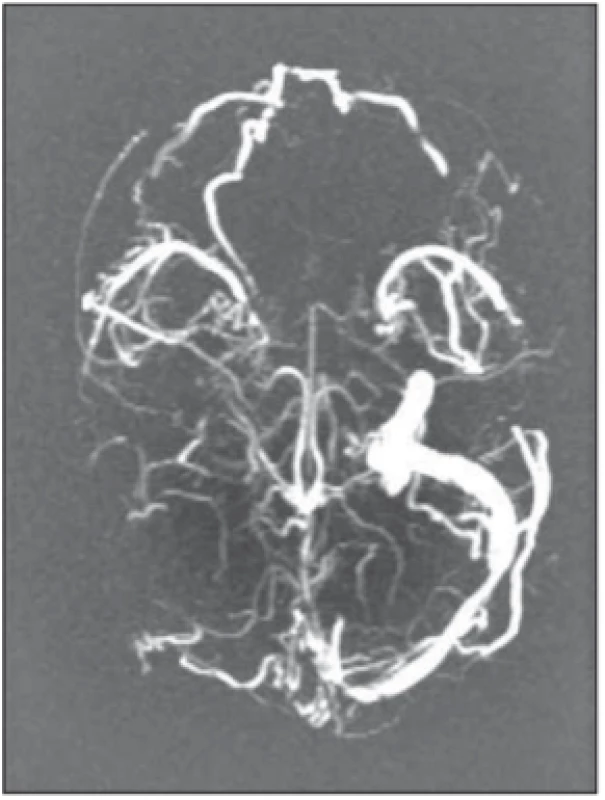
Diagnostika je založena na zobrazovacích vyšetřeních. Nekontrastní vyšetření CT může ukázat nespecifický edém či ischemii, případně další známky naznačující možné postižení (empty delta sign, dense triangle sign, cord sign). Až u 30 % pacientek je však nález normální (zejména pokud je vyšetření provedeno v prvních 5–10 dnech trvání onemocnění). Metodou volby je tedy jednoznačně nekontrastní vyšetření MR vč. MR venogramu (obr. 3) [1,20,29].
Fig. 3. Cerebral venous sinus thrombosis.
MRI venography, maximum intensity
projection reconstruction – the absence
of normal fl ow in the superior sagittal, right transverse and right sigmoid
sinuses.
V terapii se uplatňují především antikoagulancia. Lékem první volby jsou nízkomolekulární hepariny (low-molecular-weight heparin; LMWH), které neprocházejí přes placentu. Léčba by měla trvat alespoň 6 týdnů i v poporodním období a její celkové trvání je doporučováno mezi 3 a 6 měsíci. V poporodním období lze bez problémů užívat i warfarin, který je však v graviditě kontraindikován. Léčebná opatření zahrnují i léčbu intrakraniální hypertenze (pokud je přítomna) a/nebo další symptomatickou terapii při výskytu jiných komplikací (antiepileptika apod.) [20].
Apoplexie hypofýzy
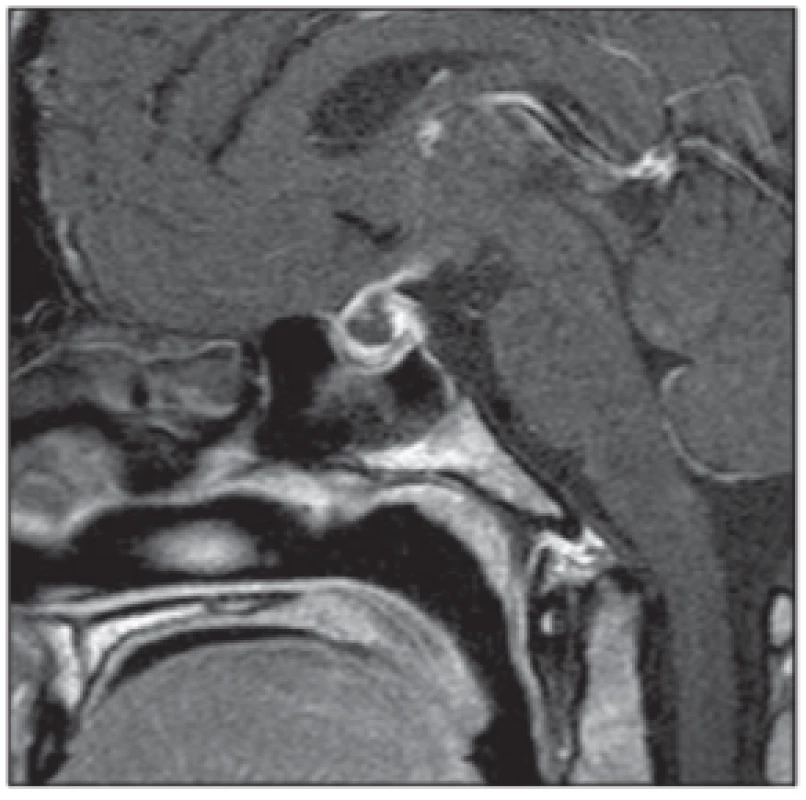
Pituitární apoplexie je vzácná cévní komplikace vyvolaná akutní hemoragií či ischemií hypofýzy. Vzniká obvykle v souvislosti s jejím růstem (nejčastěji při hypofyzárním adenomu, do té doby často klinicky němém) a související kompresí arteriálního či venózního cévního zásobení. Onemocnění se většinou vyskytuje u mužů vyššího věku. V těhotenství dochází k hyperplazii hypofyzárních buněk, které produkují prolaktin. To může v graviditě vést k nárůstu objemu hypofýzy až o 130 %, což je podkladem zvýšeného rizika rozvoje této komplikace u gravidních žen (obr. 4).
Fig. 4. Pituitary apoplexy. MRI scan,
sagittal contrast enhanced T1-weighted image – enlarged pituitary gland
with post-contrast nonhomogeneous
enhancement.
Klinicky se onemocnění nejčastěji projevuje náhle vzniklou bolestí hlavy vysoké intenzity, spojenou s nevolností a zvracením a případně se zrakovými symptomy či kvalitativní nebo kvantitativní poruchou vědomí [20,30]. Ze zrakových symptomů je nejčastější porucha některého z okohybných nervů (klinicky se projevující akutní diplopií) při jeho kompresi v oblasti kavernózního sinu v souvislosti s náhlým nárůstem objemu hypofýzy. Může také jít o oboustranné zhoršení zrakové ostrosti a/nebo výpadky zrakového pole (nejčastěji bitemporální heteronymní hemianopsii), vzácně i o Hornerův syndrom [31]. Sekundární hypopituitarizmus (jako důsledek postižení hypofýzy) může následně vést k arteriální hypotenzi a hyponatremii, které mohou být i život ohrožující [20].
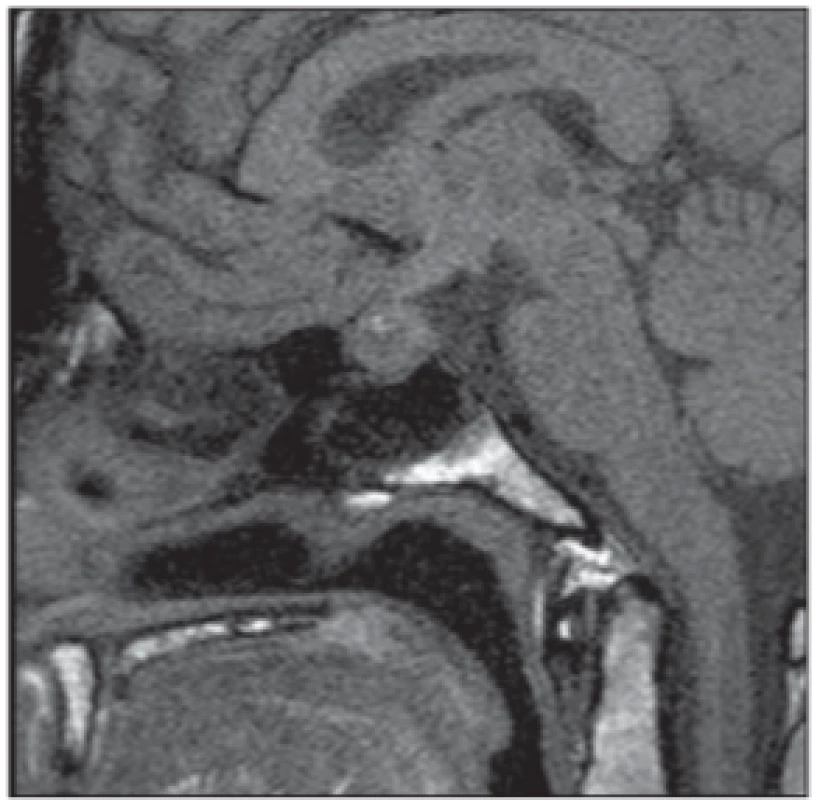
Z diagnostických metod je vhodnější MR (obr. 5), recentní hemoragii v oblasti hypofýzy však lze prokázat i nekontrastním vyšetřením CT.
Fig. 5. Pituitary apoplexy. MRI scan,
sagittal T1-weighted image – enlargement of the pituitary gland (including pituitary stalk) with nonhomogeneous signal intensity and T1 hyperintense areas
corresponding bleeding.
Terapeuticky se v případě hormonální insuficience uplatní podávání hydrokortizonu (a ev. dalších hormonů), současně je nutné korigovat případnou elektrolytovou dysbalanci. U pacientek s poruchami vidění, fokálními neurologickými deficity a/nebo s poruchou vědomí je ke zvážení urgentní dekomprese [20,30].
Subarachnoidální krvácení
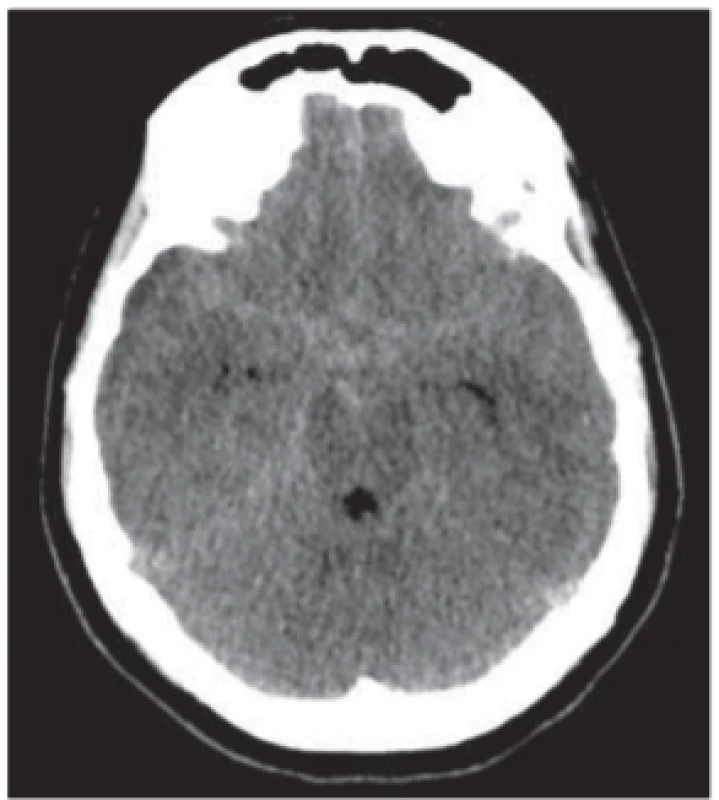
Gravidita a puerperium byly tradičně považovány za období zvýšeného výskytu subarachoidálního krvácení (SAK) (obr. 6) oproti běžné populaci. Recentní studie a metaanalýzy však ukazují, že gravidita ani porod nepředstavují zřejmě signifikantně zvýšené riziko SAK oproti riziku populačnímu [32,33]. Pokud ke krvácení v graviditě dojde, pak ruptura arteriovenózní malformace nastává typicky v časné fázi těhotenství (15.–20. týden gravidity), a to spíše u mladších žen (20–25 let). K ruptuře aneuryzmatu dochází většinou naopak později (mezi 30. a 40. gestačním týdnem), a to spíše u starších těhotných [20]. Klinické projevy, diagnostika ani terapie se v graviditě neliší od běžných doporučení.
Fig. 6. Subarachnoid hemorrhage.
CT scan – hyperdensities in the basal
cisterns and subarachnoid space.
Disekce přívodných mozkových tepen
Disekce a. carotis či a. vertebralis je další potenciální příčinou závažných sekundárních bolestí hlavy, zejména u mladších jedinců, manifestující se kromě unilateriální bolesti hlavy a krku většinou také ložiskovými neurologickými příznaky (v závislosti na postiženém povodí), případně výskytem Hornerova syndromu. Publikováno bylo několik případů disekce mozkových tepen jako příčiny bolestí hlavy v graviditě, výskyt této CMP v období těhotenství však zřejmě nepřesahuje riziko populační [20]. Diagnostika a terapie se neliší od běžné populace. V terapii se uplatňuje především LMWH, podobně jako při léčbě trombózy intrakraniálních splavů. Po porodu lze pacientky převést na warfarin. Zvážit lze možnost endovaskulární terapie (angioplastika, stent).
Idiopatická intrakraniální hypertenze
Idiopatická intrakraniální hypertenze se obecně vyskytuje zejména u mladých obézních žen v plodném věku. Její výskyt v graviditě je opět prokazatelně vyšší oproti běžné populaci. Může se objevit v kterémkoli trimestru. Onemocnění nemá negativní vliv na průběh gravidity ani na plod, případné negativní následky pro zrak jsou u těhotných pacientek prognosticky obdobné jako v období mimo graviditu. Terapeuticky lze (kromě redukce váhy a případně opakovaných lumbálních punkcí redukujících intrakraniální hypertenzi) využít acetazolamid (inhibitor karboanhydrázy, který snižuje produkci mozkomíšního moku). V minulosti byl zvažován možný teratogenní potenciál tohoto léku, v roce 2013 však byla publikována metaanalýza [34] zaměřená na podávání acetazolamidu u těhotných žen, která neprokázala vyšší výskyt vrozených vývojových vad ani abortů při užití tohoto léku. Užívání acetazolamidu u těhotných žen se tudíž jeví jako bezpečné a v oprávněných případech jej lze v graviditě podávat. Alternativou je zavedení lumboperitoneálního či ventrikuloperitoneálního shuntu, u nějž však během gravidity dochází až v 50 % ke komplikacím v podobě obstrukce či infekce shuntu [35]. Podobně jako v běžné populaci lze při nedostatečném efektu uvedených opatření a závažné či progredující poruše zraku zvážit chirurgickou fenestraci pochev optických nervů [35].
Meningitidy a encefalitidy
Výskyt neuroinfekcí v graviditě zřejmě nepřevyšuje frekvenci běžnou v populaci (s výjimkou meningitid, vyvolaných Listeria monocytogenes, které postihují predilekčně gravidní ženy) [36]. Obecně nejčastějšími bakteriálními agens vyvolávajícími meningitidy v průběhu gravidity jsou Streptococcus pneumoniae a Listeria monocytogenes [36], vzácné nejsou ani meningoencefalitidy virové, zejména herpetické (obr. 7, 8). Podobně jako v obecné populaci jsou neuroinfekce pro pacienty potenciálně letální. V graviditě navíc často vedou k úmrtí plodu, potratu či předčasnému porodu. Klinický obraz, diagnostika i terapie jsou u gravidních žen podobné jako v obecné populaci – klíčová je antibiotická terapie, která by měla být nasazena co nejdříve (ale pokud je to možné až po provedení lumbální punkce, aby nedošlo ke zkreslení kultivačních výsledků). Při možné virové příčině je vhodné přidat antivirotika (např. acyklovir). Ke zvážení je také dexametazon jako antiedémová léčba.
Fig. 7. Herpes viral encephalitis. MRI scan,
transversal T2-weighted image – pathological T2 hyperintensities in cortical/subcortical, left temporopolar and left temporomedial areas.
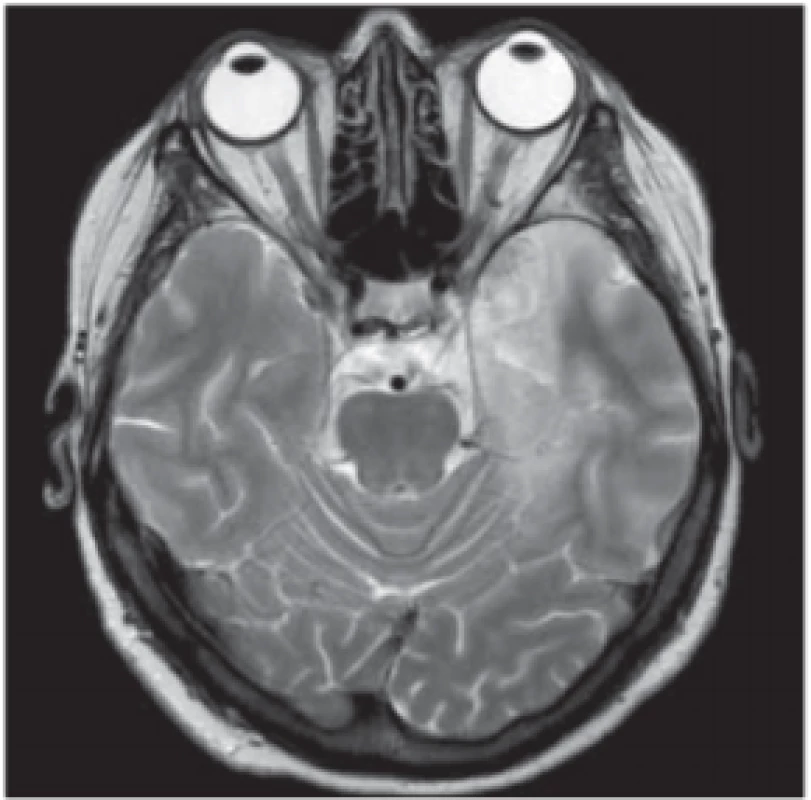
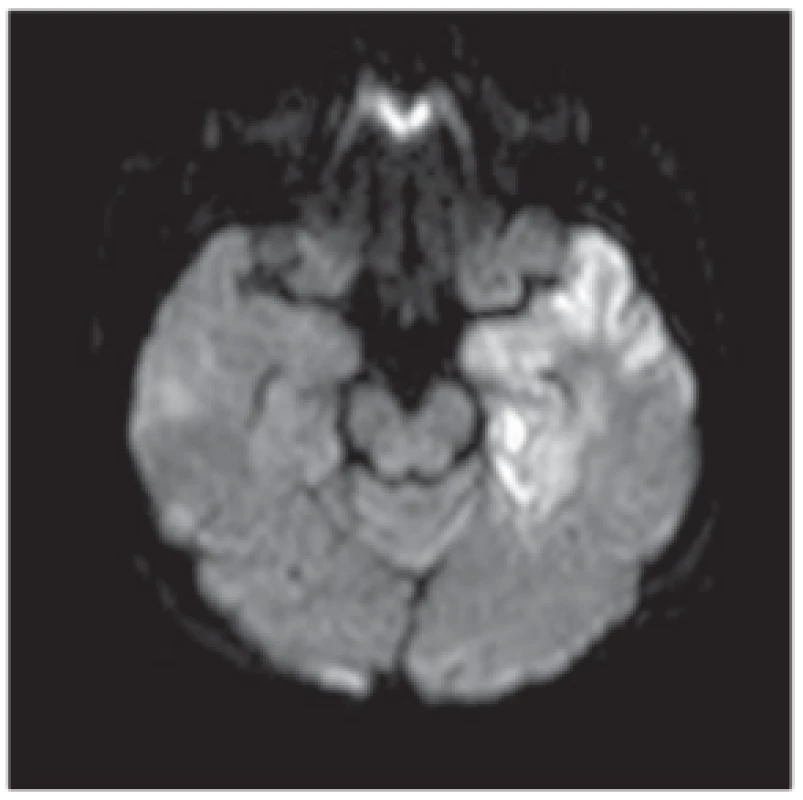
Fig. 8. Herpes viral encephalitis. MRI scan,
diff usion weighted imaging – diff usion restricted acute lesions in herpes viral encephalitis involving the left temporal lobe.
Syndrom přechodné mozkové vazokonstrikce
Syndrom přechodné mozkové vazokonstrikce (reversible cerebral vazoconstriction; RCVS) je relativně nově stanovená diagnostická jednotka způsobená přechodnou poruchou regulace cévního tonu v mozkové cirkulaci, která vede k vícečetným vazokonstrikcím a vazodilatacím na mozkových arteriích [37]. Onemocnění se může objevit bez zřejmé vyvolávající příčiny, je však častější v graviditě a zejména v poporodním období a může být asociováno s arteriální hypertenzí, případně užitím některých vazoaktivních látek (léků či ilegálních drog). Klinicky se manifestuje rekurentními epizodami náhle vzniklé intenzivní bolesti hlavy s nevolností, zvracením, foto- a fonofobií, rozmazaným viděním a přechodnou kvalitativní poruchou vědomí, objevujícími se během 1–3 týdnů. Nejvýznamnějšími komplikacemi jsou neaneuryzmatické SAK, atypicky lokalizované na konvexitě (22 % pacientů), ev. ischemický či hemoragický iktus (7 %). Jednotka je obecně poddiagnostikována, bolest hlavy bývá často nesprávně klasifikována jako migréna. Základní diagnostickou metodou je MRA (s typickým nálezem „korálkovitého“ vzhledu mozkových tepen na podkladě segmentálních vazospazmů). Specifický diagnostický test jednoznačně identifikující toto onemocnění a umožňující jeho odlišení např. od cerebrální angiitidy však není k dispozici. Léčba je prozatím spíše empirická, zahrnuje především podání kalciových blokátorů (zejména nimodipinu) a ev. vysokých dávek steroidů. Prognóza je nejistá vzhledem k možným trvalým následkům výše uvedených komplikací (zejména CMP). U většiny pacientek je však prognóza příznivá, onemocnění je pouze přechodné (self-limited) a samovolně odeznívá během 3 měsíců [37].
Grantová podpora
Práce byla podpořena z prostředků MZ ČR – RVO (FNBr, 65269705) a projektem specifického výzkumu č. MUNI/A/1325/2019 z programu podpory studentských projektů na Masarykově univerzitě.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
doc. MUDr. Eva Vlčková, Ph.D.
Neurologická klinika LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: evlckova@email.cz
Přijato k recenzi: 27. 3. 2020
Přijato do tisku: 20. 5. 2020
Zdroje
1. Skliut M, Jamieson DG. Imaging of headache in pregnancy. Curr Pain Headache Rep 2016; 20 (10): 56. doi: 10.1007/s11916-016-0585-5.
2. Headache Classification Committee of the International Headache Society (IHS). The International Classification of Headache Disorders, 3rd edition. Cephalalgia 2018; 38 (1): 1–211. doi: 10.1177/0333102417738202.
3. Rasmussen BK, Jensen R, Schroll M et al. J. Epidemiology of headache in a general population – a prevalence study. J Clin Epidemiol 1991; 44 (11): 1147–1157.
4. Faubion SS, Batur P, Calhoun AH. Migraine throughout the female reproductive life cycle. Mayo Clin Proc 2018; 93 (5): 639–645. doi: 10.1016/j.mayocp.2017.11.027.
5. Marková J. Migréna. Cesk Slov Neurol N 2009; 72/105 (3): 207–215.
6. Jay GW, Barkin RL. Primary headache disorders – part 2: tension-type headache and medication overuse headache. Dis Mon 2017; 63 (12): 342–367. doi: 10.1016/j.disamonth.2017.05.001.
7. Silberstein SD. Sex hormones and headache. Rev Neurol (Paris) 2000; 156: 4S30–4S41.
8. Kvisvik EV, Stovner LJ, Helde G et al. Headache and migraine during pregnancy and puerperium: the MIGRAstudy. J Headache Pain 2011; 12 (4): 443–451. doi: 10.1007/s10194-011-0329-1.
9. Sances G, Granella F, Nappi RE et al. Course of migraine during pregnancy and postpartum: a prospective study. Cephalalgia 2003; 23 (3): 197–205.
10. Aegidius K, Zwart JA, Hagen K et al. The effect of pregnancy and parity on headache prevalence: the Head-HUNT study. Headache 2009; 49: 851–859. doi: 10.1111/j.1526-4610.2009.01438.x.
11. Peterová V, Kron M, Vojtěchová A et al. Migréna v těhotenství. Cesk Slov Neurol N 2008; 71/104 (3): 336–341.
12. Martin VT, Behbehani M. Ovarian hormones and migraine headache: understanding mechanisms and pathogenesis – part 2. Headache 2006; 46 (3): 365–386.
13. Marcus DA, Scharff L, Turk D. Longitudinal prospective study of headache during pregnancy and postpartum. Headache 1999; 39: 625–632.
14. Státní ústav pro kontrolu léčiv (SUKL). Metamizol – dávkování, použití v těhotenství a během kojení. [online]. Dostupné z URL: http: //www.sukl.cz/metamizol-davkovani-pouziti-v-tehotenstvi-a-behem-kojeni?highlightWords=algifen.
15. Anderka M, Mitchell AA, Louik C et al. Medications used to treat nausea and vomiting of pregnancy and the risk of selected birth defects. Birth Defects Res A Clin Mol Teratol 2012; 94 (1): 22–30. doi: 10.1002/bdra.22865.
16. Ephross SA, Sinclair SM. Final results from the 16-year sumatriptan, naratriptan, and treximet pregnancy registry. Headache 2014; 54: 1158–1172. doi: 10.1111/head.12375.
17. Marchenko A, Etwel F, Olutunfese O et al. Pregnancy outcome following prenatal exposure to triptan medications: a meta-analysis. Headache 2015; 55: 490–501. doi: 10.1111/head.12500.
18. Spielmann K, Kayser A, Beck E et al. Pregnancy outcome after anti-migraine triptan use: a prospective observational cohort study. Cephalalgia 2018; 38 (6): 1081–1092. doi: 10.1177/0333102417724152.
19. Narayan B, Nelson-Piercy C. Medical problems in pregnancy. Clin Med (Lond) 2016; 16 (Suppl 6): s110–s116.
20. Schoen JC, Campbell RL, Sadosty AT. Headache in pregnancy: an approach to emergency department evaluation and management. West J Emerg Med 2015; 16 (2): 291–301. doi: 10.5811/westjem.2015.1.23688.
21. Marková J, Linhartová A. Léčba migrény během gravidity a kojení. Neurol praxi 2010; 11 (5): 300–303.
22. Bussiere JL, Davies R, Dean C et al. Nonclinical safety evaluation of erenumab, a CGRP receptor inhibitor for the prevention of migraine. Regul Toxicol Pharmacol 2019; 106: 224–238. doi: 10.1016/j.yrtph.2019.05.013.
23. Facchinetti F, Allais G, Nappi RE et al. Migraine is a risk factor for hypertensive disorders in pregnancy: a prospective cohort study. Cephalalgia 2009; 29: 286–292. doi: 10.1111/j.1468-2982.2008.01704.x.
24. Wells RE, Turner DP, Lee M et al. Managing migraine during pregnancy and lactation. Curr Neurol Neurosci Rep 2016; 16 (4): 40. doi: 10.1007/s11910-016-0634-9.
25. Bushnell CD, Jamison M, James AH. Migraine during pregnancy linked to stroke and vascular diseases: US population based casecontrol study. BMJ 2009; 338: b664. doi: 10.1136/bmj.b664.
26. Chen HM, Chen SF, Chen YH et al. Increased risk of adverse pregnancy outcomes for women with migraines: a nationwide population-based study. Cephalalgia 2010; 30: 433–438. doi: 10.1111/j.1468-2982.2009.01935.x.
27. Cozzolino M, Bianchi C, Mariani G et al. Therapy and differential diagnosis of posterior reversible encephalopathy syndrome (PRES) during pregnancy and postpartum. Arch Gynecol Obstet 2015; 292 (6): 1217–1223. doi: 10.1007/s00404-015-3800-4.
28. Jura R, Šrotová I, Adamová B et al. PRES (Posterior reversible encefalopathy syndrome) in a pre-eclamptic woman with twin pregnancy – case report. Anest intenziv Med 2015; 26 (3): 156–160.
29. Leach JL, Fortuna RB, Jones BV et al. Imaging of cerebral venous thrombosis: current techniques, spectrum of findings, and diagnostic pitfalls. Radiographics 2006; 26: S19–S43.
30. de Heide LJ, van Tol KM, Doorenbos B. Pituitary apoplexy presenting during pregnancy. Neth J Med 2004; 62: 393–396.
31. Macháčková M, Látr I, Hejcmanová D. Oční manifestace u pituitární apoplexie – kazuistika. Cesk Slov Neurol N 2009; 72/105 (5): 456–460.
32. Algra AM, Klijn CJ, Helmerhorst FM et al. Female risk factors for subarachnoid hemorrhage: a systematic review. Neurology 2012; 79: 1230–1236. doi: 10.1212/WNL.0b013e31826aace6.
33. Bateman BT, Olbrecht VA, Berman MF et al. Peripartum subarachnoid hemorrhage: nationwide data and institutional experience. Anesthesiology 2012; 116: 324–333. doi: 10.1097/ALN.0b013e3182410b22.
34. Falardeau J, Lobb BM, Golden S et al. The use of acetazolamide during pregnancy in intracranial hypertension patients. J Neuroophthalmol 2013; 33 (1): 9–12. doi: 10.1097/WNO.0b013e3182594001.
35. Kesler A, Kupferminc M. Idiopathic intracranial hypertension and pregnancy. Obstet Gynecol 2013; 56 (2): 3389–3396. doi: 10.1097/GRF.0b013e31828f2701.
36. Adriani KS, Brouwer MC, van der Ende A et al. Bacterial meningitis in pregnancy: report of six cases and review of the literature. Clin Microbiol Infec 2012; 18: 345–351. doi: 10.1111/j.1469-0691.2011.03465.x.
37. Sattar A, Manousakis G, Jensen MB. Systematic review of reversible cerebral vasoconstriction syndrome. Expert Rev Cardiovasc Ther 2010; 8 (10): 1417–1421. doi: 10.1586/erc.10.124.
Štítky
Dětská neurologie Neurochirurgie Neurologie Praktické lékařství pro dospěléČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2020 Číslo 3
Nejčtenější v tomto čísle
- Glioblastom grade IV – dlouhodobé přežití
- Bolesti hlavy v graviditě
- Primární progresivní afázie
- Kognitivní poruchy u dětí s epilepsií
