Opakovaná trombektómia u pacienta so zriedkavou kombináciou etiologických faktorov
Repeated thrombectomy in a patient with a rare combination of etiological factors
The Editorial Board declares that the manu script met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
M. Mako 1; G. Krastev 1; J. Haring 1; J. Cisár 1; A. Klepanec 2; J. Haršány 2; P. Blaško 3; P. Kurray 3
Působiště autorů:
Neurologické oddelenie, FN Trnava, Slovensko
1; Radiologická klinika FN Trnava, Slovensko
2; Kardiocentrum Nitra, Slovensko
3
Vyšlo v časopise:
Cesk Slov Neurol N 2020; 83(2): 209-211
Kategorie:
Dopis redakci
doi:
https://doi.org/10.14735/amcsnn2020csnn.eu1
Souhrn
The Editorial Board declares that the manu script met the ICMJE “uniform requirements” for biomedical papers.
Vážená redakcia,
ischemická CMP (iCMP) zapríčinená uzáverom veľkej tepny (large vessel occlusion; LVO) je devastujúce ochorenie. Endovaskulárna liečba (EVL) je účinná a bezpečná u tohto ochorenia a je štandardom v starostlivosti o pacientov v stanovenom časovom okne [1]. Takmer 25 % pacientov po iCMP prekoná recidívu počas 5 rokov [2]. Riziko recidívy LVO nie je presne stanovené, odhaduje sa zhruba na 2 % [3–5]. Etiologicky sa najčastejšie jedná o kardioembolizáciu. Výsledný stav pacientov po endovaskulárnej liečbe sa neodlišuje od outcomu pacientov po prvej mozgovej príhode [4].
U mladých pacientov je etiologické spektrum odlišné ako v staršej populácii. Perzistujúce foramen ovale je jednou z príčin kryptogénnych iCMP u týchto pacientov [6]. Predpokladaný mechanizmus je paradoxná embolizácia cez PFO. Aneuryzma predsieňového septa podstatne zvyšuje riziko paradoxnej embolizácie [7]. Podľa aktuálnych odporúčaní je indikovaný uzáver symptomatického PFO [8].
52-ročný pacient po opakovanej embolizácii do artérie pulmonalis (AP) so suspektným trombofilným stavom, ktorý ďalšou diagnostikou nebol potvrdený, bol hospitalizovaný na koronárnej jednotke intenzívnej starostlivosti pre akútne kardiorespiračné zlyhanie s potrebou katecholamínovej podpory, ktorá pretrvávala 6 týždňov bez tendencie k úprave. Pred hospitalizáciou mal pacient modifikovanú Rankinovu škálu (mRs) 0 bodov. V sekundárnej prevencii užíval rivaroxaban, pred hospitalizáciou warfarín a dabigatran. Na echokardiografickom vyšetrení bol potvrdený pokles systolickej funkcie pravej komory a progresia regurgitačného gradientu trikuspidálnej chlopne v teréne závažnej pľúcnej hypertenzie s dobrou funkciou nedilatovanej ľavej komory.
Stav pacienta sa skomplikoval náhle vzniknutou poruchou vedomia s pretrvávajúcou poruchou reči a slabosťou pravostranných končatín. V objektívnom náleze bola prítomná somnolencia, dysartria, stredne ťažká pravostranná symptomatika, National Institute of Health Stroke Scale (NIHSS) 11 bodov.
Akútne vyšetrenie CT mozgu 115 min po vzniku príznakov bolo bez čerstvých ložiskových zmien (obr. 1a), na vyšetrení CTA bola prítomná oklúzia top-of-basilaris. (obr. 1b)
Fig. 1. Non-enhanced brain CT – without acute ischemic lesions (a); CTA – top-of-basilaris
occlusion (arrow) (b); DSA – occlusion of basilar artery (arrow) (c); DSA – complete recanalization
of basilar artery occlusion (d).
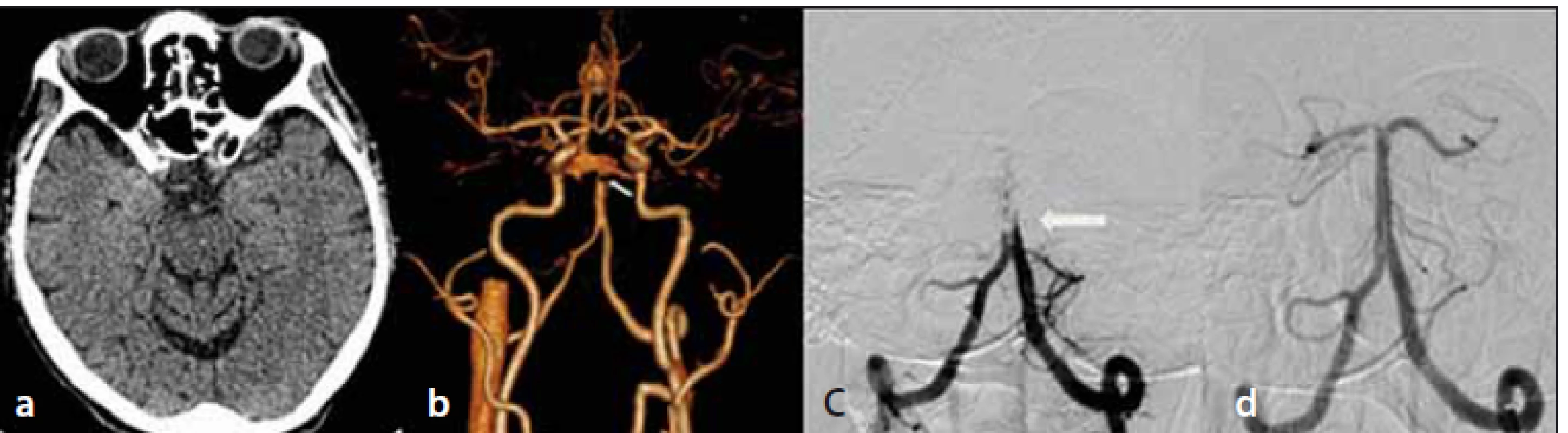
Pacientovi bola podaná intravenózna trombolýza (IVTL) v celkovej dávke 55 mg, onset-to-treatment time bol 135 min. Po 3 hodinách od zahájenia IVTL sa neurologický nález mierne zlepšil na NIHSS 9 bodov.
Pacient bol transportovaný do komplexného cerebrovaskulárneho centra za účelom EVL, onset-to-puncture time (OPT) bol 390 min. Po 10 min bola aspiračnou trombektómiou dosiahnutá rekanalizácia – Thrombolysis in cerebral infarction scale (TICI) 3 (obr. 1c, d).
Po výkone pretrvávala ľahká pravostranná symptomatika a dysartria, NIHSS 4 body. Na kontrolnom vyšetrení CT mozgu 6 h po EVL bola popísaná ischémia v pons Varoli. V sekundárnej prevencii bola podávaná duálna antiagregačná liečba – kyselina acetylsalicylová a klopidogrel; ako prevencia hlbokej žilovej trombózy (HVT) nadroparín v antikoagulančnej dávke.
Po 36 h sa stav pacienta náhle zhoršil, zvýraznila sa slabosť pravostranných končatín a porucha reči. V objektívnom náleze bola prítomná hemianopsia vpravo, hemiplégia vpravo, dysartria. NIHSS 14 bodov.
Na CT mozgu bola prítomná subakútna ischémia v cerebelle vpravo, dense artery sign a. cerebri media (MCA) vľavo (obr. 2a). Na CTA bola prítomná oklúzia M2 vľavo (obr. 2b). Zahájená bola EVL, OPT 135 min. Po 10 min bola aspiračnou trombektómiou dosiahnutá úplná rekanalizácia – TICI 3 (obr. 2c). NIHSS sa po liečbe upravilo na pôvodné 4 body.
Fig. 2. Repeated non-enhanced brain CT – dens artery sign in the left middle cerebral artery
(arrow) (a); DSA – occlusion of the left M2 (arrow) (b); DSA – complete recanalization
after endovascular treatment (c).
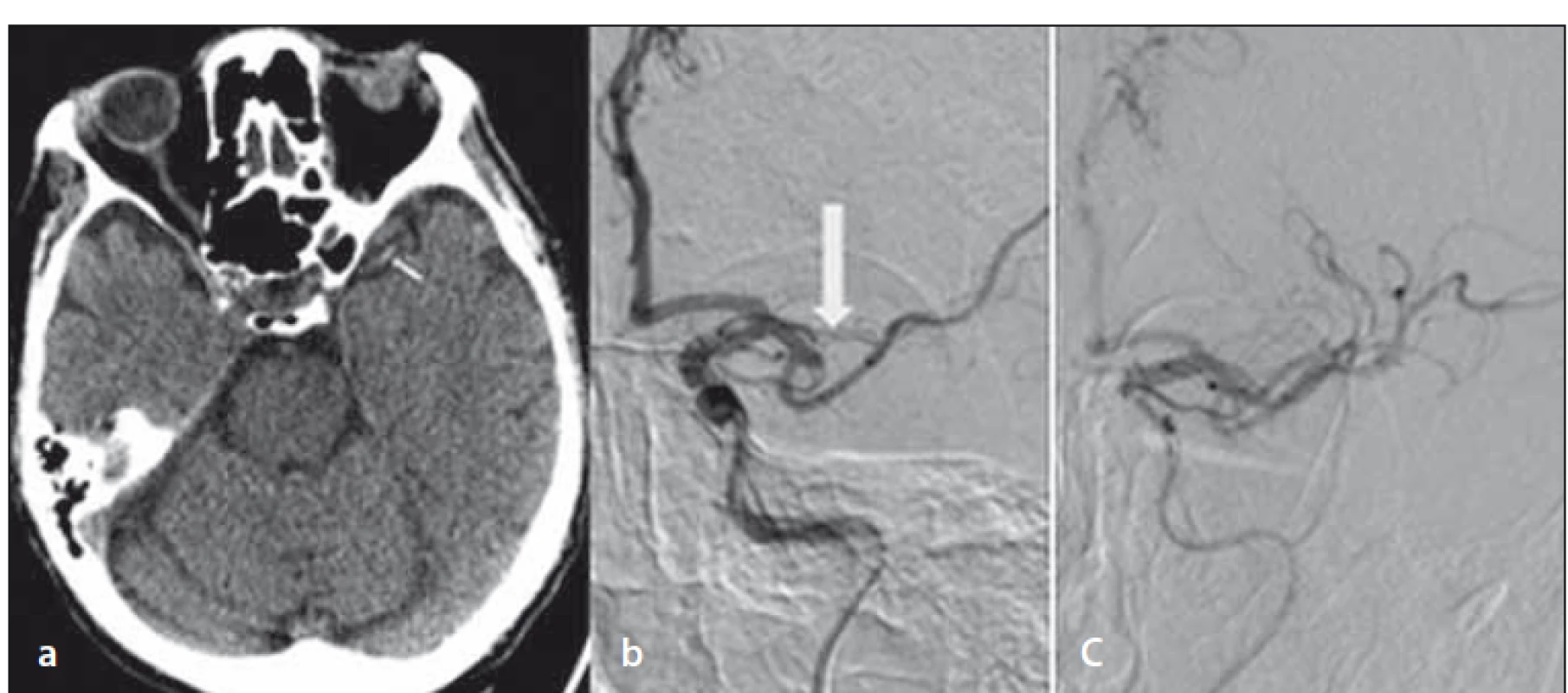
V rámci pátrania po etiológii bola doplnená detekcia pravo-ľavého skratu pomocou TCD s nálezom mnohopočetných HITS (high intenzity transient signal) pravdepodobne pri foramen ovale apertum 4. stupňa s pravo-ľavým skratom. USG vyšetrením hlbokého venózneho systému bola zistená kompletná trombóza véna femoralis superficialis vľavo a trombózou proximálneho úseku véna femoralis superficialis vpravo. Na pažerákovej echokardiografii bol potvrdený foramen ovale apertum s ľavo-pravým a závažným pravo-ľavým skratom, aneuryzma predsieňového septa vyklenujúca sa doľava. Indikovaný uzáver foramen ovale apertum (FOA) bol zrealizovaný pomocou Amplatzovho oklúdera. Vzhľadom k recidivujúcim embolizáciám do AP sme indikovali zavedenie kaválneho filtra.
Po 3 mesiacoch bol neurologický nález pacienta stabilizovaný, NIHSS 4 body, po zavedení kaválneho filtra neprekonal recidívu embolizácie do AP ani ischemickú CMP. Vzhľadom k pretrvávajúcej potrebe podpory cirkulácie katecholamínmi bol pacient aj po 3 mesiacoch pripútaný na lôžko, mRs 5 bodov. Pacient následne neprekonal recidívu ischemickej CMP ani embolizáciu do artérie pulmonalis. Počas hospitalizácie na koronárnej JIS sa rozvinula respiračná insuficiencia pri hypostatickej bronchopneumónii a pacient 5 mesiacov po EVL zomrel.
Prezentovaná kazuistika je zaujímavá z niekoľkých dôvodov. Prvý je čisto etický a týka sa medicínskej úvahy o oprávnenosti indikácie komplikovanej a finančne náročnej EVL u pacienta pripútaného na lôžko, aj keď v pomerne mladom veku. Ako vieme, pacienti s vysokým mRs sú vylúčení z klinických štúdií, a teda sú kontraindikovaní k EVL v reálnej praxi[1]. Ďalší dôvod je zriedkavý prípad opakovanej EVL pre recidívu LVO dvoch veľkých intrakraniálnych tepien v krátkom časovom úseku 36 h.
Z doteraz publikovaných dát malo asi 2 % z pacientov liečených EVL recidívu CMP vhodnú na ďalšiu EVL. Toto percento pravdepodobne podhodnocuje skutočnú frekvenciu recidívy LVO. Ovplyvňuje ju viacero faktorov vrátane toho, že závažne postihnutí pacienti po prvej NCMP nie sú kandidátmi na EVL [3–5].
Podľa nám dostupnej literatúry boli publikované 3 súbory pacientov opakovane liečených EVL. Tri práce predstavujú súbory 16, 15 a 7 pacientov, ostatné sú kazuistiky [3,4,9–16]. Zatiaľ je známy jeden prípad pacienta po solitárnej EVL s následným uzáverom FOA považovaným za etiologický zdroj, tak ako v prípade nášho pacienta [17].
V súbore 16 pacientov publikovanom Grallom s kolektívom nebola etiológia zistená v 50 % prípadov, 5 pacientov malo zriedkavú etiológiu a 3 kardioembolickú [3]. V Bouslamovom súbore 15 pacientov opakovane liečených EVL je najčastejšie sa vyskytujúcou etiológiou kardioembolizácia v 10 prípadoch, v dvoch prípadoch boli zapríčinené intrakraniálnou aterosklerózou a po jeden prípad extrakraniálnou aterosklerózou, antifosfolipidovým syndrómom a fibromuskulárnou dyspláziou. U ostatných pacientov sa etiológia neudáva [4]. V súbore našich pacientov bola najčastejšou etiológiou kardioembolizácia až v 70 % prípadov [16]. V kazuistických prácach bola najčastejšia príčina iCMP kardioembolizácia [9–15]. Myslíme si, že u nášho pacienta sa primárne jednalo o paradoxnú embolizáciu z trombózy vén dolných končatín cez FOA. Túto hypotézu podporuje zlyhanie antikoagulačnej liečby v prevencii opakovaných embolizácií do pľúcnej cirkulácie, ale neskôr aj embolizácie do CNS, ako aj nález veľkého počtu HITS pri TCD emdoldetekcie. Opakovaná EVL rekurentnej iCMP pre LVO, u ktorej je etiologická príčina paradoxná embolizácia pri FOA doteraz publikovaná nebola.
Uzáver rovnakej tepny bol medzi všetkými publikovanými pacientami prítomný u 25 pacientov, zvyšní mali uzáver inej tepny. Rovnako u nášho pacienta sa jednalo o uzáver iných tepien [3,4,9–16].
Z časového hľadiska bol rozdiel medzi prvou a druhou mozgovou príhodou 1–915 dní. 23 prípadov sa vyskytlo do 3 dní a do 90 dní spolu 34 prípadov, čo znamená že väčšina bola kontraindikovaná k podaniu IVTL. Úspešnosť rekanalizácie bola vysoká, v 98 % prípadoch na úrovni TICI 2b až 3 [3,4,9–16]. U nášho pacienta v oboch prípadoch bola dosiahnutá pomocou aspiračnej trombektómie rekanalizácia na úrovni TICI 3.
Čo sa týka bezpečnosti mal 1 pacient klinicky signifikantnú hemoragickú komplikáciu po prvej EVL, dvaja mali hemoragickú infarzáciu typ 2, čo prestavuje 7 % pacientov. Po druhom resp. treťom EVL mali traja pacienti parenchýmový hematóm typ 2 (11 %), dvaja mali SAH (7 %) a jeden hemoragickú infarzáciu typ 1 (4 %) [3,4, 9–16].
Po 3 mesiacoch malo približne 50 % pacientov dobrý výsledný klinický stav (mRs 0–2), mortalita bola približne 30 % [3–5]., jeden pacient zomrel na hemoragickú komplikáciu liečby [3,4,9–16]. Náš pacient mal po 3 mesiacoch síce vysoké mRs 5 bodov, ale to bolo zapríčinené tým, že pacient bol potrebou katecholaminergnej podpory cirkulácie pripútaný na monitorované lôžko. Reziduálne príznaky iCMP boli mierne, NIHSS bolo 4 body.
Nemenej opodstatnený je problém, či vieme odhadnúť počet pacientov, u ktorých je pre recidívu iCMP s LVO v krátkom časovom rámci indikovaná opakovaná EVL. Podľa Grallu et al ale aj podľa našich údajov z analýzy veľkého súboru pacientov po EVL sú to približne 2 % pacientov [3,16]. Tieto údaje potvrdzujú taktiež predchádzajúce informácie o bezpečnosti ale aj účinnosti týkajúce sa stupňa reperfúzie a výsledného stavu pacientov po opakovanej EVL pri recidíve iCMP s uzáverom veľkej intrakraniálnej tepny [3,9–16].
Ako vyššie uvádzame, etiologicky sa u nášho pacienta jednalo o paradoxnú embolizáciu cez FOA pri dokázanej bilaterálnej trombóze AFS. Pre zlyhanie antikoagulačnej liečby sme u pacienta indikovali uzáver FOA s následnou warfarinizáciou. Výkon bol realizovaný pomocou Amplatzovho oklúdera. V prevencii pľúcnej embolizácie sme u pacienta indikovali zavedenie kaválneho filtra.
Počet pacientov s iCMP s potvrdenou LVO z viacerých príčin narastá (zlepšenie prednemocničného a nemocničného manažmentu, rýchlej identifikácie a triáže, lepšej súčinnosti komplexných centier v SR so zložkami rýchlej zdravotnej služby). Preto predpokladáme, že sa bude zvyšovať aj počet pacientov, u ktorých správny manažment recidivujúcej CMP bude vyžadovať opakovanú EVL. Z dostupných údajov sa opakované použitie EVL pri CMP javí byť bezpečné a účinné, riziko hemoragických komplikácií a klinický výsledný stav sa nelíši od pacientov, ktorí recidívu CMP neprekonali. Na základe týchto údajov by recidíva CMP nemala byť kontraindikáciou k EVL a postupovať je potrebné rovnako aktívne ako v prípade prvotnej CMP s LVO. Vzhľadom na nízky počet pacientov (približne 2 % z celkového počtu pacientov po EVL) liečených opakovanou EVL pre recidívu iCMP, sú potrebné ďalšie dáta na potvrdenie bezpečnosti a účinnosti tohto postupu pri recidíve LVO [3,4,16].
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Miroslav Mako
Neurologické oddelenie
FN Trnava
Tamaškovičova 7526/9
917 01 Trnava
Slovensko
e-mail: makomiroslav@yahoo.com
Přijato k recenzi: 29. 4. 2019
Přijato do tisku: 20. 11. 2019
Zdroje
1. Goyal M, Menon BK, van Zwam WH et al. HERMES collaborators: endovascular thrombectomy after large-vessel ischaemic stroke: a meta-analysis of individual patient data from five randomised trials. Lancet 2016; 387(10029): 1723–1731. doi: 10.1016/S0140-6736(16)00163-X.
2. Mohan KM, Wolfe CD, Rudd AG et al. Risk and cumulative risk of stroke recurrence: a systematic review and meta-analysis. Stroke 2011; 42(5): 1489–1494. doi: 10.1161/STROKEAHA.110.602615.
3. Mordachini PJ, Kaesmacher J, Gautschi D et al. Predictors of unexpected early reocclusion after successful mechanical thrombectomy in acute ischemic stroke patients. Stroke 2018; 49(11): 2643–2651. doi: 10.1161/STROKEAHA.118.021685.
4. Bouslama M, Haussen DC, Rebello LC et al. Repeated mechanical thrombectomy in recurrent large vessel occlusion acute ischemic stroke. Intervent Neurol 2017; 6 : 1–7.
5. Webster MW, Chancellor AM, Smith HJ et al. Patent foramen ovale in young stroke patients. Lancet 1988; 2 : 11–12.
6. Lechat P, Mas JL, Lascault G et al. Prevalence of patent foramen ovale in patients with stroke. N Engl J Med 1988; 318 : 1148–1152.
7. Maron BA, Shekar PS, Goldhaber SZ. Paradoxical embolism. Circulation 2010; 122(19): 1968–1972. doi: 10.1161/CIRCULATIONAHA.110.961920.
8. Pristipino C, Sievert H, D´Ascenzo F et al. European position paper on the management of patient with patent foramen ovale. General apprach and left circulation thromboembolism. European Heart Journal 2018; 00 : 1–14.
9. Chiti A, Pizzanelli C, Terni E et al. A case of recurrent basilar artery occlusion successfully treated with repeated intravascular procedures. Neurologist 2011; 17 : 95–97.
10. Laible M, Möhlenbruch M, Hacke W et al. Repeated intra-arterial thrombectomy within 72 hours in a patient with a clear contraindication for intravenous thrombolysis. Case Rep Vasc Med 2015; 2015 : 872817. doi: 10.1155/2015/872817.
11. Lee Y, Yi H, Kim BM et al. Recurrent cardioembolic stroke treated successfully with repeated mechanical thrombectomy within the acute index stroke period. J Clin Neurol 2015 11 : 275–278.
12. Gory et al. Repeated Solitaire mechanical thrombectomy in an acute anterior stroke patient. Rev Neurol Paris 2015; 171(8–9): 682–684.
13. Quintas S, López RR, Ximénez-Carrillo A et al. Recur-rencia precoz de infarto cardioembólico tratada con éxito mediante una segunda trombectomía. Neurología 2017; 32 : 551–554.
14. Fandler S, Deutschmann H, Fazekas F et al. Repeated endovascular treatment of early recurrent proximal middle cerebral artery occlusion: case report and brief review of the literature. Front Neurol 2018; 9 : 289. doi: 10.3389/fneur.2018.00289.
15. Jakubíček S, Reif M, Vaníček J et al. Recurrent ischemic stroke treated with mechanical thrombectomy during a pregnancy: a case report. Proceeding of the 4th European Stroke Organisation Conference 2018, Gothenburg, Sweden: 16–18.
16. Mako M, Krastev G, Cisár J et al. Opakovaná mechanická trombektómia pri recidíve akútnej ischemickej cievnej mozgovej príhody s oklúziou veľkej intrakraniálnej tepny, Proceedings of 46. Český a Slovenský Cerebrovaskulárny Kongres; 2018 September 18–20; Mikulov, Česká Republika.
17. Fu Q, Guo X, Mo D et al. Young Paradoxical stroke treated successfully with mechanical thrombectomy using solitaire and transcatheter closure of patent foramen oval. Int Heart J 2017; 58(5): 812–815. doi: 10.1536/ihj.16-461.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2020 Číslo 2
-
Všechny články tohoto čísla
- Cévní morfologie, symptomy, diagnostika a léčba ischemických příhod mozkového kmene
- Je koncept vaskulární demence trvale udržitelný?
- Je koncept vaskulární demence trvale udržitelný? NE
- Je koncept vaskulární demence trvale udržitelný? Komenář
- Mezinárodní klasifikace bolestí hlavy (ICHD-3) – oficiální český překlad
- Schwannóm extrakraniálnej časti trojklanného nervu
- Chirurgická léčba mozkových metastáz
- Cavum septi pellucidi, cavum vergae a cavum veli interpositi
- Poměr fosforylovaného tau proteinu k beta amyloidu v likvoru predikuje pozitivitu amyloidové PET
- Provokační faktory a reakce na léčbu juvenilní myoklonické epilepsie – zkušenosti z tertiárního epileptického centra
- Chirurgická léčba benigních neurogenních tumorů mediastina – analýza 7letého souboru pacientů
- Transkraniální sonografie mediotemporálního laloku u pacientů s Alzheimerovou demencí
- Endarterektomie zevní karotické tepny
- Vestibulární funkce u pacientů s kochleárním implantátem
- Cystická hydatidóza mozečku – vzácná kazuistika
- Případ pozdní brachiální plexopatie po chemoterapii a radioterapii
- Spontánní vaginální extruze distálního katetru ventrikuloperitoneálního zkratu
- Opakovaná trombektómia u pacienta so zriedkavou kombináciou etiologických faktorov
- Dopis redakci
- Komentář redakce
- Prof. Mraček oslavil 90 let
- Odešla MUDr. Olga Baudyšová
- K jubileu profesorky Soni Nevšímalové
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Cavum septi pellucidi, cavum vergae a cavum veli interpositi
- Cévní morfologie, symptomy, diagnostika a léčba ischemických příhod mozkového kmene
- Mezinárodní klasifikace bolestí hlavy (ICHD-3) – oficiální český překlad
- Chirurgická léčba mozkových metastáz
