Porovnání peroperační radiační expozice při otevřené a miniinvazivní transpedikulární fixaci hrudní a bederní páteře
Comparison of Peri‑ operative Radiation Exposure during an Open and Miniinvasive Transpendicular Fixation of Thoracic and Lumbar Spine
Introduction:
Radiation exposure may lead to skin cancer, leukemia or cataracts. Minimally Invasive Spine Surgery (MISS) is associated with a higher risk of Radiation Exposure (RE) due to greater use of fluoroscopy during this procedure than during open surgery. The aim of this prospective study was to assess the risk of RE for both, patients and surgeons, during spinal surgery and to compare open surgery RE to that of MISS procedures.
Methods:
RE was measured throughout an18- month study period in all patients treated with transpendicular fixation (TPF). A sample of 73 patients (39 female and 34 male) was divided into two groups: Group 1 – open surgery with 37 patients and Group 2 – MISS with 36 patients. X‑ray was performed using spot fluoroscopy only. Total RE during a surgical procedure was recorded and the means for both groups were statistically analyzed and compared. Another measurement of RE was performed at the position of a surgeon during open and MISS surgeries (each group consisted of five surgeries) using a special device for detection of radiation.
Results:
The authors found statistically significantly higher RE in Group 2 (ø 6.3 mSv × cm2) compared to Group 1 (ø 3.2 mSv × cm2).
Conclusion:
Despite observed statistical significance, RE during MISS was still very low and did not exceed the annual exposure limits even at high frequency of surgeries. Therefore, intraoperative RE should not be the reason for limiting this type of spinal surgery.
Key words:
thoracic and lumbar spine – minimally invasive spine surgery – radiation exposure –transpedicular fixation
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
T. Wanek 1; M. Adamus 2; V. Novák 1; M. Homola 3
Působiště autorů:
LF UP a FN Olomouc
Neurochirurgická klinika
1; LF UP a FN Olomouc
Klinika anesteziologie a resuscitace
2; LF UP a FN Olomouc
Oddělení lékařské fyziky a radiační ochrany
3
Vyšlo v časopise:
Cesk Slov Neurol N 2013; 76/109(5): 608-613
Kategorie:
Původní práce
Souhrn
Úvod:
Expozice záření může vést k nádorovému onemocnění kůže, leukemii nebo kataraktě. S nástupem miniinvazivní spondylochirurgie se skiaskopické peroperační vyšetření stalo její nevyhnutelnou součástí. Vzhledem k riziku radiační zátěže pacientů i personálu u spondylochirurgických operací se autoři zaměřili na srovnání míry ozáření u otevřené techniky vůči miniinvazivní.
Metodika:
Během 18 měsíců byla prospektivně sledována radiační expozice u 73 pacientů operovaných transpedikulární fixací (TPF) pro onemocnění hrudní nebo bederní páteře. TPF byly provedeny buď klasickou otevřenou technikou (Skupina 1 s 37 pacienty), nebo miniinvazivní technikou (Skupina 2 s 36 pacienty). Skiaskopování sestávalo pouze z jednotlivých statických snímků, tzv. single shot. U každého výkonu byla zaznamenána hodnota celkové radiační expozice, tzn. sumační hodnota. Dále autoři provedli u 10 operačních výkonů (pět klasických a pět miniinvazivních) měření rozptýleného záření z místa postavení operatéra pomocí speciálního snímače záření.
Výsledky:
Statisticky významný rozdíl v operační radiační zátěži byl pozorován v neprospěch miniinvazivní fixace (ø 6,3 mSv × cm2) ve srovnání s otevřenou metodou (ø 3,2 mSv × cm2).
Závěr:
I při statisticky významném rozdílu se jedná o minimální dávky záření, a tudíž větší radiační expozice pacienta není faktor ovlivňující indikaci miniinvazivní perkutánní transpedikulární fixace. Při dodržení veškerých zásad radiační ochrany je ozáření operačního týmu zanedbatelné a nepřesáhne roční hygienické normy ani při velké frekvenci operací.
Klíčová slova:
hrudní a bederní páteř – miniinvazivní páteřní chirurgie – radiační expozice – transpedikulární fixace
Úvod
Riziko radiačního záření je v lékařství všeobecně dobře známo. Expozice záření může vést zejména k nádorovému onemocnění kůže a leukemii nebo kataraktě. Znepokojivé závěry přinesla v roce 2005 zpráva autorů Mastrangelo et al, kteří prokázali mnohem větší incidenci nádorových onemocnění u ortopedů (29 %) pracujících s peroperační skiaskopií ve srovnání s ostatními lékaři (11 %), nelékařským povoláním vystaveným radiační expozici (6 %) a záření neexponovaným dělníkům (4 %) [1].
Tato problematika se stala v současné době opět velmi aktuální s nástupem éry miniinvazivní spondylochirurgie (MISS, Minimally Invasive Spine Surgery), kdy je skiaskopické zobrazení jedinou možností orientace v operačním poli, a je tak během operací více využíváno. Z toho plyne i větší radiační expozice jak pacienta, tak operačního týmu [2,3].
Cílem naší práce bylo poukázat na riziko radiační zátěže pacientů a operačního týmu (vztaženo k osobě operatéra) u stabilizací hrudní a bederní páteře, a srovnat tím míru ozáření při klasických otevřených technikách oproti MISS.
Soubor a metodika
Na Neurochirurgické klinice LF UP a FN Olomouc jsme v období od září 2009 do března 2011 sledovali radiační expozici všech pacientů operovaných transpedikulární fixací (TPF) pro onemocnění hrudní nebo bederní páteře. Indikací k operacím byla převážně poranění páteře, méně často zadní stabilizace u degenerativních či onkologických onemocnění. Podmínkou zařazení do studie bylo splnění standardního protokolu. Za standard přitom bylo považováno provedení operace jedním ze dvou zkušených páteřních chirurgů, z nichž vždy jeden byl dostupný i ve službě, popřípadě pohotovostně na telefonu. Dále byla požadována přítomnost radiologického asistenta, který má zkušenosti s peroperačním rentgenováním našich spondylochirurgických výkonů, což splňuje většina zaměstnanců i v době služeb. U všech operací bylo použito jedno konkrétní C‑ rameno skiaskopu se snímacím a záznamovým zařízením pro radiační expozici.
Operační postup při otevřené TPF
Podle bočního skiagrafického zaměření u pacienta v pronační poloze byla provedena středočárová kožní incize v místě postižené etáže páteře, následovala oboustranná discize fascie podél spinózních výběžků a skeletizace páteře od střední čáry laterálně za meziobratlové klouby. Transpedikulární šrouby (Legacy, Medtronic, USA nebo USS, Synthes, Švýcarsko) byly zavedeny s využitím pouze boční skiagrafické projekce a systém byl kompletizován spojením šroubů tyčemi. Absenci předozadní skiaskopické projekce suplovaly anatomické znalosti a prostorová představivost chirurga a z toho plynoucí dobrá orientace v operačním poli. Pokud byl nutný přístup do páteřního kanálu z jakékoliv indikace, pak byl tento součástí výkonu. Následovala sutura operační rány po anatomických vrstvách.
Operační postup při MISS TPF
Podle skiagrafického zaměření pediklů v předozadní (AP, anteroposteriorní) a boční projekci v pronační poloze pacienta byly provedeny podélné kožní incize vždy oboustranně paravertebrálně cca 4– 5 cm od střední čáry. Po discizi svalových fascií byl v biplanární (dvě na sebe navzájem kolmé projekce) rentgenové projekci transmuskulárně a transpedikulárně zaveden do obratlových těl přes Jamshidi trokar Kirschnerův drát. Po tomto vodícím drátu pak již s využitím jen boční projekce byly implantovány kanylované šrouby uchycené na zaváděcích tubusech (SpiRIT, Synthes, Švýcarsko) a systém byl miniinvazivní technikou kompletizován spojením šroubů tyčemi, subfasciálně zavedenými využitím oněch tubusů na již zavedených šroubech. Pomocí těchto tubusů lze před definitivním dotažením fixace provést repoziční manévry (např. distrakci, lordotizaci). Po kompletizaci transpedikulární fixace byly tubusy sejmuty z hlavic šroubů a následovala sutura operačních ran po anatomických vrstvách.
Všechny operační výkony u obou skupin pacientů byly provedeny za použití peroperačního rentgenového C‑ ramene Philips BV300 (110 kV, 7,3 mA). Vlastní rentgenování sestávalo vždy jen z jednotlivých skiagrafických, tedy statických snímků, tzv. single shot. Nikdy nebyla použita kontinuální skiaskopie. Operační tým a veškerý personál na operačním sále používali ochranné pomůcky podle předpisů o radiační ochraně. Tzn. operatér, jeho asistent a instrumentářka měli oblečeny protiradiační ochranné zástěry, límce a brýle. Na zvyklém místě v kapse na zevní straně zástěry na levé straně hrudníku měli všichni členové operačního týmu při každém výkonu své vlastní dozimetry. Při každé jednotlivé skiagrafii (single shot) odstoupil operatér a jeho asistent na vzdálenost minimálně 1,5 metru od zářiče. Pozice instrumentářky a anesteziologického týmu byly vždy ve vzdálenosti větší než 1,5 metru od zářiče. Proto lze logicky předpokládat jejich menší vystavení ozáření (intenzita radiace klesá s druhou mocninou vzdálenosti od zdroje tohoto záření), a tudíž si dovolíme v této práci tyto osoby nezohledňovat. V případě operatéra a jeho asistenta to znamenalo odstoupení od pacienta po zabezpečení operačního pole (např. po zastavení zdroje krvácení). Při dobré anatomické znalosti páteře obecně a při dobré prostorové představivosti operatéra o anatomii obratlů konkrétního pacienta není nutné provádět kontinuální skiaskopii. K zobrazení aktuální pozice nástroje (např. Jamshidi trokar v pediklu) stačí vždy single shot. Pokud je operatér prostorově orientován v obratli jak polohou nástroje, tak trajektorií jeho zavádění, pak může pohnout nástrojem (trokarem v pediklu) bez kontinuální skiaskopie do nové pozice, kterou si vzápětí ověří dalším statickým snímkem (single shot). Během takovéhoto postupu zavádění trokaru, zejména při MISS, je významnou pomocí i pocitový vjem v ruce operatéra. Při vstupu trokarem do obratle (tzv. entry point) pociťuje tvrdý odpor kompaktní vrstvy kosti, který je někdy potřeba překonat lehkým úderem kladívka na rukojeť trokaru. Jakmile se dostaneme do obratle, je odpor spongiózní kosti menší a lze trokar zavádět relativně snadno bez kontinuálního či frekventovaného single shot snímkování. Pokud náhle odpor kosti vzroste, dá se s určitostí předpokládat, že je trokar tlačen proti kompaktě, a tudíž směrem z pediklu či z obratlového těla, což je varovné znamení. Je třeba ihned pozici nástroje zkontrolovat snímkem. Po zvládnutí této techniky se rapidně sníží radiační expozice u dalších výkonů (learning curve).
Radiologický asistent na závěr každého výkonu zaznamenal hodnotu celkové radiační expozice, tzn. sumační hodnotu dávky záření v jednotkách mSv × cm2. Sumační hodnota se skládala ze všech skiagrafických zobrazení od zaměření operačního pole před začátkem operace, přes peroperační skiagrafování až po finální zobrazení při ukončení výkonu. Toto finální zobrazení je v materiální podobě součástí chorobopisu pacienta.
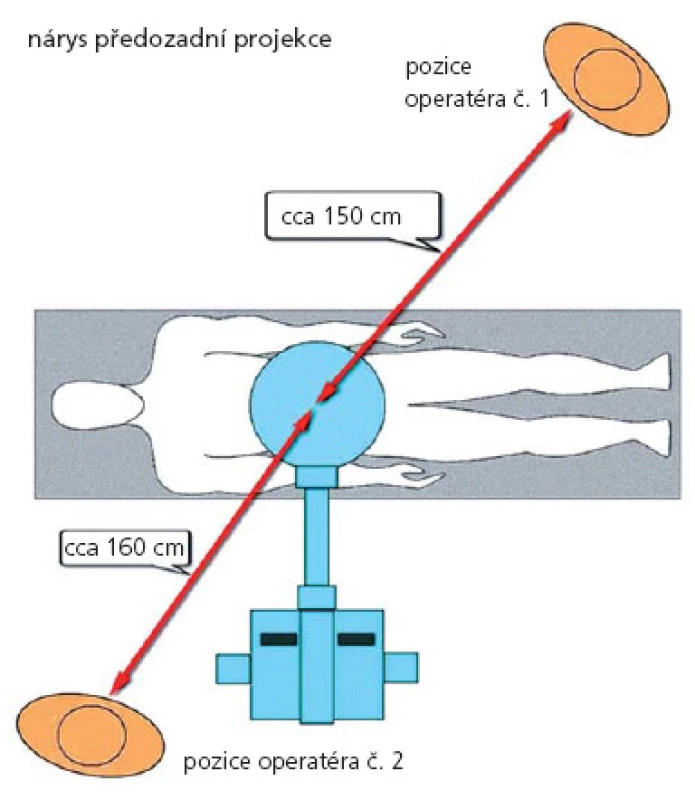
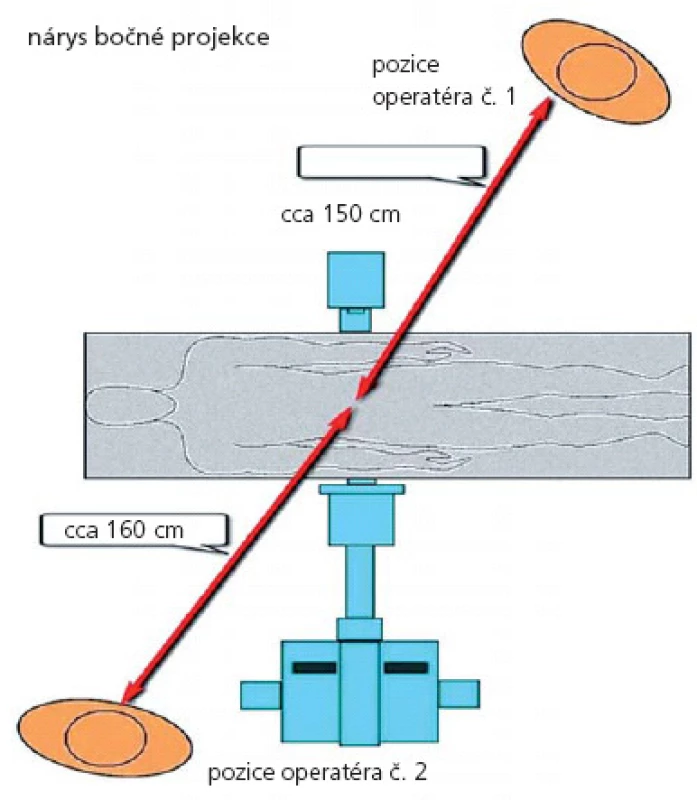
U 10 operačních výkonů (pět klasických otevřených a pět miniinvazivních) jsme hodnotili radiační zátěž operatéra, resp. asistenta, dávkou rozptýleného záření, které vzniká především odrazem primárního paprsku od těla pacienta. Během těchto výkonů byl přítomen specialista radiolog, jenž vždy z místa obvyklé pozice operatéra při jeho odstoupení od zářiče změřil speciálním měřicím přístrojem STEP OD 01 (STEP Sensortechnik und Elektronik Pockau GmbH) dávku rozptýleného záření. Operatér na daný okamžik tohoto měření poodstoupil cca 0,5 metru od své obvyklé pozice, kterou zaujal radiolog s měřičem. Přístroj STEP OD 01 je určený k měření dávkového ekvivalentu v rozsahu od 0– 2 000 µSv pomocí ionizační komory s objemem 600 cm3. Šířka měřeného energetického rozsahu se pohybuje v rozmezí od 6 keV do 15 MeV.
Měření proběhlo na mobilním sálovém RTG přístroji, C‑ rameno Philips BV 300 se zesilovačem o průměru 23 cm. Pro měření byl na skiaskopickém přístroji nastaven pulzní režim o frekvenci 1 pulz za sekundu. V tomto režimu pracoval skiaskopický přístroj u všech výkonů v našem souboru. Měřicí přístroj STEP OD 01 byl umístěn podle schématu na obr. 1 a 2.
Statistika
Data byla popsána popisnou statistikou (hodnoty radiační zátěže v mSv × cm2).
Průměrné sumační hodnoty radiační expozice u obou skupin pacientů jsme vzájemně statisticky srovnali. Ke statistickému zpracování byl použit software SPSS verze 15 s aplikací statistických testů Shapiro‑Wilk, Kruskal‑ Wallis a Mann‑Whitney. Dále těmito statistickými testy byly vyhodnoceny hodnoty dávek rozptýleného záření.
Autoři prohlašují, že studie na lidských subjektech popsaná v manuskriptu byla provedena v souladu s etickými standardy příslušné komise (institucionální a národní) odpovědné za provádění klinických studií a Helsinskou deklarací z roku 1975, revidovanou v roce 2000.
Výsledky
V prezentované studii byl prokázán statisticky významný rozdíl v operační radiační zátěži v neprospěch miniinvazivní transpedikulární fixace – Skupina 2 (ø 6,3 mSv × cm2), ve srovnání s otevřenou technikou transpedikulární fixace – Skupina 1 (ø 3,2 mSv × cm2). Výsledné hodnoty radiační expozice obou operačních technik jsou pro pacienty uvedeny v tab. 1.

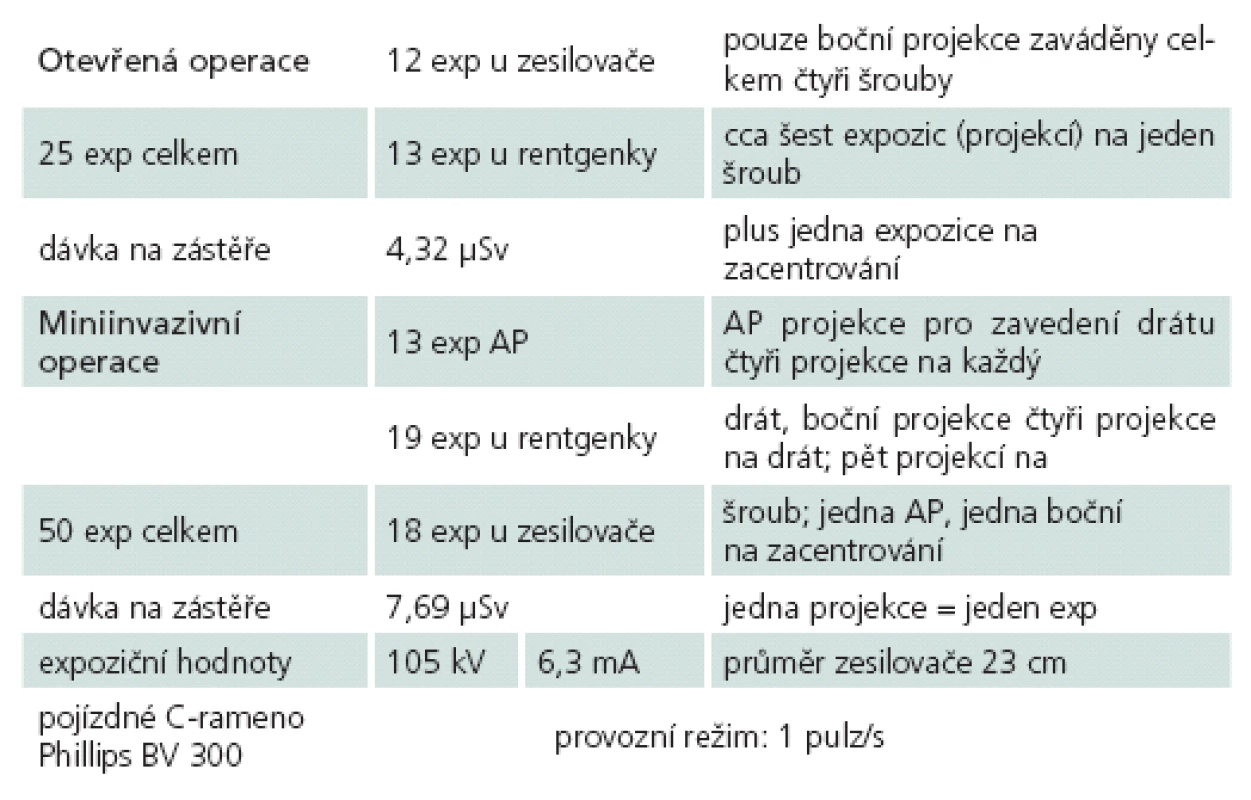
Měřením dávek rozptýleného záření byl potvrzen statisticky významný rozdíl v ozáření operatéra v neprospěch MISS. Tyto hodnoty při otevřené operaci byly o 30 % nižší než při operaci miniinvazivní. Naměřené hodnoty dávkového ekvivalentu jsou uvedeny v tab. 2.
U Skupiny 1 byla délka radiační expozice za celou operaci v rozmezí 23– 57 s, u Skupiny 2 v rozmezí 42– 89 s.
Diskuze
Dávka je definována jako poměr střední energie předané ionizujícím zářením látce o dané hmotnosti. Základní jednotkou absorbované dávky je Gray (Gy). Je pojmenována po Louisi Haroldu Grayovi. Je to energie 1 joule (J) absorbovaná v kilogramu látky. Sievert (Sv) je jednotka ekvivalentní dávky ionizujícího záření, případně dávkového ekvivalentu. Je pojmenována po Rolfu Maxmiliánovi Sievertovi, průkopníkovi radiační ochrany. Dávka 1 Sv jakéhokoli záření má stejné biologické účinky jako dávka 1 Gy rentgenového nebo gama záření. Jednotka vyjadřuje podíl množství absorbované energie v určité hmotnosti a v závislosti na daném druhu ionizujícího záření, tedy energie/ hmotnost (J × kg-1). Starší jednotkou ekvivalentní dávky/ dávkového ekvivalentu byl Rem, přičemž 1 Rem = 0,01 Sv, neboli 1 mSv = 100 mRem. Vzhledem k charakteru zářiče, ionizujícího záření a biologického materiálu lze v našem případě jednotky radiační dávky mGy a mSv používat ekvivalentně.
Mezinárodně používané limity radiačních dávek (podle NCRP, the National Council on Radiation Protection and Measurements) odpovídají českým normám. Povolená roční dávka pro celé tělo je 50 mSv, pro končetiny 500 mSv, pro kůži 500 mSv, pro oční čočky 150 mSv a pro všechny ostatní orgány 500 mSv. Při respektování těchto norem bylo vykalkulováno roční riziko mortality na následky vzniklých nádorových onemocnění s pravděpodobností 0,0017 % a riziko po 25leté expozici ve výši 0,04 % [4].
MISS technika má ve srovnání s otevřenou technikou jasnou výhodu ve výrazně menší ranné ploše, s tím související zanedbatelné peroperační krevní ztrátě, snadnějším procesem hojení s menším procentem ranných komplikací. S tím zároveň souvisí nižší stupeň a kratší trvání pooperační bolesti. Významným efektem MISS operací je zkrácení délky hospitalizace [5– 7]. Měli jsme případ pacienta, který byl první pooperační den na vlastní žádost propuštěn z hospitalizace ve výborném klinickém stavu. Nevýhodou MISS techniky je, že při použití peroperační skiaskopie během perkutánního zavádění šroubů se zvyšuje radiační expozice pacienta i operačního týmu ve srovnání s otevřenou technikou [8]. Navíc při zavádění K‑ drátu může teoreticky dojít i k poranění viscerálních nebo cévních struktur [9].
V této prezentované studii autoři prokázali statisticky významný rozdíl v operační radiační zátěži v neprospěch MISS oproti otevřené technice. I při tomto statisticky významném rozdílu se jedná o dávky záření u obou operačních technik relativně zanedbatelné, a tudíž větší radiační expozice pacienta není faktor ovlivňující indikaci, resp. kontraindikaci miniinvazivní perkutánní transpedikulární fixace. Navíc tato čísla představují jen potenciální stupeň ozáření operovaného pacienta. Jedná se o hodnoty vyjadřující vyzářenou dávku C-ramenem, avšak absorbovaná dávka tělem pacienta, zejména pak jeho jednotlivými orgány, je ve skutečnosti nižší.
V rámci legislativy České republiky žádná právní norma nestanovuje pro pacienta limity radiační expozice při peroperační skiaskopii k jakémukoliv konkrétnímu chirurgickému výkonu. Problematiku používání záření v lékařství řeší Vyhláška 307/ 2002 Sb. „O radiační ochraně“ ve znění Vyhlášky 499/ 2005 Sb. [10], z níž citujeme:
§60 Odůvodnění lékařského ozáření
- odst. 1: Lékařské ozáření jednotlivých osob se odůvodňuje očekávaným individuálním zdravotním prospěchem pacienta.
§ 62 Optimalizace radiační ochrany při lékařském ozáření
- odst. 1: Cílem optimalizace je:
- a) při radiodiagnostickém vyšetření správné použití zobrazovací metody tak, aby dávky ve tkáních byly co nejnižší, aniž by se tím omezilo získání nezbytných radiodiagnostických informací.
Z právní mluvy přeloženo tato vyhláška říká, že pokud to zdravotní stav pacienta vyžaduje a lékař ke svému diagnostickému či terapeutickému postupu ozářit pacienta potřebuje, pak není tento lékař omezen v četnosti použití a ve výši dávek radiačního záření. Lékař musí indikovat toto ozáření pacienta podle postupů lege artis. Každé další nadměrné či nadbytečné vystavení radiaci je kontraindikováno.
V dostupné literatuře se skupiny operatérů podrobily pokusům, při nichž se s pomocí dozimetrů měřilo ozáření rukou a těla během operací (tzv. real‑ time studie) [8,11– 14]. Tuohy et al prokázali během operace celkovou dávku ozáření těla pod ochrannou vestou pod 1 mRem, zevně od vesty 16 mRem a na rukou 6,3 mRem [14]. Singer et al naměřili na rukou expozici 20 mRem při průměrné délce záření 51 s, a roční limit by tak byl překročen až po 2 500 operacích [13]. Podle literatury zabere zavádění šroubů otevřenou technikou 3,4– 66 s skiaskopie na jeden šroub, tedy během celé jednosegmentové operace 13,6– 264 s [15– 17]. Perkutánní zavádění šroubů při TLIF operaci technikou „single shot“ (spot fluoroscopy) znamenalo expozici přibližně 100 s na celou operaci s průměrnou expozicí 76 mRem pro ruce a 27 mRem pro tělo pod zástěrou. V tomto případě to znamená dávku umožňující 194 stejných expozicí během jednoho roku, aniž jsou překročeny hygienické limity [8]. Jiní autoři udávají během perkutánní kyfoplastiky delší expozice, v délce přibližně 230 s [18] nebo dokonce 340 s [19]. V jiné studii radiační expozice chirurga u vertebroplastik (32 operací během tří měsíců) představovala roční riziko fatálního nádorového onemocnění 0,0025 % a roční morbidity bez fatálních následků 0,025 %. Průměrná dávka pro celé tělo chirurga při jedné operaci byla v tomto případě 1,44 mSv a pro ruce 2,04 mSv. Dávka pro oční čočky představovala přibližně 8 % hodnoty uznané pro indukci katarakty a dávka pro kůži rukou dosáhla 10 % limitu [20].
Tyto hodnoty jsou z pohledu radiační zátěže spondylochirurga v podmínkách našeho způsobu operování irelevantní i vzhledem k používání ochranných pomůcek a zvláště pak důslednému dodržování minimální vzdálenosti personálu 1,5 metru od zářiče C‑ ramene při každém snímkování, kde jsou hodnoty radiace velmi nízké. Toto tvrzení můžeme deklarovat opakovaným naměřením nulových hodnot expozičních dávek na našich osobních dozimetrech během pravidelných kontrol a zejména výsledky (tab. 2) měření rozptýleného záření přístrojem STEP OD 01. Z tohoto měření vyplývá, že při dodržení všech zásad radiační ochrany během operační skiaskopie by jeden operatér mohl provést 4 630 operací za jeden rok otevřeným způsobem (17 za jeden den) a 2 600 operací za jeden rok miniinvazivně (10 za jeden den), aniž by byly překročeny stanovené limity ozáření radiačních pracovníků kategorie A(20 mSv/ rok). Je třeba vzít v úvahu, že změřené dávkové ekvivalenty a vypočtené počty operací vychází z hodnot dávkových ekvivalentů měřených na stínící ochranné zástěře. Podle ekvivalentu tloušťky olověné stínící vrstvy používaných zástěr lze hodnoty dále upravovat (např. 0,5 mm Pb ekvivalentní zástěra snižuje dávkový ekvivalent pod zástěrou 8- až 10krát).
O významu používání ochranných prostředků pro ochranu chirurga referovali Synowitz s Kiwitem v případě přímé expozice rukou během operace o 75 % menší radiační zátěž při použití ochranných rukavic [21]. Choi prokázal, že také pozice C‑ ramene ovlivní významně dávku radiace. Pokud je zářič na kontralaterální straně chirurga a pod operačním stolem, pak je expozice operatéra potenciálně 2,7– 10krát nižší než při opačné pozici [22]. Použití mini C‑ ramene ve srovnání s klasickým C‑ ramenem taktéž sníží radiační expozici [12,13].
Cílem snahy operačního týmu je tedy snížit peroperační radiační zátěž pro pacienta i personál. Faktory ovlivňující radiační zátěž lze schematicky rozdělit na neovlivnitelné a ovlivnitelné. Neovlivnitelné faktory vycházejí ze strany pacienta a jsou dány individualitou jeho tělesné konstituce, operační diagnózou a s tím souvisejícím typem indikované operace a lokalizací operované etáže páteře. Faktory ovlivnitelné jsou dány rozhodnutím lékaře o způsobu operace (při TPF otevřeně nebo MISS technikou) či operačním postupem („single shot“ namísto kontinuální skiaskopie, zaměření více pediklů namísto jednoho na jeden snímek). Dalším takovým faktorem je i zkušenost operatéra a spolupráce radiologického asistenta.
Závěr
- Autoři prokázali statisticky významný rozdíl v operační radiační zátěži v neprospěch miniinvazivní transpedikulární fixace.
- I při tomto rozdílu se jedná o dávky záření naprosto minimální, a tudíž větší radiační expozice pacienta není faktor ovlivňující indikaci miniinvazivní perkutánní transpedikulární fixace. Není žádný racionální důvod pro rozhodování se mezi otevřeným a perkutánním výkonem na základě expozice záření.
- Při dodržení veškerých zásad ochrany proti záření – ochranné pomůcky, kvalitně odstíněný skiaskopický přístroj, vyhýbání se poli chodu paprsků při expozici, technika „single shot“ – je ozáření operačního týmu zanedbatelné a nepřesáhne hygienické normy ani při velké frekvenci operací.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Tomáš Wanek
Neurochirurgická klinika
LF UP a FN Olomouc
I. P. Pavlova 6
Olomouc
e-mail: tomas.wanek@email.cz
Přijato k recenzi: 7. 2. 2013
Přijato do tisku: 15. 4. 2013
Zdroje
1. Mastrangelo G, Fedeli U, Fadda E, Giovanazzi A, Scoizzato L, Saia B. Increased cancer risk among surgeons in an orthopaedic hospital. Occup Med 2005; 55(6): 498– 500.
2. Hrabálek L. Komplexní léčba symptomatických obratlových hemangiomů. Acta Chir Orthop Traum Cech 2010; 77(2): 149– 153.
3. Hrabálek L, Rešková I, Bučil J, Vaverka M, Houdek M.Použití titanových a PEEKových implantátů při ALIF stand‑ alone u degenerativního onemocnění lumbosakrální páteře – prospektivní studie. Cesk Slov Neurol N 2009; 72/ 105(1): 38– 44.
4. International Commission on Radiological Protection: Development of the draft 2005 Recommendations of the International Commission on Radiological Protection. Ann ICRP 2004; 34: S1– S44.
5. Hrabálek L, Bučil J, Vaverka M, Houdek M. Poraněný thorakolumbální disk – indikace k náhradě předním přístupem podle magnetické rezonance. Cesk Slov Neurol N 2010; 73/ 106(3): 238– 244.
6. Park Y, Ha JW. Comparison of one‑ level posterior lumbar interbody fusion performed with a minimallyinvasive approach or a traditional open approach. Spine 2007; 32(5): 537– 543.
7. Scheufler KM, Dohmen H, Vougioukas VI. Percutaneous transforaminal lumbar interbody fusion for the treatment of degenerative lumbar instability. Neurosurgery 2007; 60 (4 Suppl 2): 203– 212.
8. Bindal RK, Glaze S, Ognoskie M, Tunner V, Malone R, Ghosh S et al. Surgeon and patient radiation exposure in minimally invasive transforaminal lumbar interbody fusion. J Neurosurg Spine 2008; 9(6): 570– 573.
9. Heini P, Schöll E, Wyler D, Eggli S. Fatal cardiac tamponade associated with posterior spinal instrumentation. A case report. Spine 1998; 23(20): 2226– 2230.
10. Vyhláška 307/ 2002 Sb. Státního úřadu pro jadernou bezpečnost ze dne 13. června 2002 O radiační ochraně. Změna: 499/ 2005 Sb.
11. Rampersaud YR, Foley KT, Shen AC, Williams S, Solomito M. Radiation exposure to the spine surgeon during fluoroscopically assisted pedicle screw insertion. Spine 2000; 25(20): 2637– 2645.
12. Shoaib A, Rethnam U, Bansal R, De A, Makwana N.A comparison of radiation exposure with the conventional versus mini C‑ arm in orthopedic extremity surgery. Foot Ankle Int 2008; 29: 58– 61.
13. Singer G. Radiation exposure to the hands from mini C‑ arm fluoroscopy. J Hand Surg Am 2005; 30(4): 795– 797.
14. Tuohy CJ, Weikert DR, Watson JT, Lee DH. Hand and body radiation exposure with the use of mini C‑ arm fluoroscopy. J Hand Surg Am 2011; 36(4): 632– 638.
15. Perisinakis K, Theocharopoulos N, Damilakis J, Katonis P, Papadokostakis G, Hadjipavlou A et al. Estimation of patient dose and associated radiogenic risks from fluoroscopically guided pedicle screw insertion. Spine 2004; 29(14): 1555– 1560.
16. Sagi HC, Manos R, Benz R, Ordway NR, Connolly PJ. Electromagnetic field‑based image‑ guided spine surgery, part one; results of a cadaveric study evaluating lumbar pedicle screw placement. Spine 2003; 28(17): 2013– 2018.
17. Slomczykowski M, Roberto M, Schneeberger P, Ozdoba C, Vock P. Radiation dose for pedicle screw insertion. Fluoroscopic method versus computer‑ assisted surgery. Spine 1999; 24(10): 975– 982.
18. Boszczyk BM, Bierschneider M, Panzer S, Panzer W, Harstall R, Schmid K et al. Fluoroscopic radiation exposure of the kyphoplasty patient. Eur Spine J2006; 15(3): 347– 355.
19. Mroz TE, Yamashita T, Davros WJ, Lieberman IH. Radiation exposure to the surgeon and the patient during kyphoplasty. J Spinal Disord Tech 2008; 21(2): 96– 100.
20. Harstall R, Heini PF, Mini RL, Orler R. Radiation exposure to the surgeon during fluoroscopically assisted percutaneous vertebroplasty. Spine 2005; 30(16): 1893– 1898.
21. Synowitz M, Kiwit J. Surgeon’s radiation exposure during percutaneous vertebroplasty. J Neurosurg Spine 2006, 4(2): 106– 109.
22. Choi HC. Fluoroscopic radiation exposure during percutaneous kyphoplasty. J Korean Neurosurg Soc 2011; 49: 37– 42.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2013 Číslo 5
Nejčtenější v tomto čísle
- Wilsonova nemoc
- Multiformní glioblastom – přehled nových poznatků o patogenezi, biomarkerech a perspektivách léčby
- Tumoriformní varianta roztroušené sklerózy – dvě kazuistiky
- Test 3F Dysartrický profil – normativní hodnoty řeči v češtině
