Validace dotazníku pro hodnocení dysfagie u pacientů s roztroušenou sklerózou – česká verze DYMUS
Validation of DYsphagia in MUltiple Sclerosis questionnaire – Czech version of DYMUS
Aim: Swallowing problems are a relatively common and severe symptom of multiple sclerosis (MS), but dysphagia is often neglected and probably underestimated in clinical practice. The cause may be due to lacking a valid screening tool for evaluation in Czech for the risk of dysphagia in MS patients. The aim of our study was to create and validate the Czech version of the DYsphagia in MUltiple Sclerosis (DYMUS) questionnaire. It is a simple anamnestic tool consisting of 10 questions, where scores of 2 or more represent a positive screening for risk of dysphagia.
Materials and methods: The Czech version of the DYMUS questionnaire was created by the forward-backward translation method and validated on 48 MS patients and 33 healthy volunteers. The questionnaire was administered repeatedly 3–5 days apart to evaluate repeatability and reproducibility. The risk of dysphagia was reviewed using a screening 100- ml Water Swallowing test.
Results: DYMUS scores in healthy controls were between 0 and 2 (median 0). In MS patients, the values were significantly higher (P < 0.001) and ranged from 0 to 10 (median 1). An abnormal DYMUS score correlating with dysphagia (≥ 2) was demonstrated in 16 patients (33%), but only in one healthy subject (3%) (P < 0.001). Data correlated with expert testing (r = 0.66; P = 0.01) and reviewed screening testing (r = 0.49; P = 0.01). The repeatability evaluated by the Spearman correlation was 0.94 (P < 0.001), and the Cronbach alpha value reflecting reproducibility reached 0.954 demonstrating high internal consistency of the questionnaire.
Conclusion: The Czech version of the DYMUS questionnaire showed very good validity, reproducibility and internal consistency of testing in the screening of dysphagia in MS patients.
Keywords:
Multiple sclerosis – questionnaire – dysphagia – validation
Authors:
J. Kolčava 1,2; N. Lasotová 2
; P. Štourač 1,2; J. Bednařík 1,2; E. Vlčková 1,2
Authors‘ workplace:
Neuroglická klinika LF MU, Brno
1; Neurologická klinika FN Brno
2
Published in:
Cesk Slov Neurol N 2020; 83/116(3): 285-290
Category:
Original Paper
doi:
https://doi.org/10.14735/amcsnn2020285
Overview
Cíl: Potíže s polykáním jsou relativně častým a závažným symptomem RS, který je však v klinické praxi často opomíjen a zřejmě podhodnocen. Příčinou může být mimo jiné absence validního skríningového nástroje pro hodnocení rizika dysfagie u pacientů s RS v českém jazykovém prostředí. Cílem naší studie bylo proto vytvořit a validovat českou verzi dotazníku DYsphagia in MUltiple Sclerosis (DYMUS). Jedná se o jednoduchý anamnestický nástroj sestávající z 10 otázek, skóre 2 a více svědčí pro riziko dysfagie.
Materiál a metodika: Česká verze dotazníku DYMUS byla vytvořena metodou zpětného překladu a validována na souborech 48 pacientů s RS a 33 zdravých dobrovolníků. Dotazník byl administrován opakovaně s odstupem 3–5 dní za účelem hodnocení opakovatelnosti a reprodukovatelnosti. Riziko dysfagie bylo kontrolně hodnoceno pomocí skríningového 100ml Water Swallowing testu.
Výsledky: Skóre DYMUS dosáhlo u zdravých kontrol hodnot v rozmezí 0–2 (medián 0). U pacientů s RS byly hodnoty významně vyšší (p < 0,001) a pohybovaly se v rozmezí 0–10 (medián 1). Abnormální výsledek skóre DYMUS korelující s rizikem dysfagie (≥ 2) byl prokázán u 16 pacientů (33 %), ale pouze u jednoho zdravého subjektu (3 %) (p < 0,001). Data jsou v korelaci s expertním hodnocením (r = 0,66; p = 0,01) i kontrolním skríningovým testem (r = 0,49; p = 0,01). Opakovatelnost hodnocená pomocí Spearmanovy korelace má hodnotu 0,94 (p < 0,001). Hodnota Cronbachova alfa odrážející reprodukovatelnost dosáhla 0,954, což prokazuje vysokou vnitřní konzistenci dotazníku.
Závěr: Česká verze dotazníku DYMUS prokázala velmi dobrou validitu, reprodukovatelnost a vnitřní konzistenci testování ve skríningu dysfagie u pacientů s RS.
Klíčová slova:
roztroušená skleróza – dysfagie – dotazník – validace
Úvod
Roztroušená skleróza je chronické demyelinizační onemocnění CNS. K častým a závažným klinickým projevům RS patří mimo jiné potíže s polykáním (dysfagie). Výskyt tohoto příznaku v populaci pacientů s RS mezi publikovanými studiemi kolísá v širokém rozmezí 10–90 %, zejména v závislosti na diagnostické metodě použité k jejímu průkazu [1–5]. Podle nejpravděpodobnějších odhadů se výskyt dysfagie pohybuje kolem třetiny pacientů s RS [2,3,5] a signifikantně narůstá s dysabilitou hodnocenou pomocí Expanded Dis-ability Status Scale (EDSS) [1,3,6,7] a délkou trvání onemocnění [1,3].
Potíže s polykáním se však překvapivě vyskytují také u 17 % pacientů s EDSS nižším než 2,5 [8,9]. Dysfagie byla zjištěna u 11,1 % soběstačných pacientů a 48 % pacientů nesoběstačných [1]. Příčinou rozvoje dysfagie u pacientů s RS je komplexní postižení senzomotorického komplexu odpovědného za kontrolu polykacího aktu. Dysfunkce tohoto komplexu může být podmíněna lézí mozečku, kortikobulbárního traktu či hlavových nervů. Nejčastěji jde o kombinaci postižení více zmíněných systémů [2,10].
Potíže s polykáním mohou způsobit závažné komplikace jako aspirační pneumonie. Pacienti s RS mají téměř 5× častěji diagnostikovanou pneumonii než běžná populace [11]. Výskyt dysfagie zvyšuje také riziko dehydratace a malnutrice a snižuje kvalitu života pacientů v důsledku sociálního vyloučení, ztráty soběstačnosti a sníženého sebevědomí [1,12–15]. Zmíněné komplikace dysfagie jsou častou příčinou úmrtí pacientů s RS s těžším postižením [15].
Testování a efektivní skríning polykacích potíží jsou proto důležitými prvky péče o pacienty s RS, protože včasné odhalení a management dysfagie mohou být prevencí závažných následků poruch polykání [10]. Rehabilitace dysfagie bývá v řadě případů úspěšná [1]. K časnému rozpoznání dysfagie obecně bylo v posledních letech vyvinuto několik cílených dotazníků [12,16].
Dotazník DYsphagia in MUltiple Sclerosis (DYMUS) [17] byl jako jediný vyvinut cíleně pro hodnocení polykacích potíží u pacientů s RS. Skládá se z 10 otázek, na které pacient odpovídá ano či ne. Kladná odpověď je hodnocena jedním bodem, záporná nula body. Celkové skóre je tedy 0–10 bodů a lze je ještě rozdělit na dílčí škály reflektující polykání pevné stravy a tekutin. Dle původní práce provedené pouze na souboru pacientů s RS (bez kontrolní skupiny zdravých dobrovolníků) byla již jedna pozitivní odpověď považována za pozitivní skríning dysfagie. Tři a více pozitivních odpovědí byly považovány za korelát vysoce pravděpodobné závažné (alarmující) dysfagie [17]. V pozdějších validačních studiích byla normativní data rozšířena o další skupiny pacientů s RS i soubory zdravých dobrovolníků a bylo navrženo přehodnocení výsledků dotazníku, přičemž až skóre 2 či více značí patologický výsledek dotazníku DYMUS korelující s dysfagií [18]. Výskyt dysfagie u pacientů s RS hodnocený pomocí dotazníku DYMUS se v publikovaných studiích pohybuje v rozmezí 31–58 % [4,5,8,18,19]. Mezi hlavní výhody dotazníku patří jednoduchost, bezpečnost a nízká nákladovost, které umožňují použít tento dotazník pro širokou skupinu pacientů, ale také časová nenáročnost pro personál. Dotazník nemusí být administrován specialistou (otorinolaryngologem či logopedem).
Cílem naší studie bylo vytvořit a validovat českou verzi dotazníku DYMUS pro potřeby české populace, protože validovaný dotazník pro hodnocení dysfagie u pacientů s RS dosud v českém jazykovém prostředí chybí.
Materiál a metodika
První fází této prospektivní validační studie bylo vytvoření české jazykové verze dotazníku DYMUS metodou zpětného překladu (forward-backward translation) s pomocí profesionálního překladatele a rodilého mluvčího dle publikovaných doporučení [20,21]. Česká i originální anglická verze jsou uvedeny v tab. 1 a 2.
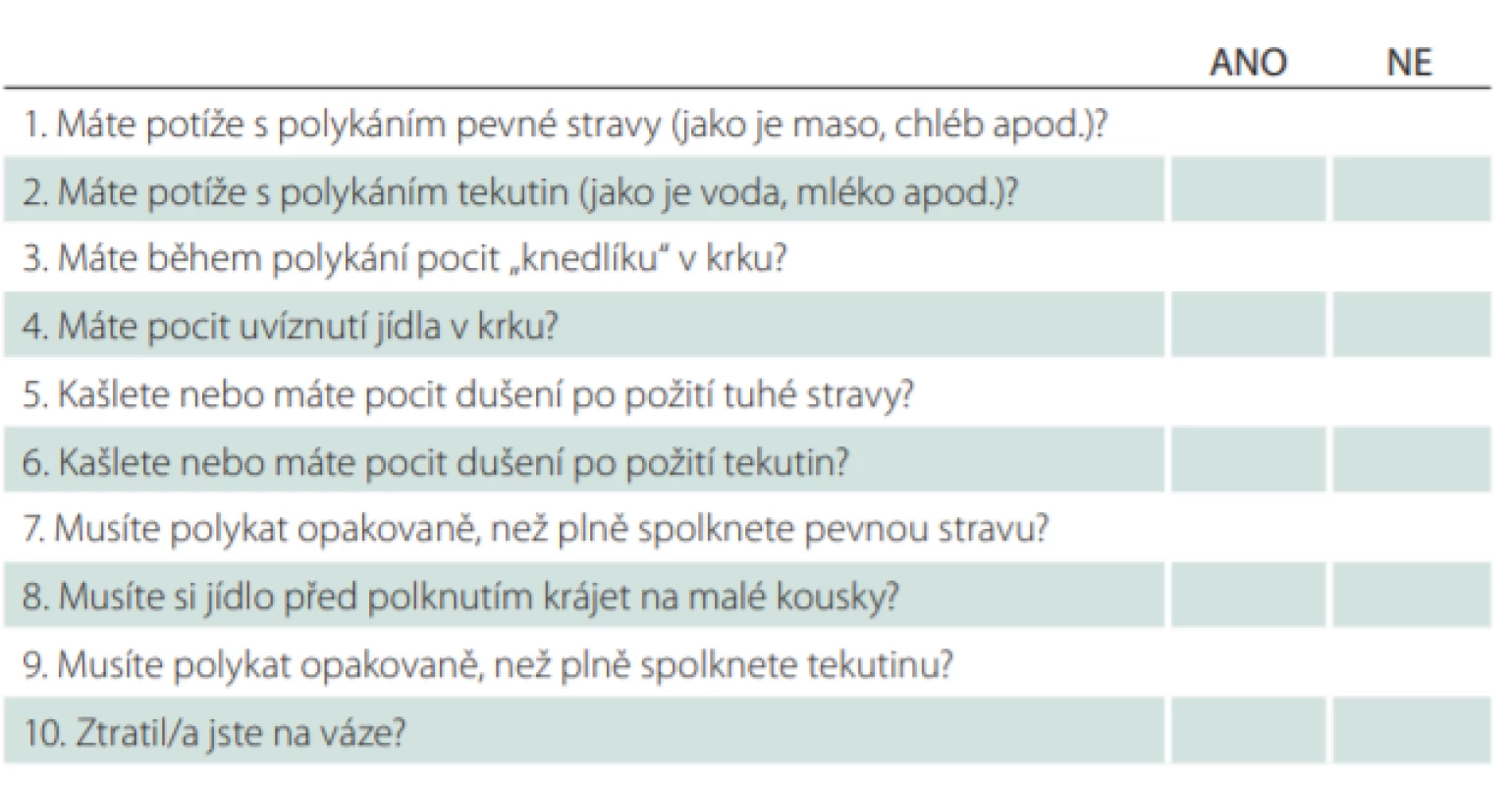
![Dotazník DYMUS – původní verze [17].](https://www.csnn.eu/media/cache/resolve/media_object_image_small/media/image_pdf/6d8027d0aeb86b4202ab77837ebda857.png)
Na každou položku dotazníku odpovídá pacient ano (1 bod) nebo ne (0 bodů). Celkové skóre může tedy dosahovat hodnot v rozmezí 0–10. Za pacienty se suspektní dysfagií jsou označeni pacienti s pozitivní odpovědí na 2 či více otázek [18].
Dotazník lze dále rozdělit na 2 dílčí škály, reflektující dysfagii pro tekutou stravu (otázky číslo 2, 6 a 9) a dysfagii pro stravu pevnou (otázky číslo 1, 3, 4, 5, 7, 8 a 10).
Česká verze dotazníku DYMUS byla následně administrována dvěma skupinám jedinců:
- 33 asymptomatickým dobrovolníkům (průměrný věk byl 40,3 let ± 11,7 let, 23 žen). Dobrovolníci nesměli mít známé neurologické onemocnění či onemocnění v oblasti hlavy a krku, které by mohlo způsobovat dysfagii, a měli normální nález při orientačním klinickém neurologickém a logopedickém vyšetření;
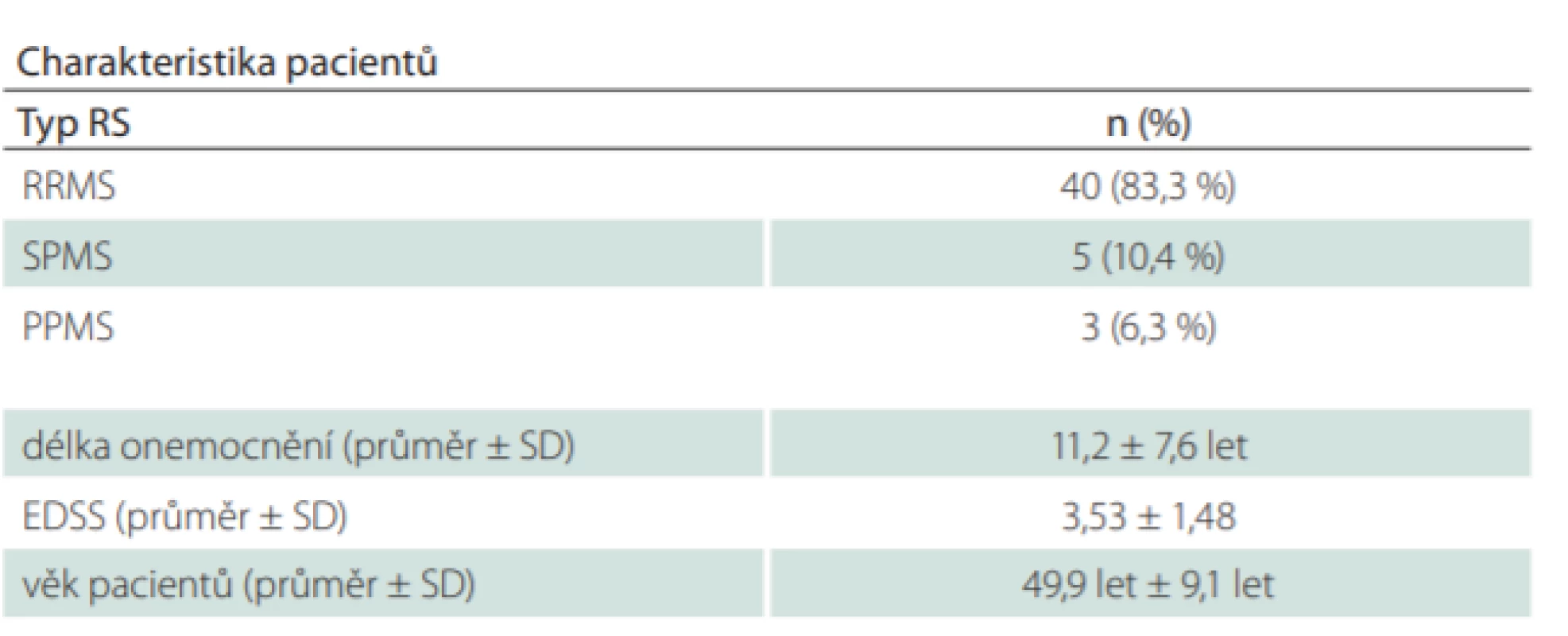
- 48 pacientům s RS sledovaným v RS centru FN Brno. Všichni pacienti splňovali diagnostická McDonaldova kritéria 2017 [22]. Vylučujícím kritériem pro účast v tomto projektu byly výskyt komorbidních neurologických nebo otorinolaryngologických onemocnění s potenciálním vlivem na polykací funkce (např. CMP, kraniotraumata či tumory v oblasti hlavy a krku) a/nebo relaps onemocnění za poslední 3 měsíce. Celkem bylo do studie zařazeno 7 mužů (15 %) a 41 žen (85 %), průměrný věk 49,9 let ± 9,1 let, průměrná doba trvání základního onemocnění byla 11,2 ± 7,6 let. Čtyřicet pacientů mělo relabující-remitující formu RS (83 %), pět pacientů sekundárně progresivní formu (10 %) a tři pacienti primárně progresivní formu (6 %) (tab. 3). Průměrné EDSS bylo 3,53 ± 1,48 (tab. 3). Testování proběhlo u těchto pacientů během rutinních kontrol.
Všichni pacienti a kontroly prodělali při vstupu do studie klinické neurologické vyšetření a expertní logopedické vyšetření (v rámci kterého byli klinicky dotazováni na potíže s polykáním). U zdravých kontrol byl normální výsledek obou vyšetření (nesvědčící pro dysfagii ani onemocnění, které by k ní mohlo vést) podmínkou pro zařazení do studie. U pacientů byly další testy provedeny bez ohledu na výsledek těchto vyšetření a poté absolvovali skríningový test polykacích funkcí (100- ml Water Swallowing Test) [23]. Následně bylo u pacientů i zdravých dobrovolníků provedeno testování pomocí dotazníku DYMUS. Po ukončení administrace dotazníku byli pacienti i kontroly dotazováni na jehosrozumitelnost.
K vyhodnocení opakovatelnosti a reprodukovatelnosti dotazníku DYMUS v českém jazyce bylo použito opakované testování (test-retest). Pacienti i zdravé kontroly byli po 3–5 dnech telefonicky kontaktováni a v rámci tohoto telefonického rozhovoru jim byl s jejich souhlasem znovu administrován dotazník DYMUS, přičemž neměli přístup k dříve vyplněnému dotazníku [24]. Opakovatelnost a reprodukovatelnost byla ověřena na vzorcích 48 pacientů s RS a 33 zdravých kontrol.
Statistická analýza
Data byla statisticky zpracována pomocí programu SPSS verze 25 (IBM, Armonk, NY, USA). Pro popis rozložení hodnot v jednotlivých souborech byla použita robustní sumární statistika (medián, rozsah, kvantily). Pro non-normální distribuci hodnot dotazníku DYMUS byly ke statistické analýze používány primárně neparametrické testy. Rozdíly hodnot skóre DYMUS mezi jednotlivými skupinami či podskupinami pacientů/zdravých dobrovolníků byly hodnoceny pomocí Mann-Whitneyho testu. Spolehlivost, validita a vnitřní konzistence dotazníku byly testovány pomocí koeficientu Cronbachova alfa a Spearmanovy korelace. Srovnání kategoriálních dat (pohlaví, počet abnormit DYMUS v jednotlivých skupinách/podskupinách pacientů) bylo provedeno pomocí chí-kvadrát testu. Demografické a klinické charakteristiky, které vykazují normální distribuci dat (věk, EDSS, délka trvání onemocnění), byly srovnány t-testem.
Výsledky
Vytvoření české verze dotazníku DYMUS prokázalo vynikající shodu mezi originální a zpětně přeloženou verzí a v rámci zpětného překladu nebyl zaznamenán žádný konfliktní či problematický termín.
Pacienti s RS i dobrovolníci neměli v rámci vstupní administrace potíže s porozuměním otázkám a byli schopni dotazník vyplnit do 2 minut.
Skóre DYMUS dosáhlo u zdravých kontrol hodnot v rozmezí 0–2 (medián 0) (tab. 4). U pacientů s RS byly hodnoty významně vyšší (Man-Whitneyho test; p < 0,001) a pohybovaly se v rozmezí 0–10 (medián 1). Abnormální výsledek skóre DYMUS korelující s dysfagií (≥ 2) byl prokázán u 16 pacientů s RS (33 %), ale pouze u jednoho zdravého subjektu (3 %) (chí-kvadrát test; p < 0,001).
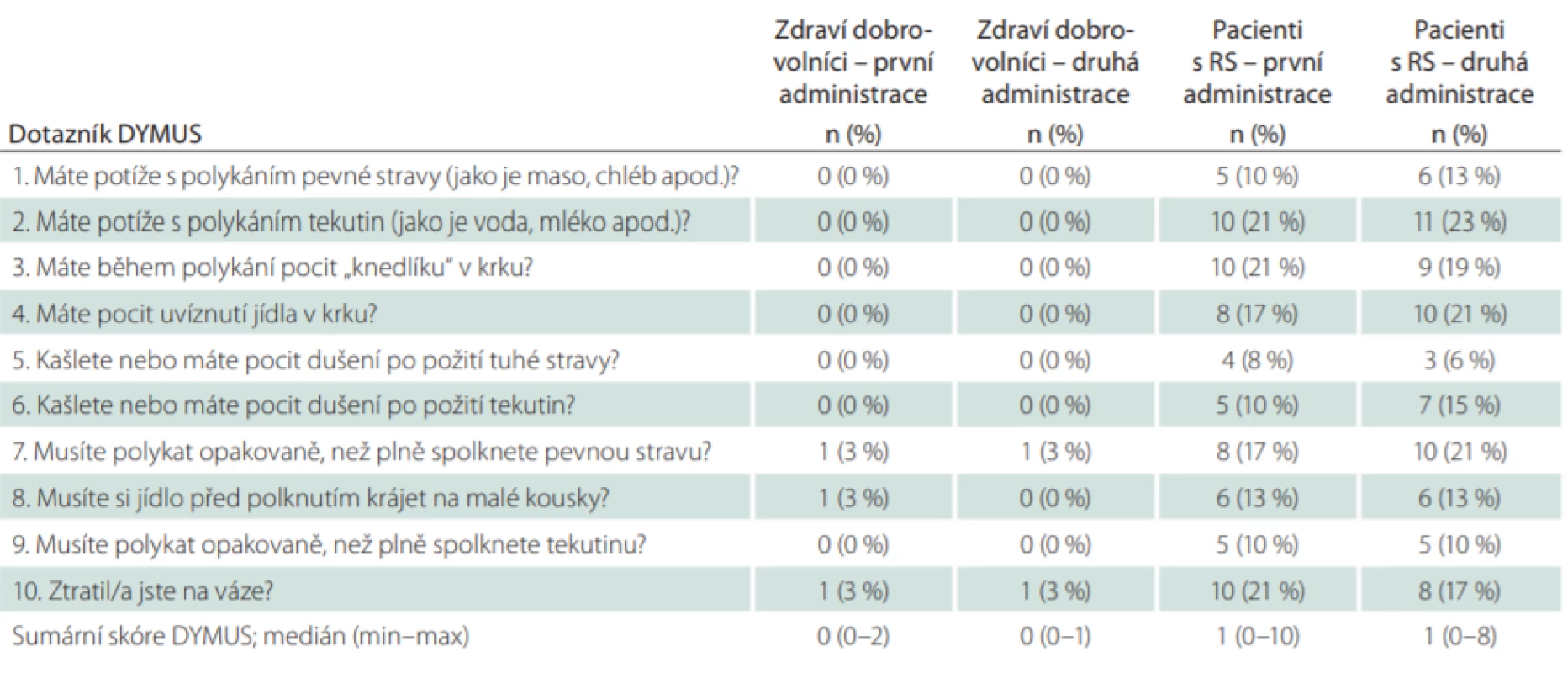
Celkem 24 pacientů (50 %) udávalo při vstupní administraci dotazníku potíže s polykáním tuhé stravy (otázky číslo 1, 3, 4, 5, 7, 8 a 10), 13 pacientů (27 %) pak potíže s polykáním stravy tekuté (otázky číslo 2, 6 a 9) a 8 pacientů (17 %) potíže s oběma konzistencemi (tab. 4).
Zjistili jsme také signifikantní korelaci (Spearmanův korelační koeficient; r = 0,49; p = 0,01) dotazníku se skríningovým testem (100- ml Water Swallowing test), který byl v normě u všech zdravých dobrovolníků, oproti tomu byl patologický u 15 pacientů (31 %).
Pacienti, kteří byli expertním hodnocením posouzeni jako pacienti s dysfagií (23 %), měli signifikantně vyšší skóre v dotazníku DYMUS (Man-Whitneyho test; p = 0,01) (medián 4; rozmezí 1–10, u pacientů s dysfagií podle expertního hodnocení vs. medián 0; rozmezí 0–3, u pacientů bez expertně hodnocené dysfagie).
Ve skupině pacientů s RS byla zjištěna signifikantní pozitivní korelace dotazníku DYMUS s EDSS (r = 0,83; p = 0,03) (Spearmanův korelační koeficient v tomto případě i všech dalších případech korelací v tomto odstavci) a trváním onemocnění (r = 0,84; p = 0,03) (vstupní hodnoty obou těchto klinických parametrů jsou uvedeny v tab. 3). Naopak korelace sumárního skóre dotazníku DYMUS s věkem zdravých dobrovolníků (r = 0,21; p = 0,7) i pacientů s RS (r = 0,29; p = 0,08) nebyla statisticky významná. Prokázán nebyl ani statisticky významný rozdíl skóre DYMUS mezi muži a ženami, a to ve skupině pacientů s RS (Mann-Whitneyho test; p = 0,56) (muži: rozmezí 0–2, medián 0; ženy: rozmezí 0–10, medián 1) ani mezi zdravými dobrovolníky (Mann-Whitneyho test; p = 0,21) (muži: všechny hodnoty 0; ženy: rozmezí 0–2; medián 0).
Opakovatelnost testu mezi vstupní a kontrolní administrací (tab. 4) hodnocená pomocí Spearmanovy korelace dosáhla při souhrnném hodnocení všech subjektů vynikající hodnoty r = 0,94 (p < 0,001). Opakovatelnost byla poněkud lepší ve skupině zdravých dobrovolníků (r = 0,96; p < 0,001) než v souboru pacientů s RS (r = 0,923; p < 0,01), i když z praktického hlediska jsou tyto rozdíly minimální. Hodnota Cronbachova alfa (reflektující reliabilitu neboli spolehlivost testu) dosáhla při souhrnném hodnocení všech zařazených jedinců úrovně 0,954, což prokazuje celkově vysokou vnitřní konzistenci dotazníku. Reliabilita se mezi oběma testovanými soubory významně nelišila (dosáhla hodnoty 0,916 ve skupině pacientů s RS a 0,921 u zdravých dobrovolníků).
Diskuze
Prezentovaná práce umožnila vytvoření české verze dotazníku DYMUS a prokázala, že představuje jednoduchý a efektivní nástroj ke zhodnocení rizika dysfagie u pacientů s RS. Potvrdila také časově nenáročnou administraci dotazníku a jeho snadné použití pro pacienty i personál, což jsou zjištění, která korelují s předchozími pracemi [4,18]. Naše data prokazují i výbornou opakovatelnost české verze dotazníku, a tedy jeho spolehlivost při vícenásobném použití, např. v rámci longitudinálního sledování pacientů nebo při hodnocení terapeutických intervencí zaměřených na rehabilitaci dysfagie.
Administrace dotazníku byla v naší studii ve všech případech bezproblémová, a to dokonce i při jeho použití v rámci telefonického kontaktu s pacientem. Pacienti neměli problém s porozuměním žádné z otázek. V předcházejících studiích byla vyslovena hypotéza, že otázka číslo 10 („Ztratil/a jste na váze?“) není příliš nespecifická pro dysfagii. Pro tuto otázku byla navíc v některých publikovaných pracích nalezena jistá nekonzistence při validačních studiích, což jejich autoři reflektují vytvořením modifikovaného dotazníku DYMUS o devíti položkách při vynechání otázky číslo 10 [18,25]. Snížení chuti k jídlu obecně je skutečně méně specifickým příznakem a objevuje se u pacientů s RS také v důsledku snížené mobility, únavy, deprese nebo může být nežádoucím účinkem léků [7,21]. Ztráta na váze je však naproti tomu považována za jeden ze závažných až alarmujících příznaků dysfagie a ověření jejího výskytu při podezření na dysfagii řada autorů doporučuje [26]. V naší studii se jednalo o jednu z nejsenzitivnějších položek: podobně jako u otázek 2 a 3 („Máte potíže s polykáním tekutin jako je voda, mléko apod.?“ a „Máte během polykání pocit „knedlíku“ v krku?“) jsme pozitivní odpověď na otázku 10 prokázali při první administraci u nejvyššího počtu pacientů (21 %). Tato otázka vykazovala také dobrou korelaci s kontrolním hodnocením dysfagie (expertním či skríningovým pomocí 100- ml Water Swallowing testu), což potvrzuje její úzký vztah k polykacím obtížím. Autorům práce se proto jeví racionální použití plné verze dotazníku zahrnující i otázku č. 10.
Prevalence suspektní dysfagie prokázaná pomocí dotazníku DYMUS byla v naší kohortě 33 %, což je výskyt srovnatelný s předchozími studiemi. Tato shoda zpětně svědčí pro srovnatelnou validitu české verze DYMUS s jinými jazykovými verzemi tohoto skríningového nástroje. Výskyt suspektní dysfagie u třetiny hodnocených pacientů současně poukazuje na skutečnost, že jde o vcelku častý symptom RS, který by měl být u pacientů monitorován a v případě průkazu postižení řešen. Potvrdili jsme také dříve prokázanou pozitivní korelaci mezi dysfagií a výší EDSS a také délkou trvání onemocnění [4,5,8,17–19,27].
Skríningové hodnocení dysfagie pomocí 100- ml Water Swallowing testu i expertní hodnocení bylo v naší studii v korelaci s výskytem suspektní dysfagie potvrzeným dotazníkem DYMUS [23]. Tato data podporují skutečnost, že dotazník reflektuje vhodným způsobem polykací obtíže a v běžné ambulantní klinické praxi může orientačně nahradit obtížněji dostupné expertní vyšetření.
Samotná otázka „Máte nějaké potíže s polykáním?“ je totiž pro validní hodnocení výskytu dysfagie nedostatečná a je nezbytné se pacientů přímo ptát na další specifické potíže, které jsou s výskytem dysfagie často spojeny, resp. jsou jejím příznakem (např. výše zmiňovaná ztráta hmotnosti, pocit uvíznutí jídla v hrdle či knedlíku v krku během polykání, častý kašel během polykání pevné stravy či tekutin, nutnost krájet jídlo na malé kousky apod.). Část pacientů s RS si nemusí být svých potíží s polykáním vůbec vědoma (a na základní otázku zjišťující jejich výskyt tedy odpoví negativně) či o riziku dysfagie vůbec neví a/nebo s ní popsané klinické potíže asociované s dysfagií vůbec nespojují. Proto na ně lékaře spontánně neupozorní a jejich odeslání ke specializovanému vyšetření může být opožděno. Lékaři i pacienti by přitom měli mít na paměti, že dysfagie je závažným problémem, a pacienti by měli být vyšetřeni již v počátečních stadiích jejího rozvoje, aby se předešlo potenciálním komplikacím, jako jsou malnutrice, dehydratace či aspirační pneumonie [1,12–15]. Podezření na výskyt dysfagie by mělo být samozřejmě objektivizováno jinými metodami než pouze anamnestickým dotazníkem, tedy prostřednictvím logopedického či otorinolaryngologického vyšetření a/nebo objektivních testů polykacích funkcí. Tato vyšetření však v klinické praxi nelze z řady důvodů provádět rutinně a jejich pomocí monitorovat pacienty již v presymptomatickém období. Při rozhodování o indikaci objektivního vyšetření polykání je proto možné vyjít právě z pozitivního výsledku skríningového nástroje DYMUS. DYMUS tak může sloužit jako indikační kritérium k dalšímu diagnostickému postupu při zachycení rizikových symptomů dysfagie.
Dotazník přitom v naší studii prokázal velmi dobrou opakovatelnost výsledků a jejich spolehlivost a vysokou vnitřní konzistenci testu.
Pro hodnocení opakovatelnosti jsme pro zajištění srovnatelnosti výsledků s dříve publikovanými studiemi použili korelační koeficient, a to s ohledem na non-normální distribuci našich dat koeficient Spearmanův. Tento statistický přístup není optimální [28], zvolili jsme ho ale právě pro možnost srovnání s výsledky ostatních publikovaných studií. Většina publikovaných studií však používá koeficient Pearsonův, a to navzdory tomu, že je takový přístup statisticky nesprávný, protože i v případě těchto studií vykazuje rozložení hodnot dotazníku DYMUS zcela jednoznačně non-normální distribuci [18,27]. Opakovatelnost vyjádřená korelačním koeficientem byla v naší práci vynikající a dosáhla hodnoty 0,94 (p < 0,001). Printza et al [18] hodnotí opakovatelnost pomocí Pearsonova korelačního koeficientu, který zde dosáhl hodnoty r = 0,637. Statistická významnost parametrických statistických testů (vč. Pearsonova korelačního koeficientu) je však při jejich použití na identických datech vždy nižší oproti testům neparametrickým (vč. koeficientu Spearmanova) a prosté numerické srovnání hodnot není validní. Rozdíl v použitých statistických testech tak umožňuje pouze konstatovat, že v případě obou studií je opakovatelnost vysoká, i když vlastní hodnoty korelačních koeficientů nejsou plně srovnatelné. Dotazník DYMUS prokázal v naší studii také vysokou míru vnitřní konzistence hodnocenou pomocí tzv. Cronbachovy alfa, která dosáhla hodnoty 0,916 ve skupině pacientů s RS a 0,921 v souboru zdravých dobrovolníků. Předchozí publikované validační studie originálního dotazníku či jeho jazykových verzí prokazují ve stejném statistickém testu velmi podobné hodnoty: hodnota Cronbachova alfa dosáhla v řecké validační studii 0,866 [18] v originální verzi 0,914 [17], a v turecké validační studii 0,91 [27].
V souhrnu tedy naše práce přinesla vytvoření a validaci české verze dotazníku DYMUS, který je jednoduchým skríningovým nástrojem pro zhodnocení rizika dysfagie u pacientů s RS. Česká verze dotazníku vykazuje srovnatelnou validitu, opakovatelnost, spolehlivost a vnitřní konzistenci jako originální verze DYMUS a jeho následně validované další jazykové mutace.
Etické aspekty
Autoři prohlašují, že studie na lidských subjektech popsaná v manuskriptu byla provedena v souladu s etickými standardy příslušné komise (institucionální a národní) odpovědné za provádění klinických studií a Helsinskou deklarací z roku 1975, revidovanou v roce 2000.
Postupy byly schváleny Etickou komisí FN Brno dne 9. 1. 2019 (03-090119/EK), pacienti podepsali informovaný souhlas. Původní autor dotazníku (Roberto Bergamaschi – roberto.bergamaschi@mondino.it) souhlasil s překladem do českého jazyka.
Rukopis byl přečten a schválen k publikaci všemi spoluautory a byly splněny požadavky na autorství.
Grantová podpora
Práce byla podpořena z prostředků MZ ČR – RVO (FNBr, 65269705) a projektem specifického výzkumu č. MUNI/A/1325/2019 z programu podpory studentských projektů na Masarykově univerzitě.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Poděkování
Bc. Naděždě Šaškové za pomoc při překladu dotazníku DYMUS.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
doc. MUDr. Eva Vlčková, Ph.D.
Neurologická klinika LF MU a FN Brno
Jihlavská 340/20
625 00 Brno
e-mail: evlckova@email.cz
Přijato k recenzi: 29. 1. 2020
Přijato do tisku: 23. 4. 2020
Sources
1. Calcagno P, Ruoppolo G, Grasso MG et al. Dysphagia in multiple sclerosis – prevalence and prognostic factors. Acta Neurol Scand 2002; 105 (1): 40–43. doi: 10.1034/j.1600-0404.2002.10062.x.
2. Fernandes AM, Duprat Ade C, Eckley CA et al. Oropharyngeal dysphagia in patients with multiple sclerosis: do the disease classification scales reflect dysphagia severity. Braz J Otorhinolaryngol 2013; 79 (4): 460–465. doi: 10.5935/1808-8694.20130082.
3. Guan XL, Wang H, Huang HS et al. Prevalence of dysphagia in multiple sclerosis: a systematic review and meta-analysis. Neurol Sci 2015; 36 (5): 671–668. doi: 10.1007/s10072-015-2067-7.
4. Pajouh SD, Moradi N, Yazdi MJ et al. Diagnostic evaluation of dysphagia in multiple sclerosis patients using a Persian version of DYMUS questionnaire. Mult Scler Relat Disord 2017; 17: 240–243. doi: 10.1016/j.msard.2017.08.012.
5. Solaro C, Rezzani C, Trabucco E et al. Prevalence of patient-reported dysphagia in multiple sclerosis patients: an Italian multicenter study (using the DYMUS questionnaire). J Neurol Sci 2013; 331 (1–2): 94–97. doi: 10.1016/j.jns.2013.05.020.
6. Kurtzke JF. Rating neurologic impairment in multiple sclerosis: an Expanded Disability Status Scale (EDSS). Neurology 1983; 33 (11): 1444–1452. doi: 10.1212/wnl.33.11.1444.
7. Thomas F, Wiles CM. Dysphagia and nutritional status in multiple sclerosis. J Neurol 1999; 246 (8): 677–682. doi: 10.1007/s004150050431.
8. Bergamaschi R, Crivelli P, Rezzani C et al. The DYMUS questionnaire for the assessment of dysphagia in multiple sclerosis. J Neurol Sci 2008; 269 (1–2): 49–53. doi: 10.1016/j.jns.2007.12.021.
9. Wiesner W, Wetzel SG, Kappos L et al. Swallowing abnormalities in multiple sclerosis: correlation between videofluoroscopy and subjective symptoms. Eur Radiol 2002; 12 (4): 789–792. doi: 10.1007/s003300101086.
10. Tassorelli C, Bergamaschi R, Buscone S et al. Dysphagia in multiple sclerosis: from pathogenesis to diag-nosis. Neurol Sci 2008; 29 (Suppl 4): S360–S363. doi: 10.1007/s10072-008-1044-9.
11. Sumelahti ML, Hakama M, Elovaara I et al. Causes of death among patients with multiple sclerosis. Mult Scler 2010; 16 (12): 1437–1442. doi: 10.1177/1352458510379244.
12. Belafsky P, Mouadeb D, Rees C et al. Validity and reliability of the Eating Assessment Tool (EAT-10). Ann Otol Rhinol Laryngol 2008; 117 (12): 919–924. doi: 10.1177/000348940811701210.
13. Ekberg O, Hamdy S, Woisard V et al. Social and psychological burden of dysphagia: its impact on diagnosis and treatment. Dysphagia 2002; 17 (2): 139–146. doi: 10.1007/s00455-001-0113-5.
14. Hemmett L, Holmes J, Barnes M et al. What drives quality of life in multiple sclerosis? QJM 2004; 97 (10): 671–676. doi: 10.1093/qjmed/hch105.
15. Prosiegel A, Schelling E, Wagner-Sonntag E. Dysphagia and multiple sclerosis. Int MS J 2004; 11 (1): 22–31.
16. Patel DA, Sharda R, Hovis KL et al. Patient-reported outcome measures in dysphagia: a systematic review of instrument development and validation. Dis Esophagus 2017; 30 (5): 1–23. doi: 10.1093/dote/dow028.
17. Bergamaschi R, Rezzani C, Minguzzi S et al. Validation of the DYMUS questionnaire for the assessment of dysphagia in multiple sclerosis. Funct Neurol 2009; 24 (3): 159–162.
18. Printza A, Kalaitzia M, Bakirtzisb C et al. Reliability and validity of the DYMUS questionnaire for the assessment of dysphagia in multiple sclerosis (Greek version) and proposed modification. Mult Scler Relat Disord 2018; 23: 62–68. doi: 10.1016/j.msard.2018.05.004.
19. Sales D, Alvarenga R, Vasconcelos C et al. Translation, cross-cultural adaptation and validation of the Portuguese version of the DYMUS questionnaire for the assessment of dysphagia in multiple sclerosis. Springerplus 2013; 2: 332. doi: 10.1186/2193-1801-2-332.
20. Beaton DE, Bombardier C, Guillemin F et al. Guidelines for the process of cros s-cultural adaptation of self-report measures. Spine 2000; 25 (24): 3186–1391.
21. Guillemin F, Bombardier C, Beaton D. Cross-cultural adaptation of health-related quality of life measures: literature review and proposed guidelines. J Clin Epidemiol 1993; 46 (12): 1417–1432. doi: 10.1016/0895-4356 (93) 90142-n.
22. Thompson A, Banwell B, Barkoff F et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald Criteria. Lancet Neurol 2018; 17 (2): 162–173. doi: 10.1016/S1474-4422 (17) 30470-2.
23. Wu MC, Chang YC, Wang TG et al. Evaluating swallowing dysfunction using a 100- ml water swallowing test. Dysphagia 2004; 19 (1): 43–47. doi: 10.1007/s00455-003-0030-x.
24. Bot AG, Becker SJ, Mol MF et al. Validation of phone administration of short-form disability and psychology questionnaires. J Hand Surg Am 2013; 38 (7): 1383–1387. doi: 10.1016/j.jhsa.2013.03.033.
25. Alali D, Ballard K, Bogaardt H. Treatment effects for dysphagia in adults with multiple sclerosis: a systematic review. Dysphagia 2016; 31 (5): 610–618. doi: 10.1007/s00455-016-9738-2.
26. Terre-Boliart R, Orient-Lopez D, Guevara-Espinosa S et al. Oropharyngeal dysphagia in patients with multiple sclerosis. Rev Neurol 2003; 39 (8): 707–710. doi: 10.33588/rn.3908.2004247.
27. Tenekeci E, Kara B, Cetiz A et al. Validity and reliability of the Turkish version of the questionnaire for the assessment of dysphagia in multiple sclerosis. Arch Neuropsychiatr 2016; 55 (3): 243–247. doi: 10.5152/npa.2016.18105.
28. Dušek L, Pavlík T, Koptíková J. Analýza dat v neurologii VI. Přesnost, spolehlivost a reprodukovatelnost měření u diskrétních dat. Cesk Slov Neurol N 2007; 70/103 (6): 719-721.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2020 Issue 3
Most read in this issue
- Glioblastom grade IV – dlouhodobé přežití
- Bolesti hlavy v graviditě
- Primární progresivní afázie
- Kognitivní poruchy u dětí s epilepsií
