Trénink lokomoce v závěsu u pacientů po poranění míchy
Body Weight Support Locomotion Training in Spinal Cord Injured Patients
Body weight support locomotion training is a classical rehabilitation method in patients who have suffered injury to the spinal cord. It is based on the discovery that repetitive cyclic passive movements can stimulate locomotor centres in the spinal cord. Numerous studies have documented motor recovery in vertebrate animals and in incomplete spinal‑ cord‑ injured humans. Manual‑ assisted, body‑ weight support treadmill training requires a large number of physiotherapists working in an ergonomically inconvenient position. New approaches to robotic locomotion training are therefore being developed. The aim is to design a device that provides minimal necessary locomotion assistance depending on the severity of the motor impairment.
Key words:
spinal cord injury – plasticity – locomotion – rehabilitation – robotic device – treadmill
Authors:
J. Kříž; P. Káfuňková; B. Schreier; P. Kolář
Authors‘ workplace:
Spinální jednotka, Klinika rehabilitace a tělovýchovného lékařství UK 2. LF a FN v Motole, Praha
Published in:
Cesk Slov Neurol N 2010; 73/106(2): 124-130
Category:
Review Article
Overview
Lokomoční trénink v závěsu je dlouhodobě využívaná rehabilitační metoda u pacientů s míšní lézí. Vychází z poznatků, že opakovaným rytmickým pohybem dochází ke stimulaci lokomočních center v míše. Prováděné studie potvrzují obnovu či zlepšení motorických schopností u nižších obratlovců, ale také u lidí s nekompletní míšní lézí. Manuálně asistovaný trénink lokomoce na pohyblivém chodníku je náročný na dostatek personálu a vyčerpávající pro fyzioterapeuty, kteří jej provádějí v ergonomicky nepříznivé pozici. Proto jsou rozvíjeny a zdokonalovány různé koncepty robotem asistované chůze. Cílem je vytvořit zařízení schopné poskytnout pacientovi pouze takovou míru pomoci, kterou bude při nácviku chůze podle závažnosti motorického postižení vyžadovat.
Klíčová slova:
míšní poranění – plasticita – lokomoce – rehabilitace – robotické zařízení – pohyblivý chodník
Úvod
Jako nejzávažnější následek poranění míchy se většinou uvádí ztráta hybnosti. Dlouhodobě probíhá výzkum zaměřený na reparaci postižené nervové tkáně a především na obnovu lokomoce. Studie věnované intenzivnímu lokomočnímu tréninku u spinalizovaných krys a koček prokázaly obnovení chůzového vzoru. Další práce, které tuto metodu aplikovaly na vyšší obratlovce a člověka, však nejsou zdaleka tak úspěšné. Zlepšení chůzového stereotypu bylo zaznamenáno pouze ve skupině pacientů s motoricky nekompletní míšní lézí. Pozitivní efekt lokomočního tréninku je přikládán plasticitě centrálního nervového systému (CNS).
Plasticita CNS po spinálním poranění
Plasticita CNS je definována jako její schopnost průběžně reagovat na změny, které se odehrávají ve vnitřním a zevním prostředí, a přizpůsobovat se jim. Může se jednat i o reparaci patologicky změněné nervové tkáně. V případě poškození míchy mohou probíhat tyto procesy na všech úrovních centrálního nervového systému, tedy jak v kortikální a subkortikální oblasti, tak v míše samotné, a to nad úrovní léze i pod ní [1]. Reparace nervové tkáně probíhá dvěma způsoby: modifikací synaptických spojů v preexistujících spinálních okruzích (synaptická či neurální plasticita) a tvorbou nových spinálních okruhů remyelinizací a růstem nových nervových buněk (anatomická plasticita) [1,2].
Neurální plasticita představuje reorganizaci preexistujících neuronálních okruhů, které jsou přítomny v míše. Tyto spinální okruhy jsou u nižších savců zodpovědné za lokomoci a mohou pracovat nezávisle na supraspinální aktivitě [3,4]. Jsou definovány jako generátory centrálního pohybového vzoru (central pattern generators, CPG). Bylo zjištěno, že aktivitou podmíněná plasticita těchto neuronálních okruhů u zvířat mění senzitivně‑motorické funkce lumbosakrální míchy. Trénink lokomoce na pohyblivém chodníku u koček po kompletním přetětí míchy významně zlepšil obnovu jejich chůzového stereotypu. Stále však chybí jednoznačný důkaz o existenci CPG a hlavně jejich úloze v lokomoci u člověka [5].
Remyelinizace a růst nových nervových buněk byly pozorovány převážně u lézí periferních nervů nebo u lézí v oblasti zadních kořenů míšních [6]. V nedávné studii však byla pomocí opakovaného vyšetřování motorických evokovaných potenciálů u pacientů s nekompletní míšní lézí potvrzena hypotéza, že intenzivním lokomočním tréninkem na pohyblivém chodníku může dojít ke zlepšení funkce postiženého kortikospinálního traktu, a to i v chronickém stadiu po míšním poranění [7]. Růst nových nervových vláken jako reakce na poškození nervové tkáně může mít i negativní důsledky, jako je zhoršení spasticity nebo rozvoj neuropatické bolesti [8].
Trénink lokomoce v závěsu a jeho efekt na obnovení chůze
Pro stimulaci lokomočních center v míše je zásadní optimální množství aferentních vzruchů. Toho je dosaženo, pokud je dolními končetinami pohybováno v opakovaném rytmickém fyziologickém vzoru [9]. Senzorické vjemy, ke kterým v průběhu pasivních pohybů dochází, vedou k aktivaci svalů končetin, jež nejsou pod volní kontrolou [5,10]. Ke stimulaci lokomoce u pacientů po poranění míchy se již před více než 30 lety začal používat a rozvíjet trénink na pohyblivém chodníku s odlehčením hmotnosti těla v závěsu.
Existuje několik základních přístupů v rehabilitaci chůze – trénink s odlehčením hmotnosti těla s manuální asistencí, trénink s odlehčením hmotnosti těla v kombinaci s funkční elektrickou stimulací (FES), robotický trénink a podle míry poškození lze využít i trénink chůze v terénu. Trénink s odlehčením hmotnosti těla s použitím manuální asistence terapeuta umožňuje lépe cítit míru potřebné asistence pro jednotlivý krok. Je však obtížný pro fyzioterapeuty, dopomoc není konstantní a její míra a vývoj v čase se obtížně monitoruje. Trénink s odlehčením hmotnosti těla v kombinaci s funkční elektrickou stimulací podporuje více spinální reflexní aktivitu. Opakující se aktivace těchto reflexů může souviset s pozitivními neurálními změnami a může zlepšit synaptickou účinnost tohoto okruhu [11]. Na druhou stranu elektrický impulz podporující svalovou aktivitu může být vnímán u pacientů s inkompletní míšní lézí nepříjemně. Robotický trénink (počítačem řízené ortézy) umožňuje i velmi postiženým jedincům generovat chůzový motorický vzor podobný zdravým jedincům. I když je robotická chůze neustále zdokonalována tak, aby splňovala parametry chůze fyziologické, neumožňuje rotační pohyb pánve a nedovoluje pohyb kloubů dolních končetin v jiné než v sagitální rovině. Chůze v terénu a v přirozeném prostředí má celkový facilitační efekt, ale je náročná na stabilitu a koordinaci.
Srovnáním výsledků různých přístupů v rehabilitaci chůze a s ní spojených funkčních schopností u pacientů s nekompletní míšní lézí se ve své práci zabývali Field‑ Fote et al [12]. Podmínkou zařazení do studie byla schopnost vstát ze sedu s dopomocí jedné osoby a provést alespoň jeden krok. Hodnocená data napříč skupinami ukázala signifikantní vliv tréninku na rychlost chůze. Rozdíly mezi jednotlivými skupinami dle typu tréninku však byly statisticky nevýznamné. Mehrholz et al [13] zaznamenali významnější zlepšení u skupin, které absolvovaly trénink na pohyblivém chodníku s FES a trénink v terénu s FES. V další studii nebyl prokázán významný rozdíl mezi skupinou pacientů trénovaných na pohyblivém chodníku a skupinou pacientů, u kterých vertikalizace probíhala konvenčními metodami rehabilitace [14].
Efektivitu tréninku s odlehčením hmotnosti těla je možné podpořit faktory zvyšujícími lokomoční potenciál, jako jsou maximální možné zatížení dolních končetin (DKK) při stoji, rychlost pohybu, extenze v kyčli a zátěž, kterou nesou horní končetiny (HKK). Nárůst zatížení DKK při stoji zvyšuje extenční motoneuronovou aktivitu a facilituje lokomoci [9,10]. Rychlost pohybu by měla být podobná rychlosti běžné chůze. Extenze v kyčli při zatížení končetin na konci stojné fáze ulehčuje švihovou fázi krokového cyklu. Odpor kladený pohybu DKK ve švihové fázi může efektivně podpořit aktivitu flexorů během tréninku [9]. Aktivita HKK se ukazuje být stěžejní pro dynamiku chůze. Opora o HKK inhibuje dynamiku kroku a naopak reciproční přirozený švih HKK facilituje pohyb DKK při chůzi [10]. Lokomoční trénink může být limitován faktory vyplývajícími z neurologického deficitu, jako je snížená svalová aktivace, posturální nestabilita, hyperaktivita spinálních reflexů a s ní spojená spasticita. Vliv na obnovu či zlepšení lokomočních schopností mají dále tyto faktory: věk, výška léze, iniciální AIS (ASIA Impairment Scale) a případná sdružená poranění či komplikace jiných orgánových systémů.
Řada studií [10,12,15–18] ukazuje, že trénink s odlehčením hmotnosti těla u jedinců s inkompletní lézí je efektivní způsob, jak zlepšit parametry související s obnovou chůze (rychlost, vzdálenost a krokové dovednosti) a přispět ke zlepšení koordinace pohybu končetin, svalové síly, zvýšení energetického výdeje. Tento způsob tréninku má také vliv na stupeň nezávislosti, kvalitu života, neurologické změny, jako je EMG aktivita svalů, a funkci kortikospinálního traktu. Několik studií [10,19–21] hodnotilo efekt lokomočního tréninku u jedinců s kompletní míšní lézí. Bylo prokázáno, že ačkoli jsou tito pacienti schopni vyvinout patřičný lokomoční pohyb či nějakou svalovou aktivitu na pohyblivém chodníku během tréninku, nejsou schopni chůze v terénu. Profitovali však z tréninku zlepšením posturální adaptace, funkce kardiovaskulárního systému, střevních funkcí, trofiky tkání a psychické kondice.
Další pozitivní vlivy tréninku lokomoce v závěsu
Vývoj tréninku lokomoce v závěsu jako rehabilitační metody u spinálních pacientů byl veden snahou o zmírnění neurologického deficitu a obnovu aktivní hybnosti dolních končetin, která by byla využitelná pro chůzi. S rozvojem této metody se stále více objevují i práce hodnotící vliv tréninku lokomoce v závěsu i na jiné zdravotní důsledky poškození míchy.
Jedinci po míšním poranění mají vyšší prevalenci kardiovaskulárního onemocnění v porovnání s běžnou populací [22]. Příčinou je velmi pravděpodobně nejen snížení fyzické aktivity po úraze, ale i další změny tkáňového metabolizmu, které vedou ke zvýšené hladině LDL cholesterolu, celkového cholesterolu a triglyceridů a snížené hladině HDL cholesterolu. Dalším častým rizikovým faktorem je hyperglykemie a snížená glukózová tolerance. Pravidelný trénink lokomoce 3krát týdně u pacientů s nekompletní míšní lézí zlepšuje lipidový profil snížením LDL cholesterolu a poměru celkového a HDL cholesterolu, dále zlepšuje glukózovou toleranci a zvyšuje inzulinovou senzitivitu [14]. Rovněž byl zaznamenán pozitivní zásah do autonomního regulačního systému s ovlivněním srdeční frekvence a tlaku i pozitivní efekt v cévní dynamice femorálních a karotických arterií [23].
Zřejmým důsledkem plegie je výrazný úbytek svalové hmoty. Prvních 6–12 měsíců po poranění míchy dochází ke svalové atrofii a změnám v distribuci svalových vláken (zejména typu I, IIa a IIx). Zařadíme‑li lokomoční trénink do terapie v prvních šesti měsících od úrazu alespoň 2krát týdně, nedojde ke svalové atrofii a redistribuci svalových vláken v takovém rozsahu [14]. I u chronických pacientů, kde je do terapie zařazen lokomoční trénink v závěsu, dojde po určité době k nárůstu svalové hmoty. Pomocí biopsie byly také zaznamenány pozitivní změny v morfologii svalu. Po čtyřměsíčním tréninku lokomoce v závěsu u pacientky s chronickou motoricky kompletní míšní lézí došlo k nárůstu svalové hmoty, a to především hypertrofií vláken typu IIa a IIx [24].
V důsledku ztráty motoriky DKK, a tudíž přirozené zátěže, dochází rovněž k úbytku kostní hmoty (osteoporóza z inaktivity), a to již od druhého až čtvrtého dne po úraze. Osteoporóza je nejvýraznější v prvním až druhém roce po úraze. Pouze několik studií se zabývalo posouzením, zda lokomoční trénink ovlivní metabolizmus kosti, tyto studie však nepotvrdily přímý vliv tohoto tréninku na zvýšení kostní denzity [25].
Důležitým profitem tréninku lokomoce je zlepšení fyzické i psychické kondice, tedy i kvality života [14]. Studie zabývající se sledováním kvality života, výskytu deprese, pocitu zdraví a běžných denních aktivit potvrdila, že 12měsíční trénink lokomoce 3krát týdně u pacientů v chronickém stadiu po nekompletní míšní lézi byl spojen se zlepšením pocitu spokojenosti sám se sebou a se svými fyzickými schopnostmi, i když nedošlo k významnému zlepšení v běžných denních aktivitách. Nebyl prokázán vliv na výskyt deprese [26].
Typy přístrojů pro trénink lokomoce v závěsu
Manuálně asistovaný trénink chůze na pohyblivém chodníku má své limity. Trénink vyžaduje dostatek školeného personálu. Fyzioterapeuti jej provádějí v ergonomicky nepříznivé pozici a terapie pacientů s těžším postižením je často nad jejich fyzické možnosti. Postrádá také přesnost opakování pohybů DKK, neboť každý fyzioterapeut má specifický individuální přístup podle vlastních znalostí a zkušeností [27]. Manuálně asistovaný trénink rovněž neumožňuje objektivní hodnocení změny stavu v průběhu cvičení a výsledku lokomočního tréninku. Proto začala být vyvíjena řada robotických chůzových trenažérů.
V současné době jsou používány a rozvíjeny dva hlavní koncepty robotem asistované chůze. První koncept pracuje s pohyblivým chodníkem a řízenými ortézami (exoskeleton), které vedou pohyb DKK (např. Lokomat). Terapeut vstupuje do terapie jen prostřednictvím korekce pohybu pomocí počítačového programu. Druhým je koncept pohyblivých stupaček (footplates), které vedou pohyb chodidel. Kolenní ani kyčelní klouby nejsou fixovány, je třeba jejich manuální kontrola, což je podle autorů výhoda, neboť terapeut může korigovat postavení DKK podle potřeby [28]. Takto je konstruován německý Gait Trainer.
Zařízení využívající pohyblivý chodník
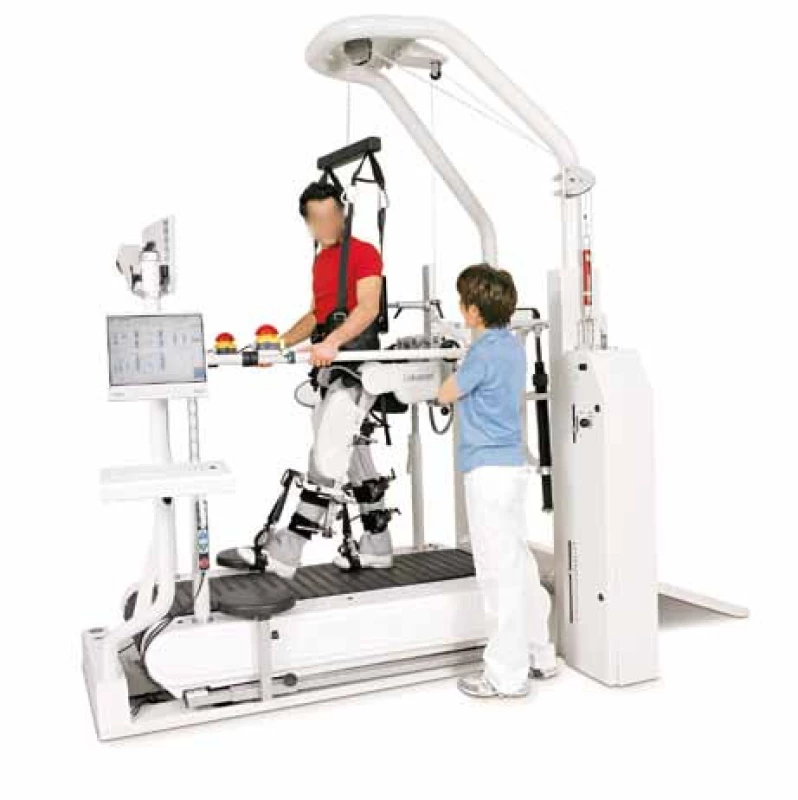
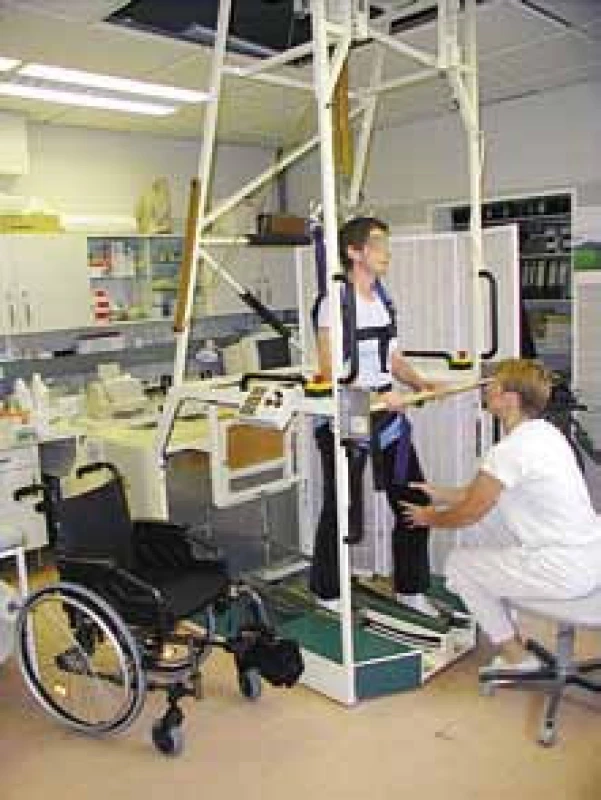
Lokomat
Zařízení bylo vyvinuto týmem odborníků z rehabilitačního centra ParaCare a firmy Hocoma z Zürichu. Lokomat tvoří motoricky řízené chůzové ortézy (driven gait orthosis, DGO), motoricky řízený závěsný systém odlehčení hmotnosti těla a pohyblivý chodník (obr. 1). Ortézy obsahují lineární pohony a senzory síly, které umožňují kontrolu flexe a extenze kyčle i kolene obou končetin. Senzory síly a senzory polohy kloubu jsou spojeny přes uživatelské rozhraní k počítači, který řídí přesný pohyb ortéz a synchronizuje jejich pohyb s pohyblivým chodníkem. Software je dále vybaven funkcí „guidance“, kterou terapeut nastavuje míru vedení pacientových DKK Lokomatem [29]. Senzory v ortézách zpětně informují o změnách silových momentů oproti přednastaveným parametrům. Tato zpětná vazba je graficky zobrazena na monitoru a terapeut i pacient je průběžně informován, nakolik je pohyb DKK aktivní nebo pasivní [30].
Lokomat má v terapii chůze své nevýhody, pasivní upnutí chodidla (foot lifter) a fixace pánve mění fyziologický kinetický vzor chůze. Trupová ortéza s popruhy na odlehčení a šířka postroje omezují přirozený souhyb horních končetin. Tato omezení jsou nutná z hlediska bezpečnosti. Pacienti jsou přesto schopni adaptace na chůzový vzor Lokomatu [31].
AutoAmbulator
Robotické zařízení vyvinuté Gerym Westem pro společnost HealthSouth v USA. Přístroj se skládá ze závěsného systému BWS, pohyblivého chodníku a tříramenného exoskeletonu (obr. 2). Horizontální rameno, které je pevně spojeno s hlavní částí přístroje, je v úrovni pánve pacienta, na jeho konec navazuje pohyblivý segment se stehenní objímkou a pod ním je segment pro upnutí bérce. Oba klouby mají jeden stupeň volnosti pro pohyb v sagitální rovině. K bércové části exoskeletonu je připojena ortéza pro uchycení přednoží. Pacient stojí čelem k hlavní části přístroje a drží se hrazdy. Závěsný systém umožňuje dávkování vertikální zátěže [32].
PAM (Pelvic Assist Manipulator)
Tým odborníků pod vedením D. Reinkensmeyera z University of California, Irvine a S. Harkemy z University of Louisville pracuje na robotickém chůzovém zařízení, které umožňuje během tréninku vést pohyby pánve. Předpokládají, že čím je pohyb v robotickém trenažéru přirozenější, tím větší funkční zlepšení lze očekávat.
PAM sestává z párových robotických stojanů s vodorovnou konzolou, na ní jsou tři pneumatické písty, které se upínají do zadní části pásu obepínajícího pánev pacienta (obr. 3). Systém využívá počítačovou regulaci tlaku v pístech a vede všechny pohyby pánve kromě anteverze a retroverze. Další funkcí systému PAM je činnost v režimu „teach‑ and‑ replay“. Software zaznamenává tlaky v pístech při manuálně asistovaném tréninku a následně přizpůsobuje dle aktuálního stavu robotickou asistenci [33].
POGO (Pneumatically Operated Gait Orthosis)
Pro zajištění stereotypu chůze u samostatně nechodících pacientů je potřeba kromě pánve vést také pohyby DKK. K tomu účelu je PAM propojen se systémem POGO. Skládá se z kolenních ortéz, ovládaných podobnými písty jako PAM (každá ortéza má jeden píst), které provádějí švihovou fázi DKK a brání podklesnutí či rekurvaci kolene ve fázi stojné.
Výhodou PAM a POGO je poddajnějšívedení pohybu a méně rigidní vzorec chůze po pohyblivém chodníku, než u Lokomatu. Tato volnost je však spojena s vět-ším rizikem nečekaných situací při tréninku. Autoři popisují, že bez další korekce může postupně docházet k desynchronizaci a interferencím mezi systémem PAM/POGO a pacientem [33].
ARTHuR (Assisting Robotic Tool for Human Rehabilitation)
Snahou vývoje optimálního přístroje pro trénink chůze je zajistit jen takovou asistenci pohybu, jaká je aktuálně třeba. Skupina rozvíjející systém PAM proto spolupracuje s týmem projektu ARTHuR. Technicky je systém kromě pohyblivého chodníku a závěsu vybaven kotníkovými ortézami, které jsou přes vodicí tyče ve tvaru „V“ připojeny k pohyblivým elektromotorům (obr. 4). Elektromotory s vodicími tyčemi se pohybují v kolejnicích pod postranními madly chodicího pásu. Pohybem vpřed ortézy provádějí švihovou fázi kroku, při stojné fázi se vracejí zpět synchronně s pohybem pásu. Zároveň se při švihu od sebe vzdálí a zvedají kotníkovou ortézu. Při došlapu a na konci stojné fáze se k sobě přiblíží tak, aby bylo chodidlo stále na pásu. ARTHuR pracuje rovněž v režimu „teach‑ and‑ replay“. Nejprve se provádí trénink chůze po pásu s manuální asistencí. Přístroj zaznamená prováděný pohyb (fáze učení) a je schopen jej automaticky opakovat již bez asistence terapeuta (fáze opakování). Je tak více využita zpětná vazba terapeuta a chůze je přesněji přizpůsobena aktuálnímu stavu pacienta [34].
LokoHelp
LokoHelp se skládá ze tří částí. Tvoří jej závěsný systém, pohyblivý chodník a samostatné elektromechanické chůzové zařízení Pedago (obr. 5). Pedago je fixováno k pohyblivému chodníku a převádí pohyb pásu na páky umístěné po obou stranách převodové skříně podobně jako pedály. Na pákách jsou připevněny hlezenní ortézy, do kterých se upínají DKK, proximální části končetin ani pánev nejsou zajištěny. Zařízení provádí cyklický pohyb po elipsové dráze a simuluje fáze kroku [35]. Nevýhodou je, že DKK nejsou v přímém kontaktu s pásem a terapeut musí kontrolovat postavení v kyčelních a kolenních kloubech.
Zařízení využívající pohyblivé stupačky
Mechanický chůzový trenažér „Mechanized Gait Trainer“ (GT I)
GT I vyvinutý týmem S. Hesseho z Berlína je přístroj, který provádí chůzi podobné cyklické pohyby dolních končetin u pacienta v závěsu. Místo chůze po pohyblivém chodníku má pacient chodidla ve stupačkách, které jsou spojnicemi uchyceny v otáčecímu mechanizmu (obr. 6). Výsledný pohyb je podobný krokovému cyklu DKK, klopení stupaček simuluje odvíjení chodidla od podložky. Převodní systém zaznamenává a vyhodnocuje aktuální rychlost a upravuje otáčivý moment podle toho, zda pacient pomáhá pohybu nebo mu naopak brání. Fyzioterapeut zajišťuje manuálně stabilitu kolenních kloubů a brání jejich hyperextenzi.
Výhodou tohoto systému je menší riziko poranění DKK než u přístrojů s pohyblivým chodníkem. Nevýhodou GT I je vymezení pohybu mechanickou trajektorií pouze v sagitální rovině. Na rozdíl od přirozené chůze nebo chůze po pohyblivém chodníku je u GT I menší dorzální flexe (DF) chodidla na konci švihové a začátku stojné fáze [36].
Pro zvýšení účinnosti tréninku bylo GT I doplněno o FESm. quadriceps femoris am. biceps femoris pro podporu stabilizace kolenního kloubu během stojné fáze [37].
HapticWalker
Skupina GT I dále rozvíjela svůj koncept pohyblivých stupaček a vyprojektovala přístroj HapticWalker (obr. 7). Zde jsou již pohyby stupaček (footplates) programovatelné. Každá stupačka je ovládána dvěma nezávislými elektromotory, které přes převodní systém táhel za stupačku vedou pohyby DKK. Pohybují‑li se současně dopředu nebo dozadu, pohyb stupačky probíhá v horizontální rovině, při změně vzdálenosti motorů je pohyb veden vertikálně. Navíc je na konci táhel motor s rotačním momentem, který klopí stupačku ve frontální rovině. Na počítači lze programovat trajektorii pohybu. Stupačky jsou vybaveny silovými senzory. Data ze senzorů jsou aktuálně vyhodnocována a porovnávána s nastavenou trajektorií. Výhodou této verze GT by měla být možnost tréninku přirozenějších krokových pohybů, včetně chůze po schodech a simulace nerovností terénu [28].
Systémy ARTHuR, PAM/POGO a Haptic Walker nejsou zatím komerčně dostupné.
Závěr
Současný výzkum je věnován vývoji takového zařízení, které by dokázalo rozeznat pohybový úmysl a motorické schopnosti pacienta a dát pacientovi zpětnou vazbu o provedeném pohybu. Tato zařízení by měla vést rehabilitaci chůze stejně jako kvalifikovaný terapeut, to znamená asistovat pacientovu pohybu jen tolik, kolik je třeba, a informovat pacienta, jak nejlépe koordinovat volní svalové úsilí pro daný pohyb.
I přes neustálé zdokonalování přístrojů pro nácvik lokomoce je zřejmé, že obnovení či zlepšení schopnosti chůze lze očekávat pouze u pacientů s motoricky nekompletní míšní lézí. Přesto je patrný pozitivní vliv tréninku například na kardiovaskulární systém, svalový metaboliz-mus a celkové zlepšení kvality života. Proto by měl být lokomoční trénink sou-částí rehabilitace pacientů po spinálním poranění.
Poděkování za zaslané fotografie přístrojů firmám Hocoma AG, Lokohelp Group, HealthSouth Corp., prof. Reinkensmeyerovi a prof. Hessemu
Přijato k recenzi: 17. 12. 2009
Přijato do tisku: 18. 1. 2010
MUDr. Jiří Kříž
Spinální jednotka, Klinika rehabilitace a tělovýchovného lékařství UK 2. LF a FN v Motole, Praha
V Úvalu 84
150 06 Praha 5
e-mail: jiri.kriz@fnmotol.cz
Sources
1. Raineteau O, Schwab ME. Plasticity of motor system after incomplete spinal cord injury. Nat Rev Neurosci 2001; 2(4): 263–273.
2. Curt A, Van Hedel HJ, Klaus D, Dietz V, EM‑SCI Study Group. Recovery from a spinal cord injury: significance of compensation, neural plasticity, and repair. J Neurotrauma 2008; 25(6): 677–685.
3. Duysens J, Van de Crommert HW. Neural control of locomotion; The central pattern generator from cats to humans. Gait Posture 1998; 7(3): 131–141.
4. Dietz V, Harkema SJ. Locomotor activity in spinal cord‑injured persons. J Appl Physiol 2004; 96(5): 1954–1960.
5. Dietz V. Body weight supported gait training: from laboratory to clinical setting. Brain Res Bull 2009; 78(1): I–VI.
6. Wilson P, Kitchener PD. Plasticity of cutaneous primary afferent projections to the spinal dorsal horn. Prog Neurobiol 1996; 48(2): 105–129.
7. Thomas SL, Gorassini MA. Increases in corticospinal tract function by treadmill training after incomplete spinal cord injury. J Neurophysiol 2005; 94(4): 2844–2855.
8. Woolf CJ, Salter MW. Neuronal plasticity: increasing the gain in pain. Science 2000; 288(5472): 1765–1769.
9. Lam T, Wirz M, Lünenburger L, Dietz V. Swing phase resistance enhances flexor muscle activity during treadmill locomotion in incomplete spinal cord injury. Neurorehabil Neural Repair 2008; 22(5): 438–446.
10. Behrman AL, Harkema SJ. Locomotor training after human spinal cord injury: a series of case studies. Phys Ther 2000; 80(7): 688–700.
11. Crone C, Nielsen J, Petersen N, Ballegaard M, Hultborn H. Disynaptic reciprocal inhibition of ankle extensors in spastic patients. Brain 1994; 117(5): 1161–1168.
12. Field‑Fote EC, Lindley SD, Sherman AL. Locomotor training approaches for individuals with spinal cord injury: a preliminary report of walking-related outcomes. J Neurol Phys Ther 2005; 29(3): 127–137.
13. Mehrholz J, Kugler J, Pohl M. Locomotor training for walking after spinal cord injury. Spine 2008; 33(21): E768–E777.
14. Hicks AL, Ginis KA. Treadmill training after spinal cord Injury: it’s not just about walking. J Rehab Res Dev 2008; 45(8): 241–248.
15. Morrison SA, Backus D. Locomotor training: is translating evidence into practice financially feasible? J Neurol Phys Ther 2007; 31(2): 50–54.
16. Behrman AL, Lawless‑Dixon AR, Davis SB, Bowden MG, Nair P, Phadke C et al. Locomotor traning progression and outcomes after incoplete spinal cord injury. Phys Ther 2005; 85(12): 1356–1371.
17. Hornby TG, Zemon DH, Campbell D: Robotic‑assisted, body‑weight‑supported treadmill training in individuals following motor incomplete spinal cord injury. Phys Ther 2005; 85(1): 52–66.
18. Visintin M, Barbeau H. The effects of body weight support on the locomotor pattern of spastic paretic patients. Can J Neurol Sci 1989; 16(3): 315–325.
19. Wirz M, Colombo G, Dietz V. Long term effects of locomotor training in spinal humans. J Neurol Neurosurg Psychiatry 2001; 71(1): 93–96.
20. Harkema SJ, Hurlley SL, Patel UK, Requejo PS, Dobkin BH, Edgerton VR. Human lumbosacral spinal cord interprets loading during stepping. J Neurolophysiol 1997; 77(2): 797–811.
21. Dietz V, Colombo G, Jensen L, Baumgartner L. Locomotor capacity of spinal cord in paraplegic patients. Ann Neurol 1995; 37(5): 574–582.
22. Bauman WA, Kahn NN, Grimm DR, Spungen AM. Risk factors for atherogenesis and cardiovascular autonomic function in persons with spinal cord injury. Spinal Cord 1999; 37(9): 601–616.
23. Phillips SM, Stewart BG, Mahoney DJ, Hicks AL, McCartney N, Tang JE et al. Body‑weight‑support treadmill training improves blood glucose regulation in persons with incomplete spinal cord injury. J Appl Physiol 2004; 97(2): 716–724.
24. Adams MM, Ditor DS, Tarnopolsky MA, Phillips SM, McCartney N, Hicks AL. The effect of body weight‑supported treadmill training on muscle morphology in an individual with chronic, motor‑complete spinal cord injury: A case study. J Spinal Cord Med 2006; 29(2): 167–171.
25. Giangregorio LM, Webber CE, Phillips SM, Hicks AL, Craven BC, Bugaresti JM, McCartney N. Can body weight supported treadmill training increase bone mass and reverse muscle atrophy in individuals with chronic incomplete spinal cord injury? Appl Physiol Nutr Metab 2006; 31(3): 283–291.
26. Hicks AL, Adams MM, Ginis KA, Giangregorio LM, Latimer A, Phillips SM et al. Long‑term body‑weight‑supported treadmill training and subsequent follow‑up in persons with chronic SCI: effects on functional walking ability and measures of subjective well‑being. Spinal Cord 2005; 43(5): 291–298.
27. Colombo G, Joerg M, Schreier R, Dietz V. Treadmill training of paraplegic patients using a robotic orthosis. J Rehabil Res Dev 2000; 37(6): 693–700.
28. Schmidt H, Werner C, Bernhardt R, Hesse S, Krüger J. Gait rehabilitation machines based on programmable footplates. J Neuroeng Rehabil 2007; 4: 2.
29. Riener R, Lünenburger L, Colombo G. Human‑centered robotics applied to gait training and assessment. J Rehabil Res Dev 2006; 43(5): 679–694.
30. Lünenburger L, Colombo G, Riener R. Biofeedback for robotic gait rehabilitation. J Neuroeng Rehabil 2007; 4: 1.
31. Hidler JM, Wall AE. Alterations in muscle activation patterns during robotic‑assisted walking. Clin Biomech 2005; 20(2): 184–193.
32. Mantone J. Getting a leg up? Rehab patients get an assist from devices such as HealthSouth’s AutoAmbulator, but the robots‘ clinical benefits are still in doubt. Mod Healthc 2006; 36(7): 58–60.
33. Aoyagi D, Ichinose WE, Harkema SJ, Reinkensmeyer DJ, Bobrow JE. A robot and control algorithm that can synchronously assist in naturalistic motion during body‑weight‑supported gait training following neurologic injury. IEEE Trans Neural Syst Rehabil Eng 2007; 15(3): 387–400.
34. Emken JL, Harkema SJ, Beres‑Jones JA, Ferreira CKand Reinkensmeyer DJ. Feasibility of Manual Teach‑-and‑Replay and Continuous Impedance Shaping for Robotic Lokomotor Training Following Spinal cord Injury. IEEE Trans Biomed Eng 2008; 55(1): 322–334.
35. Freivogel S, Mehrholz J, Husak‑Sotomayor T, Schmalohr D. Gait training with the newly developed ‚LokoHelp‘‑system is feasible for non‑ambulatory patients after stroke, spinal cord and brain injury. A feasibility study. Brain Inj 2008; 22(7–8): 625–632.
36. Hesse S, Uhlenbrock D. A mechanized gait trainer for restoration of gait. J Rehabil Res Dev 2000; 37(6): 701–708.
37. Hesse S, Werner C, Bardeleben A. Electromechanical gait training with functional electrical stimulation: case studies in spinal cord injury. Spinal Cord 2004; 42(6): 346–352.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2010 Issue 2
Most read in this issue
- Huntingtonova nemoc
- Neobvyklé klinické obrazy u migrény – kazuistiky
- Retrospektivní studie nálezů na magnetické rezonanci míchy a mozku u pacientů s diagnózou neuromyelitis optica
- Neurorehabilitace