Extra- intrakraniální arteri ální mikro anastomóza
Extra- intracranial Arteri al Micro anastomosis
Introducti on:
The a uthors present the gro up of pati ents indicated to extra- intracrani al bypass on the basis of evalu ati on of cerebrovascular re activity (CVR) by Transcrani al Doppler Sonography (TCD) and Functi onal Magnetic Resonance Imaging (fMRI).
Pati ents and methods:
Extra- intracrani al bypass was indicated for 35 pati ents over the last five ye ars.
Results:
During one ye ar follow‑up, CVR improved in 29 (82 %) pati ents. The patency of bypass was 92 % by TCD. CVR improvement was recorded in one pati ent after nine months. 30- day mortality was zero and 30- day morbidity was 2.9 %.
Conclusi on:
Both the non‑invasive methods of evalu ati on of CVR are safe, generally available and can be used for postoperative screening. Based on o ur experi ence, the use of the two methods can be recommended.
Key words:
extracrani al- intracrani al arteri al bypass – cerebrovascular re activity – transcrani al Doppler sonography – functi onal magnetic resonance imaging
Authors:
D. Krahulík 1; M. Vaverka 1; R. Herzig 2; P. Hluštík 2; M. Ho udek 1
Authors‘ workplace:
Ne urochirurgická klinika LF UP a FN Olomo uc, 2Ne urologická klinika LF UP a FN Olomo uc
1
Published in:
Cesk Slov Neurol N 2009; 72/105(2): 142-146
Category:
Original Article
Overview
Úvod:
V následujícím sdělení a utoři prezentují výsledky paci entů indikovaných k extra- intrakrani ální anastomóze na základě vyšetření cerebrovaskulární re aktivity (CVR) pomocí transkrani álního dopplerovského vyšetření (TCD) a funkční magnetické rezonance (fMR).
Paci enti a metodika:
V průběhu pěti let bylo pomocí výše uvedených metod indikováno k extra- intrakrani ální anastomóze 35 paci entů.
Výsledky:
Během ročního sledování došlo ke zlepšení CVR u 29 (82 %) paci entů. Průchodnost bypassu byla dle TCD vyšetření 92 %. Nejdelší interval do zlepšení CVR po operaci byl více než devět měsíců. 30denní mortalita byla v so uboru nulová a 30denní morbidita v so uboru byla 2,9 %.
Závěr:
Obě neinvazivní metody používané k vyšetření CVR a indikaci k extra- intrakrani álnímu bypassu (TCD a fMR) jso u spolehlivé, dostupné a lze je po užít i k po operačnímu sledování, protože umožňují provádění longitudinálních studi í bez radi ační zátěže. Na základě prezentovaných zkušeností a utorů lze kombinaci těchto metod doporučit k širšímu využití
Klíčová slova:
extra- intrakrani ální anastomóza – cerebrovaskulární re aktivita – transkrani ální dopplerovské vyšetření – funkční magnetická rezonance
Úvod
Extrakraniální-intrakraniální (EC-IC) anastomóza je operace, která má za cíl prevenci ischemického iktu u pacientů s vyčerpanou cerebrovaskulární reaktivitou při okluzi krkavice. V současné době se k vyšetření cerebrovaskulární reaktivity (CVR) a indikaci extra-intrakraniální mikroanastomózy používá několik metod testujících odpověď (vazodilataci, vazokonstrikci, změnu v extrakční frakci kyslíku) na rozdílný stimulus (změna pCO2, aplikace vazodilatátorů, motorický podnět). Za nejpřesnější vyšetření kvantitativně hodnotící CVR je stále považována pozitronová emisní tomografie (PET) sledující extrakční frakci kyslíku po inhalaci 15O značeného plynu. Další metody jako výpočetní tomografie (CT) s aplikací 133Xe [1], perfuzní CT [2], jednofotonová emisní výpočetní tomografie (SPECT) využívající 99mTc-HMPAO (SPECT) a near-infrared spektroskopie (NIRS) se také používají ke zjištění CVR, ale na rozdíl od PET dávají pouze nepřímou a semikvantitativní informaci o cerebrální reaktivitě. Vyšetření PET je v současné době špatně dostupné pro krátký poločas rozpadu 15O a většina dalších využívaných metod je také spojena s radiační zátěží.
Ve Fakultní nemocnici Olomouc se začala k vyšetření CVR používat kombinace neinvazivních metod – transkraniální dopplerovské sonografie (TCD) a funkční magnetické rezonance (fMR). Cílem práce bylo uvést výsledky pacientů indikovaných pomocí těchto metod k provedení EC-IC anastomózy.
Materiál a metodika
1. Pacienti
Od roku 2003 do roku 2008 bylo na základě vyšetření CVR pomocí TCD a fMR indikováno provedení EC-IC anastomózy u 35 pacientů (20 mužů, 15 žen; průměrný věk 64 let). 16 pacientů prodělalo cévní mozkovou příhodu (CMP) s dobrou regresí, 12 bylo zařazeno po TIA, event. RIND a sedm pacientů bylo asymptomatických. Každý pacient měl CT vyšetření nebo MR vyšetření mozku, kde ve 40 % bylo zachyceno postischemické ložisko. Bylo doplněno angiografické vyšetření (CTAG, popř. MRAG) k posouzení donoru a vhodného recipienta. K vyšetření CVR nebyli indikováni pacienti v těžkém celkovém stavu s výrazným fixním neurologickým deficitem a polymorbiditou neumožňující provedení operačního zákroku. Timing operace byl elektivní s průměrnou dobou pět měsíců od ischemické ataky nebo prvním kontaktem s naším pracovištěm u asymptomatických pacientů.
2. Vyšetření cerebrální vazomotorické reaktivity
2.1. Transkraniální dopplerovská sonografie
Vyšetření TCD bylo prováděno za použití přístroje Agilent SONOS 4500 (Agilent Technologies, Andover, MA) s použitím 2MHz transkraniální sondy. U pacientů s horší prostupností temporálního okna byl podán intravenózně echokontrast Optison®. Pacienti při vyšetření leželi pohodlně na zádech v tiché místnosti se standardní teplotou bez rušivých zrakových či sluchových stimulů. Rychlost krevního toku je změřena na obou středních mozkových tepnách (ACM) v klidu (normokapnie). K vyšetření CVR byla rychlost změřena také při hyper‑hypokapnii (test se zadržením dechu a hyperventilací, breath-holding/hyperventilation, BH/HV test) a také pouze při hyperkapnii (apnea test s výpočtem breath-holding indexu, BHI) [5–9]. Při prvním testu (BH/HV) bylo krátkodobé zadržení dechu (10 s) následováno hyperventilací (40 s). Pokles střední rychlosti toku krve alespoň o 15 % od základní hodnoty byl při BH/HV testu považován za fyziologický. BHI index byl vypočítán jako relativní nárůst střední rychlosti toku krve dělený délkou zadržení dechu v sekundách. Hodnoty 1,2 ± 0,6 byly považovány za normální. Paradoxní reakce se vzrůstem rychlosti toku krve při BH/HV a jejím poklesem při BHI testu byla považována za patologickou. Apnea test byl prováděn 10 minut po BH/HV testu.
2.2. Funkční magnetická rezonance
Vyšetření pomocí fMR předcházela instruktáž pacienta a zkouška jeho schopnosti provádět bimanuální sekvenční opozici palce a prstů ruky s frekvencí jednou za vteřinu. Tyto pohyby byly prováděny synchronně na obou rukou v určených intervalech a následným odpočinkem.
Vyšetření fMR bylo prováděno na přístrojích Siemens 1,5 Tesla (Avanti a Symphony, Siemens, Erlangen, Německo). Jako první bylo provedeno vyšetření mozku ve 30 vrstvách po pěti milimetrech zahrnující anatomické T1 vážené obrazy, Fluid-Attenuated Inversion Recovery (FLAIR) snímky k zachycení mozkových lézí, funkční T2 vážené obrazy, Blood Oxygenation Level Dependent (BOLD) vyšetření v průběhu pohybů prstů pacienta a také v klidu a jako poslední high‑resolution 3D anatomický sken (Magnetization Prepared Rapid Gratient Echo, MPRAGE). Pacient ležel v klidové pozici s fixovanou hlavou k minimalizaci pohybu. V průběhu strukturální části vyšetření pacient odpočíval a poté následovalo vyšetření fMR, při kterém byl pacient slovními pokyny instruován k zahájení, resp. ukončení pohybů. Časový interval pohybu a klidu byl 15 a 15 vteřin. Dále bylo provedeno vyšetření k zachycení evokované hemodynamické odpovědi na krátký čtyřsekundový stimulus a 26vteřinový klidový interval. Všechna vyšetření se opakovala dvakrát do celkového počtu čtyř vyšetření,trvajících cca 24 min (obr. 1, graf 1). Analýza dat proběhla za použití volně dostupného software AFNI a FSL.
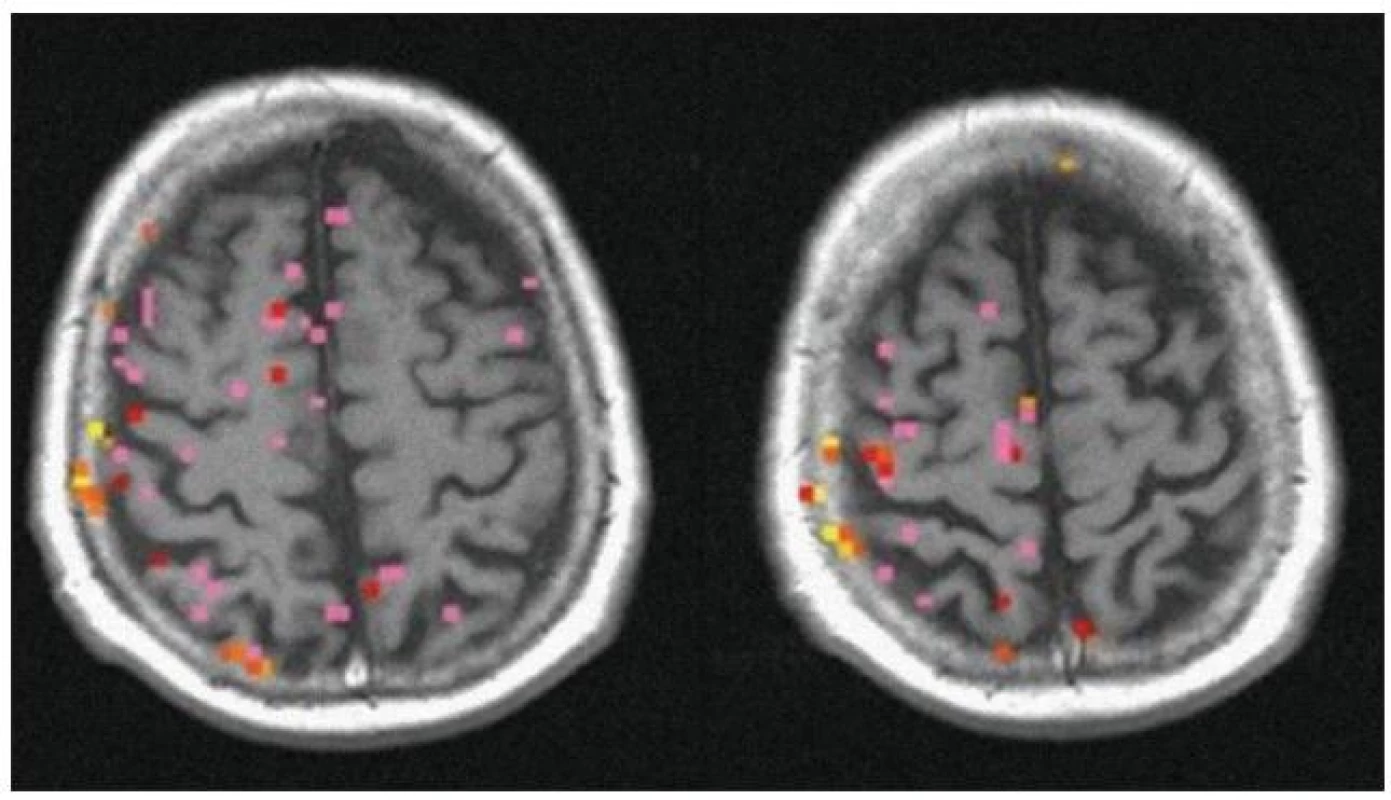

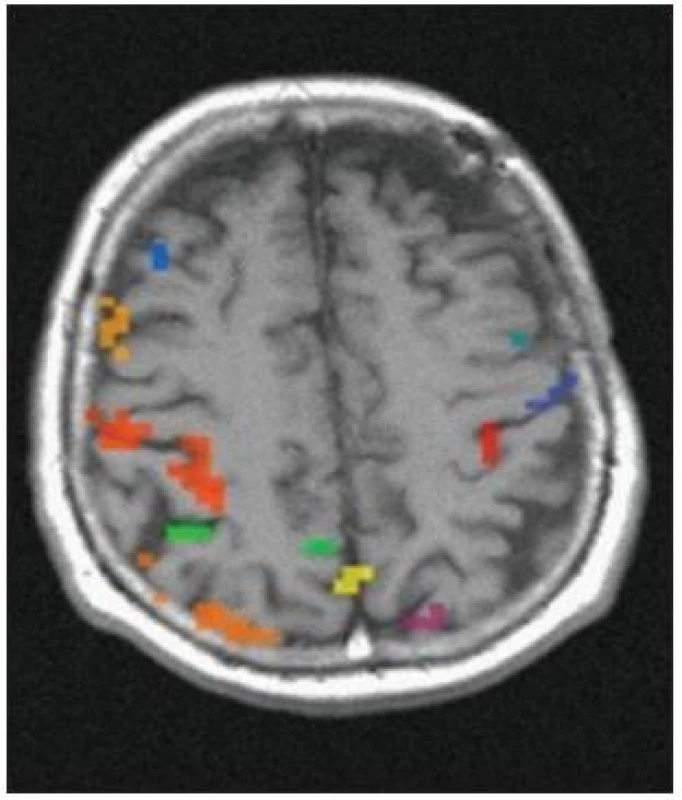
Případ minimálního hemodynamického postižení u pacienta s okluzí ACI vpravo demonstruje graf 2. Na grafu 3 je zobrazeno výrazné postižení hemodynamiky u pacienta s okluzí ACI vlevo.


3. Indikace extra-intrakraniální anastomózy
Neurochirurg ve spolupráci s neurologem vyhodnotil výsledky testů a zhodnotil také celkový stav pacienta. Před definitivní indikací k operaci byl pacient kompletně interně vyšetřen se zhodnocením rizika operačního výkonu vzhledem k vyššímu věku indikovaných pacientů a komplexnímu aterosklerotickému postižení. Donor arteria temporalis superficialis (ATS) byl vyšetřen palpačně a pouze při minimální pulzaci byla k jeho zobrazení použita CT angiografie nebo digitální subtrakční angiografie (s možnou balónkovou dilatací).
4. Extra-intrakraniální anastomóza
Operační výkon probíhal standardně v celkové anestezii, z malé pterionální kraniotomie, preparací obou větví ATS. Variací byl lineární řez nad průběhem ATS s použitím pouze jednoho raménka při respektování možné kranializace frontální větve ATS. Byly nasazeny klipy na donor, donor propláchnut a poté dilatován. Provedena malá kraniotomie centrovaná nad Silviovu rýhu. Připraveny recipienty M4 eventuálně při příznivém průběhu M3 a našit konvenční end to side bypass jednotlivými stehy Prolen 10.0. Okraje anastomózy a donoru upraveného do tvaru „fish mouth“ byly obarveny pyocyaninem. Byl kladen důraz jak na kvalitu anastomózy, tak i čas uzávěru. Následovala sutura tvrdé pleny, fixace záklopky a sutura po anatomických vrstvách, přičemž uzávěr jednotlivých vrstev je kompromisem mezi potenciálním uskřinutím tepny-donoru a prevencí vytvoření podkožní likvorové pseudocysty.
5. Pooperační sledování
Průchodnost bypassu byla sledována pomocí TCD. K dalším pooperačním kontrolám CVR byla použita vyšetření pomocí TCD a fMR za tři měsíce od operace (graf 4) a dále dle nálezu každý rok včetně hodnocení klinického stavu.

Výsledky
Korelace mezi BH/HV a BHI byla 58,6 %; κ = 0,205; mezi BH/HV a fMR 65,5 %; κ = 0,322; mezi BHI a fMR 58,6 %; κ = 0,151 a TCD (výsledek obou BH/HV a BHI testu) a fMR 70,6 %; κ = 0,414. Při indikaci k operaci při ne zcela korelujícím nálezu bylo superiorní vyšetření pomocí fMR, které je při vyšetření CVR přesnější.
V souboru 35 pacientů s porušenou CVR byla jednostranná okluze a. carotis interna (ACI) přítomna u 32, oboustranná u dvou pacientů a u jednoho pacienta byl přítomen uzávěr M1 úseku ACM.
Během ročního sledování došlo ke zlepšení CVR u 29 (82 %) pacientů. Průchodnost bypassu byla dle TCD vyšetření 92 %. Nejdelší interval do zlepšení CVR po operaci byl více než devět měsíců (obr. 2).
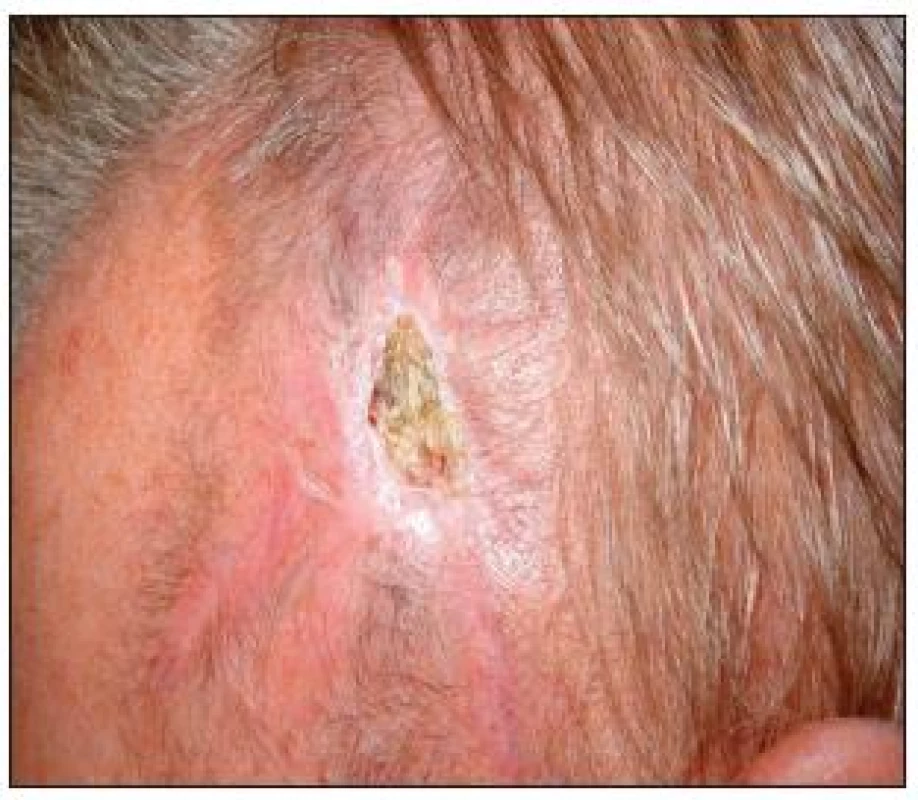
30denní mortalita byla v souboru nulová, jeden pacient zemřel půl roku po operaci na akutní infarkt myokardu a jedna pacientka tři měsíce po operaci na následky úrazu. Dva pacienti přestali docházet na pravidelné kontroly a dle registru pojištěnců nedošlo k jejich úmrtí do jednoho roku od operace. 30denní morbidita v souboru byla 2,9 %. 30denní přechodná morbidita pak byla 6,7 % a zahrnovala drobnou nekrózu rány (obr. 3), jeden případ subdurální kolekce a jednu přechodnou mozkovou ischemii s kompletní úpravou klinického stavu během čtyř měsíců. V průběhu ročního sledování došlo u jednoho pacienta k rozvoji ischemického iktu s hemiparézou homolaterálně ke spojce a u jedné pacientky k tranzitorní ischemické atace.
Diskuze
V současné době není zřejmé, zda vyšetření fMR může plnohodnotně nahradit PET [1]. TCD je široce rozšířená jako primární metoda k posouzení cerebrovaskulární reaktivity a kolaterální cirkulace. CVR je definována jako posun mezi cerebral blood flow (CBF) před použitím různého stimulu a po něm. Vyšetření CVR kombinací TCD a provokační vazodilatace umožňuje zjišťovat hemodynamický stav u pacientů při okluzi ACI. Předpokládá se, že TCD vyšetření by mohlo být využíváno k porovnání hemodynamické situace před provedením EC-IC bypassu a po něm, k posouzení kolaterální cirkulace v různých částech mozkového řečiště a také k predikci rozvoje demence po iktu [4,5]. Alternativní neinvazivní hemodynamické vyšetření používané ve FN Olomouc k vyšetření CVR je fMR za použití BOLD kontrastního vyšetření [2,3,6–8]. Funkční MR vyšetření může být použito k hemodynamickému vyšetření například i u asymptomatické stenózy ACI [9].
První EC-IC anastomózu provedli 30. 10. 1967 M. G. Yaşargil a P. Donaghy [10,11]. Od té doby si tato elegantní chirurgická metoda našla mnoho příznivců a zažila celosvětový rozmach, který byl téměř ukončen publikací Barnettovy studie [12,13], započaté v roce 1977 a publikované v roce 1985. Do této studie bylo zařazeno celkem 1 377 pacientů, z toho 714 do konzervativní a 663 do chirurgické větve. Ve výsledcích potom incidence závažných příhod a úmrtí v chirurgické větvi převyšovala incidenci mezi léčenými konzervativně o 3,2 %. Přestože tato studie obsahovala několik „bias“ a pacienti byli zařazování bez ohledu na stav CVR, trvalo pak desetiletí, než se EC-IC anastomóza opět vrátila do neurochirurgické praxe. Nové vyšetřovací metody uvedené na počátku práce zpřesnily vyšetření pacientů a umožnily vybrat specifickou skupinu profitující z provedení EC-IC bypassu. Jedná se cca o 10 % pacientů s uzávěrem ACI a vyčerpanou CVR v důsledku minimálního zásobení přirozenými kolaterálami, u kterých lze pomocí EC-IC anastomózy signifikantně snížit riziko rozvoje ischemické příhody [15–17]. V průběhu The St. Louis Carotid Occlusion Study bylo prokázáno, že riziko ipsilaterální mozkové příhody u pacientů s porušenou CVR činí 10,6 %/rok, resp. 26,5 %/dva roky. Oproti tomu u pacientů s neporušenou CVR činí riziko mozkového inzultu 2,4 %/rok, resp. 5,3 %/dva roky [14]. V současné době na základě výše uvedených výsledků je tato metoda používána ve větších centrech běžně, přestože její indikace je dle doporučení ESO 2008 experimentální. Vzhledem k nízké frekvenci tohoto výkonu, která v centrech kolísá kolem 6–8 operací za rok, považujeme za vhodné přípravu v laboratoři. Provádíme po vynikajících zkušenostech z workshopu v Českých Budějovicích anastomózu na potkanech, která dovoluje i při menším počtu výkonů zachovat operatérovi dostatečnou rutinu, zhodnocenou v kvalitě anastomózy a čase uzávěru.
Závěr
Obě neinvazivní metody požívané k vyšetření CVR a indikaci k EC-IC bypassu (TCD a fMR) jsou spolehlivé, dostupné a lze je použít i k pooperačnímu sledování, protože umožňují provádění longitudinálních studií bez radiační zátěže. Na základě prezentovaných zkušeností autorů lze kombinaci těchto metod doporučit k širšímu využití. EC-IC anastomóza reprezentuje typickou elektivní operaci sloužící u pacientů s okluzí ACI a vyčerpanou CVR ke snížení rizika rozvoje ischemického iktu, ale i kognitivního deficitu. Minimální doprovodná morbidita a mortalita jsou samozřejmým požadavkem. V případě nižší frekvence tohoto výkonu na pracovišti proto představuje laboratorní trénink vhodný doplněk.
MUDr. David Krahulík
Neurochirurgická klinika
LF UP a FN Olomouc
I. P. Pavlova 6
775 20 Olomouc
e‑mail:
david.krahulik@fnol.cz
Sources
1. Yamashita T, Kashiwagi S, Nakano S, Takasago T, Abiko S, Shiroyama Y et al. The effect of EC- IC bypass surgery on resting cerebral blo od flow and cerebrovascular reserve capacity studi ed with stable XE- CT and acetazolamide test. Ne uroradi ology 1991; 33(3): 217– 222.
2. Lythgoe DJ, Willi ams SC, Cullinane M, Markus HS. Mapping of cerebrovascular re activity using BOLD magnetic resonance imaging. Magn Reson Imaging 1999; 17(4): 495– 502.
3. Kleinschmidt A, Steinmetz H, Sitzer M, Merboldt KD, Frahm J. Magnetic resonance imaging of regi onal cerebral blo od oxygenati on changes under acetazolamide in carotid occlusive dise ase. Stroke 1995; 26(1): 106– 110.
4. Müller M, Voges M, Pi epgras U, Schimrigk K. Assessment of cerebral vasomotor re activity by transcrani al Doppler ultraso und and bre ath- holding. A comparison with acetazolamide as vasodilatory stimulus. Stroke 1995; 26(1): 96– 100.
5. Widder B. Use of bre ath holding for evalu ating cerebrovascular reserve capacity. Stroke 1992; 23(11): 1680– 1681.
6. Hlustik P, Solodkin A, Gullapalli RP, Noll DC, Small SL. Somatotopy in human primary motor and somatosensory hand representati ons revisited. Cereb Cortex 2001; 11(4): 312– 321.
7. Small SL, Hlustik P, Noll DC, Genovese C, Solodkin A. Cerebellar hemispheric activati on ipsilateral to the paretic hand correlates with functi onal recovery after stroke. Brain 2002; 125(7): 1544– 1557.
8. Herzig R, Hlustik P, Mares J, Burval S, Herman M, Kanovsky P. Cerebral vasore activy assessment in unilateral common carotidartery occlusi on with patency of external and internal carotidarteri es. An fMR study of the motor cortex. Cerebrovasc Dis 2006; 21 (Suppl 4): 67.
9. Carusone LM, Srinivasan J, Gitelman DR, Mesulam MM, Parrish TB. Hemodynamic response changes in cerebrovascular dise ase: implicati ons for functi onal MR imaging. Am J Ne uroradi ol 2002; 23(7): 1222– 1228.
10. Yaşargil MG. Microsurgery Appli ed To Ne urosurgery. Stuttgart: Ge org Thi eme Verlag 1969.
11. Yaşargil MG, Krayenbuhl HA, Jacobson JH jr. Microne urosurgical arteri al reconstructi on. Surgery 1970; 67(1): 221– 233.
12. Barnett HJ, Fox A, Hachinski V, Haynes B, Peerless SJ, Sackett D et al. Further conclusi ons from the extracrani al- intracrani al bypass tri al. Surg Ne urol 1986; 26(3): 227– 235.
13. Barnett HJ, Sackett D, Taylor DW, Haynes B, Peerless SJ, Meissner I et al. Are the results of the extracrani al- intracrani al bypass tri al generalizable? N Engl J Med 1987; 316(13): 820– 824.
14. Derdeyn CP, Yundt KD, Videen TO, Carpenter DA, Grubb RL jr, Powers WJ. Incre ased oxygen extracti on fracti on is associ ated with pri or ischemic events in pati ents with carotid occlusi on. Stroke 1998; 29(4): 754– 758.
15. Beneš V et al (eds). Ischémi e mozku. Praha: Galén 2003.
16. Kaku Y, Watarai H. Less invasive technique for EC- IC bypass. Acta Ne urochir Suppl 2008; 103: 83– 86.
17. Mehdorn HM. Cerebral revascularizati on by EC- IC bypass – present status. Acta Ne urochir Suppl 2008; 103: 73– 77.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2009 Issue 2
Most read in this issue
- Krční myelopatie – diagnostický problém
- Neurodegenerativní demence
- Maligní tumor z pochvy periferního nervu – dvě kazuistiky
- Radi ofrekvenční terapi e facetových bolestí bederní páteře