Manažment pacientov s roztrúsenou sklerózou liečených perorálnym kladribínom po štyroch rokoch od začiatku liečby
Authors:
P. Turčáni 1; A. Cimprichová 2; A. Cvengrošová 3; V. Donáth 4; V. Hančinová 5; F. Jurčaga 6; E. Kantorová 7; E. Klímová 3; P. Koleda 8; S. Kováčová 9; G. Krastev 10; D. Slezáková 11; J. Szilasiová 12; M. Vítková 12
Authors‘ workplace:
I. neurologická klinika LF UK a UN Bratislava, Slovensko
1; Neurologické oddelenie FN Trenčín, Slovensko
2; Neurologické oddelenie FNsP J. A. Reimana Prešov, Slovensko
3; II. neurologická klinika SZU a FNsP FDR Banská Bystrica, Slovensko
4; Neurologická klinika SZU a UN Bratislava, Slovensko
5; Neurologická klinika SZU UN-Nemocnica sv. Michala Bratislava, Slovensko
6; Neurologická klinika JLF a UN Martin, Slovensko
7; Neurologická klinika UVN-FN Ružomberok, Slovensko
8; Neurologická klinika FN Nitra, Slovensko
9; Neurologické oddelenie FN Trnava, Slovensko
10; II. neurologická klinika LF UK a UN Bratislava, Slovensko
11; Neurologická klinika LF UPJŠ a UNLP Košice, Slovensko
12
Published in:
Cesk Slov Neurol N 2023; 86(4): 283-285
Category:
doi:
https://doi.org/10.48095/cccsnn2023283
Stanovisko Slovenskej neurologickej spoločnosti SLS na základe konsenzu panelu expertov
Perorálny kladribín je vysoko účinná pulzná selektívna imunorekonštitučná liečba relapsujúcej roztrúsenej sklerózy (RS) [1]. Kladribín (2-chlóro-2‘-deoxyadenozín [2-CdA]) je analóg deoxyadenozínu, ktorý selektívne a prechodne znižuje počet B lymfocytov (predovšetkým CD19+) a T lymfocytov (CD4+ a CD8+) indukciou apoptózy, čím sa preruší kaskáda imunopatologických mechanizmov rozvoja ochorenia. Špecifická aktivita kladribínu voči lymfocytom adaptívneho imunitného systému a súčasne jeho mierny vplyv na vrodenú imunitu znižuje riziko nežiaducich infekcií v dôsledku liečby [2–4]. Úplná liečba kladribínom pozostáva z dvoch liečebných cyklov (kumulatívna dávka 3,5 mg/kg) podávaných s ročným odstupom, po ktorých sa v 3. a 4. roku nevyžaduje a neodporúča ďalšie podanie kladribínu. Aktuálne platný Súhrn charakteristických vlastností (summary of product characteristics; SPC) lieku Mavenclad (Merck, Darmstadt, Nemecko) pokrýva len štvorročné obdobie a nerieši manažment pacienta v 5. a nasledujúcich rokoch z hľadiska možnosti opakovaného podania kladribínu, keďže doteraz neboli zrealizované relevantné klinické štúdie [5].
Na Slovensku je terapia Mavencladom hradená z verejného zdravotného poistenia od septembra 2018 a v súčasnosti viacerí liečení pacienti vstúpili do piateho roku od obdobia iniciácie liečby. Vzhľadom na možnosť reaktivácie choroby [6,7] je potrebné venovať týmto pacientom osobitnú pozornosť a mať pripravený terapeutický program pri prípadnom znovuobjavení sa zápalovej aktivity, resp. pri progresii choroby. V krajinách, kde táto situácia vznikla skôr, riešili absenciu výsledkov relevantných klinických štúdií vydaním expertných stanovísk odborníkov [8–10]. Analogický postup zvolila aj Slovenská neurologická spoločnosť. V septembri 2022 bol vytvorený panel expertov (14 neurológov z 12 neurologických pracovísk na Slovensku dlhodobo sa zaoberajúcich liečbou RS a zároveň majúcich vlastné klinické skúsenosti s liečbou Mavencladom), ktorí dosiahli konsenzus na nasledovnom expertnom stanovisku:
1. Mavenclad predstavuje vysoko účinnú a vo všeobecnosti bezpečnú a dobre tolerovanú dlhodobú liečbu relapsujúcej roztrúsenej sklerózy, ktorá má v porovnaní s režimom kontinuálnej liečby viacero výhod – plánovanie gravidity, očkovanie, nenáročný predpísaný monitoring, nižšia záťaž pacienta, priaznivý pomer rizika a prínosu liečby, lepšia adherencia a vysoký komfort pacienta vďaka krátkym cyklom perorálnej aplikácie, čo prispieva k zlepšeniu kvality života pacienta.
2. Podanie Mavencladu po 4 rokoch od začatia liečby je v súlade s SPC lieku, pretože ani v časti 4.3 (Kontraindikácie) a ani v časti 4.4 (Osobitné upozornenia a opatrenia pri používaní) nie je uvedená ako kontraindikácia maximálna kumulatívna dávka kladribínu alebo predchádzajúca liečba kladribínom.
3. Manažment pacienta liečeného Mavencladom má vychádzať z pravidelného štrukturovaného monitorovania, ktoré okrem predpísaného stanovenia počtu lymfocytov 2 mesiace a 6 mesiacov po začatí liečby v každom terapeutickom roku a štandardného skríningu rakoviny, zahŕňa aj hodnotenie aktivity a progresie choroby najmenej raz ročne – počet a závažnosť relapsov, Expanded Disability Status Scale (EDSS), nové alebo zväčšené T2 lézie na MR. Pre uľahčenie rozhodovania o liečebnej stratégii je vhodné používať aj ďalšie parametre – chôdza na čas (Timed 25-Foot Walk; T25-FW), 9-jamkový kolíkový test (Nine-Hole Peg Test; 9-HPT), Symbol Digit Modalities Test (SDMT), hladina neurofilamentov v krvi (NfL), volumetria mozgu.
4. Algoritmus manažmentu pacientov liečených Mavencladom zosúladený s platnými indikačnými obmedzeniami (IO) (obr. 1):
DMT – chorobu modifikujúcu liečba; IO – indikačné obmedzenie
Fig. 1. Decision-making algorithm for the management of multiple sclerosis patients treated with oral cladribine.
DMT – disease modifying treatment; IO – indicative limitation
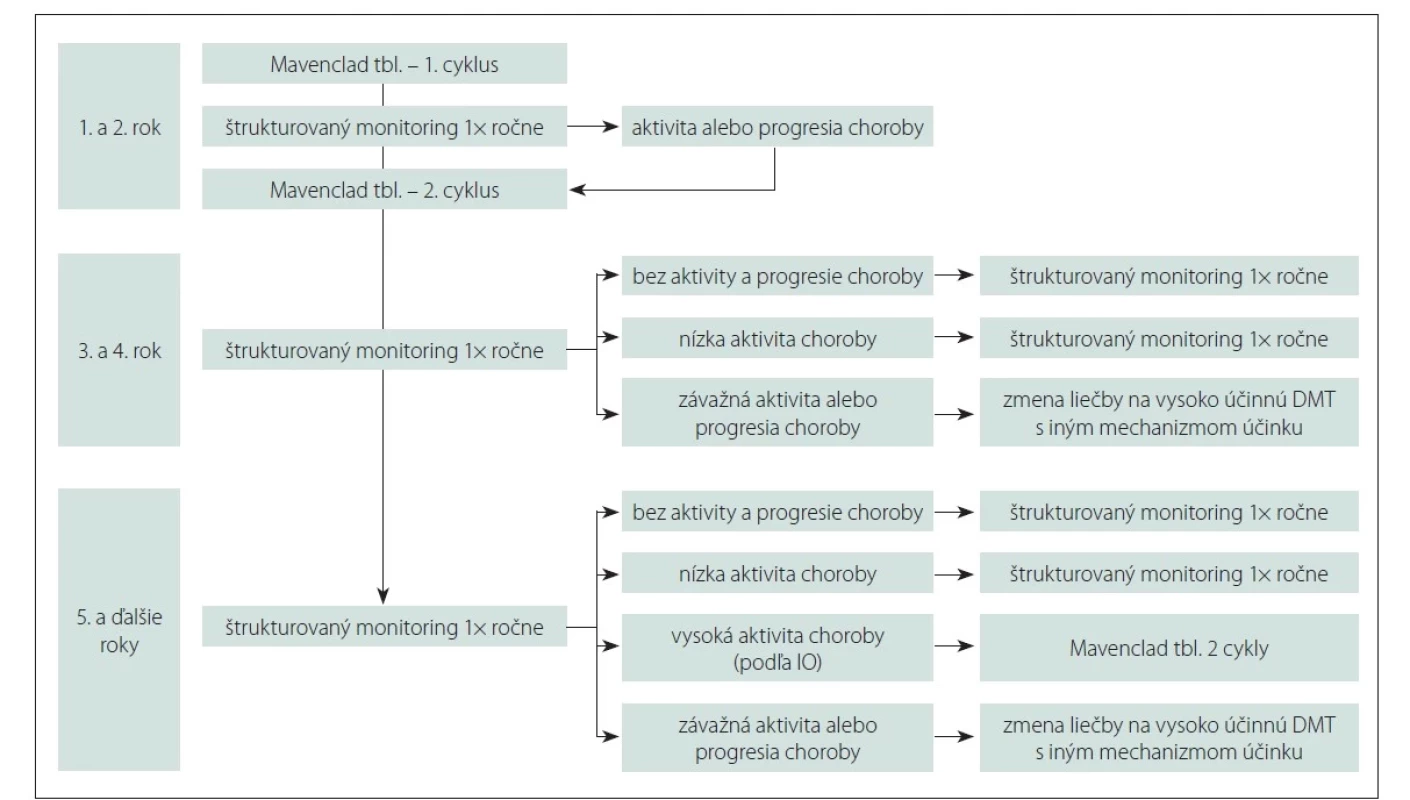
• Podanie 1. a 2. cyklu liečby Mavencladom – štrukturovaný monitoring raz ročne. V prípade pretrvávania zápalovej aktivity alebo progresie po podaní 1. cyklu pokračovať v liečbe 2. cyklom. Zmenu liečby zvážiť len pri závažnej zápalovej aktivite alebo progresii – > 1 relaps alebo > 4 T2 lézie, zvýšenie EDSS (potvrdené po 6 mesiacoch) o 1,5 bodu pri východzej hodnote EDSS = 0, o 1 bod pri východzej hodnote EDSS > 0 a < 5, o 0,5 bodu pri východzej hodnote EDSS ≥ 5. Pri rozhodovaní je potrebné zohľadniť aj priebeh choroby, predchádzajúcu liečbu, fakultatívne parametre aktivity, komorbidity a tiež individuálne potreby pacienta.
• V rokoch 3 a 4 u pacientov, ktorí absolvovali dva cykly liečby Mavencladom – štrukturovaný monitoring raz ročne. Ak sa zistí nízka zápalová aktivita (pribudnutie 1–2 T2 lézií) odporúčame pokračovať v monitoringu bez nasadenia inej chorobu modifikujúcej liečby (disease modifying treatment; DMT).
• Pri závažnej zápalovej aktivite alebo progresii choroby zvážiť liečbu iným vysokoúčinným liekom s iným mechanizmom účinku. Neodporúčame použiť liek s nižšou terapeutickou účinnosťou, pretože ide o pacienta, ktorému bol indikovaný Mavenclad vzhľadom na vysokú aktivitu choroby. Pri voľbe alternatívneho lieku zvážiť priebeh choroby, závažnosť relapsov, počet nových lézií, liečbu pred podaním Mavencladu, komorbidity a tiež individuálne potreby pacienta. V intervale troch mesiacov pred podaním novej liečby je potrebné zrealizovať MR pre aktualizáciu východiskových hodnôt.
• V 5. a ďalších rokoch po kompletnej liečbe Mavencladom – štrukturovaný monitoring rozšírený o fakultatívne parametre raz ročne. U pacientov bez aktivity a progresie choroby a u pacientov s nízkou aktivitou pokračovať v monitoringu. Snaha o predĺženie obdobia bez liečby vychádza z predpokladu pozitívneho vplyvu na kvalitu života pacienta.
Vysoká aktivita choroby v zmysle platných IO („Hradená liečba sa môže indikovať u dospelých pacientov s diagnózou vysoko aktívnej relapsujúcej RS definovanou klinickými príznakmi alebo pomocou zobrazovacích vyšetrení: 1. s 1 závažným relapsom liečeným kortikosteroidmi alebo zvýšením EDSS aspoň o jeden stupeň v predchádzajúcom roku a aspoň 1 T1 Gd+ léziou, alebo ≥ 9 T2 léziami počas liečby aspoň jedným DMT, alebo 2. s 2 alebo viacerými nespôsobilosť spôsobujúcimi relapsami liečenými kortikosteroidmi v prechádzajúcom roku, liečených alebo neliečených iným DMT“ [11]) je indikáciou pre opakované podanie kompletnej liečby Mavencladom (2 cykly, celková dávka 3,5 mg/kg telesnej hmotnosti počas 2 rokov). Preferencia opakovaného podania Mavencladu je daná skutočnosťou, že už odliečení pacienti sa považujú za respondérov so strednodobou alebo pretrvávajúcou odpoveďou [9,12].
Pacienti so závažnou aktivitou choroby nespĺňajúcou alebo prekračujúcou IO lieku Mavenclad sú kandidátmi pre liečbu inou vysoko účinnou DMT. Finálne rozhodnute o liečbe musí byť prísne individualizované a je potrebné zohľadniť klinický priebeh choroby, históriu liečby, odpoveď na predchádzajúcu liečbu, aktivitu choroby pred podaním Mavencladu, počet a závažnosť relapsov, počet a lokalizáciu nových/rozširujúcich sa lézií na MR, perzistujúcu a recidivujúcu aktivitu, fakultatívne parametre aktivity, komorbidity ako aj individuálne potreby pacienta.
Konflikt záujmov
Autori deklarujú, že v súvislosti s predmetom štúdie nemajú žiadny konflikt záujmov.
prof. MUDr. Peter Turčáni, PhD.
I. neurologická klinika
LF UK a UN Bratislava
Pažítková 4
821 01 Bratislava
Slovensko
e-mail: turcani1@gmail.com
Přijato do tisku: 3. 8. 2023
Sources
1. Giovannoni G, Comi G, Cook S et al. A Placebo-controlled trial of oral cladribine for relapsing multiple sclerosis. N Engl J Med 2010; 362 (5): 416–426. doi: 10.1056/NEJMoa0902533.
2. Comi G, Cook S, Giovannoni G et al. Effect of cladribine tablets on lymphocyte reduction and repopulation dynamics in patients with relapsing multiple sclerosis. Mult Scler Relat Disord 2019; 29: 168–174. doi: 10.1016/j.msard.2019.01.038.
3. Leist TP, Weissert R. Cladribine: mode of action and implications for treatment of multiple sclerosis. Clin Neuropharmacol 2011; 34 (1): 28–35. doi: 10.1097/ WNF.0b013e318204cd90.
4. Giovannoni G, Mathews J. Cladribine tablets for relapsing-remitting multiple sclerosis: a clinician’s review. Neurol Ther 2022; 11 (2): 571–595. doi: 10.1007/s40120-022-00339-7.
5. European Medicines Agency. Súhrn charakteristických vlastností lieku. Mavenclad. [online]. Available from: https: //www.ema.europa.eu/en/documents/product-information/mavenclad-epar-product-information_sk.pdf.
6. Giovannoni G, Soelberg Sorensen P, Cook S et al. Safety and efficacy of cladribine tablets in patients with relapsing-remitting multiple sclerosis: Results from the randomized extension trial of the CLARITY study. Mult Scler J 2018; 24 (12): 1594–1604. doi: 10.1177/1352458517727603.
7. Giovannoni G, Aydemir A, Cantogno EVD et al. CLASSIC-MS: Long-term efficacy and real-world treatment patterns for patients with relapsing multiple sclerosis who received cladribine tablets in phase III parent trials (1919). [online]. Available from: https: //n.neurology.org/content/96/15_Supplement/1919.
8. Meca-Lallana V, García Domínguez JM, López Ruiz R et al. Expert-agreed practical recommendations on the use of cladribine. Neurol Ther 2022; 11 (4): 1475–1488. doi: 10.1007/s40120-022-00394-0.
9. Meuth SG, Bayas A, Kallmann B et al. Long-term management of multiple sclerosis patients treated with cladribine tablets beyond year 4. Expert Opin Pharmacother 2022; 23 (13): 1503–1510. doi: 10.1080/14656566.2022.2106783.
10. Habek M, Drulovic J, Brecl Jakob G et al. Treatment with cladribine tablets beyond year 4: a position statement by southeast european multiple sclerosis centers. Neurol Ther 2023; 12 (1): 25–37. doi: 10.1007/s40120-022-00422-z.
11. Ministerstvo zdravotníctva SR. Zoznam kategorizovaných liekov 1. 5. 2023 – 31. 5. 2023. [online]. Dostupné z: https: //www.health.gov.sk/Zdroje?/Sources/kategorizacia/zkl/202305/cast_B_ind_obmedzenia_k_-01_05_ 2023.rtf.
12. Meuth SG, Bayas A, Kallmann B et al. Long-term management of multiple sclerosis patients treated with cladribine tablets: an expert opinion. Expert Opin Pharmacother 2020; 21 (16): 1965–1969. doi: 10.1080/ 14656566.2020.1792885.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2023 Issue 4
Most read in this issue
- Diagnostika kořenové avulze u poranění brachiálního plexu před chirurgickým výkonem
- Psychometrická validácia dotazníka MSQOL-54 na Slovensku – pilotná štúdia
- Klonální hematopoéza neurčitého potenciálu je možná a dosud nepopsaná příčina cévní mozkové příhody
- Zrakové evokované potenciály lze vyšetřit novým mobilním přístrojem kdekoliv
