Management deliria v neurointenzivní péči v České republice – dotazníková studie
Delirium management in neurointensive care in the Czech Republic – a survey
Delirium is a phenotypic syndrome that is difficult to detect in the intensive care. In neurointensive care, the symptoms of delirium overlap with those of primary brain injury. At the same time, delirium is a predictive factor of higher morbidity and mortality and is often a sign of untreated extracerebral dysfunction or disease like sepsis, metabolic disturbance, and pharmacotherapy combined with immobilization. Thus, the monitoring of delirium in the neurointensive care is an important part of therapy and improvement of patients’ prognosis. Currently, there are validated tests with a relatively high validity and predictive value also in the Czech language. One of the diagnostic pitfalls, so far, is inadequate differential diagnosis of nonconvulsive epileptic status. In the survey, we focused on delirium management in neurointensive care in the Czech Republic. We have found sufficient awareness of the severity of delirium and its other consequences. On the other hand, its systematic monitoring, which is recommended, appears to be a persistent problem in our inpatient care.
Keywords:
stroke – delirium – delirium management
Authors:
L. Hrežová; J. Bednařík
Authors‘ workplace:
Neurologická klinika LF MU a FN Brno
Published in:
Cesk Slov Neurol N 2022; 85(4): 325-329
Category:
Short Communication
doi:
https://doi.org/10.48095/cccsnn2022325
Overview
Delirium je fenotypický syndrom, jehož detekce je v podmínkách intenzivní péče obtížná. U pacientů v neurointenzivní péči s primárním postižením mozku se navíc symptomy deliria překrývají s příznaky primární mozkové dysfunkce. Delirium přitom predikuje vyšší morbiditu a mortalitu a je často signálem neléčené extracerebrální poruchy či onemocnění, jako jsou sepse i metabolická porucha, vč. farmakologických vlivů v kombinaci s vlivem imobilizace. Proto je monitorace deliria v podmínkách neurointenzivní péče důležitou součástí léčby pacientů a zlepšení jejich prognózy. Aktuálně existují i v českém jazyce validované testy s relativně vysokou validitou a predikční hodnotou. Jedním z diagnostických úskalí je dosud nedostatečná diferenciální diagnostika nonkonvulzivního epileptického statu. V našem dotazníku jsme se zaměřili na management deliria v prostředí neurointenzivní péče v ČR. Zjistili jsme dostatečnou informovanost ohledně závažnosti deliria a jeho následků, na druhou stranu jeho systematická monitorace, která se doporučuje, se jeví jako přetrvávající problém v naší hospitalizační péči.
Klíčová slova:
cévní mozková příhoda – delirium – management deliria
Úvod
Delirium představuje závažnou kvalitativní poruchu vědomí, která se vyznačuje poruchou pozornosti, fluktuací mentálního stavu, narušenou úrovní vědomí a dezorganizovaným myšlením. Jedná se o fenotypicky různorodý syndrom, který se klinicky prezentuje ve třech formách: hyperaktivní, hypoaktivní a smíšené [1]. Hypoaktivní delirium se vyznačuje letargií a sníženými psychomotorickými funkcemi. Hyperaktivní delirium není na rozdíl od hypoaktivní formy obvykle přehlédnutelné, jelikož bývá spojeno s eskalací psychomotorického neklidu, agitací, agresivitou a občas i halucinacemi či bludy. Diagnostika smíšeného deliria může být složitá právě kvůli kolísání mezi hypoaktivitou a hyperaktivitou [2]. Delirium je nejčastější komplikací u hospitalizovaných pacientů nad 65 let [3] a jeho prevalence je dle nedávné metaanalýzy 31% v rámci dospělé populace na smíšené jednotce intenzivní péče (JIP) [1]. Je velmi časté zejména v prostředí intenzivní péče a u pacientů v kritickém stavu. Podkladem je akutní mozková dysfunkce. Patofyziologie deliria je komplexní a multifaktoriální, často jde o kombinaci několika vyvolávajících a predisponujících faktorů [2]. Jedním z předpokládaných patofyziologických mechanizmů akutní mozkové dysfunkce je porucha neurotransmiterů mozku, nejčastěji hypofunkce cholinergního nebo hyperfunkce dopaminergního systému [3]. Příčinou mohou být infekce, sepse, metabolický rozvrat, selhání vnitřních orgánů, farmakologické vlivy s imobilizací, senzorická deprivace, nedostatečná analgezie, ale i jakákoli strukturální mozková patologie [3]. Detekce deliria bývá v prostředí neurointenzivní péči komplikovaná, jelikož symptomy deliria se navíc překrývají s ložiskovými i celkovými příznaky primární mozkové dysfunkce [4]. I přes svou vysokou prevalenci se až 60 % epizod deliria nepodaří diagnostikovat, zejména u jeho hypoaktivní varianty [5]. Delirium přitom predikuje vyšší morbiditu a mortalitu a je spojené s krátkodobými i dlouhodobými následky. Pacienti, u kterých se po dobu hospitalizace rozvine delirium, mají značně prodlouženou délku hospitalizace a větší riziko úmrtí během ní [6]. S přihlédnutím k dlouhodobým následkům bylo delirium během hospitalizace asociováno s vyšší mortalitou během prvního roku po propuštění a u pacientů došlo častěji k poškození kognitivních funkcí [7]. V rámci prevence mají význam nefarmakologické postupy jako časná mobilizace, naopak farmakologická prevence (podávání antipsychotik) neprokázala vliv na snížení incidence nebo zkrácení trvání deliria u pacientů na JIP [8]. Monitorace deliria v podmínkách neurointenzivní péče je důležitou součástí léčby pacientů a zlepšení jejich prognózy. Doporučení Společnosti pro intenzivní medicínu (The Society of Critical Care Medicine’s guidelines for Pain Agitation and Delirium) radí rutinní monitoraci přítomnosti deliria u dospělých kriticky nemocných pacientů pomocí dotazníků, jako jsou the Confusion Assessment Method for the ICU (CAM-ICU) [9] nebo Intensive Care Delirium Screening Checklist (ICDSC) [10]. Pátrání po deliriu v podmínkách neurologické JIP má i svoje limitace, mezi které patří encefalopatie, kóma, pre-existující kognitivní deficit a specificky pro neurologické JIP pak afázie, neglect syndrom nebo jiné neurologické bariéry v interakci [11]. CAM-ICU a ICDSC jsou dva nejčastěji využívané screeningové testy a zároveň oba využívají škálu Richmond Agitation and Sedation Scale (RASS) [12]. Kvůli velké variabilitě prezentace deliria a jeho typické fluktuaci symptomů může být detekce složitá. Šance na úspěšnou diagnostiku deliria může zvýšit opakování vyšetření v průběhu dne a zapojení sesterského personálu. Původní validační studie pro ICDSC probíhala na smíšené JIP, která zahrnovala také pacienty s neurologickým onemocněním [10]. Na druhou stranu, validační studie pro CAM-ICU nezahrnovala pacienty s neurologickým deficitem, ale pacienty na umělé plicní ventilaci [9]. Na našem pracovišti jsme provedli validační studii české verze CAM-ICU, která potvrdila, že tento screeningový dotazník je vhodný k rutinnímu monitorování na iktových jednotkách [13]. Přetrvávajícím úskalím je mnohokrát absentující spolupráce pacienta, která je v případě dotazníku CAM-ICU nepostradatelná. V nedávné studii kohorty pacientů s intracerebrálním krvácením prokázal dotazník ICDSC větší přesnost v porovnání s CAM-ICU, jelikož ne všechny položky ICDSC vyžadují kooperujícího pacienta [14]. Větší senzitivitu pro ICDSC oproti CAM-ICU jsme dokázali i v průběhu pilotní studie na naší neurologické klinice, kdy jsme porovnávali již validovanou českou verzi CAM-ICU s nově validovanou českou verzí ICDSC [15]. Hledání vhodného univerzálního screeningového nástroje deliria, stejně jako jeho optimální management, však nadále zůstávají velkou výzvou.
Cíle a metodika
Podmínkou pro zlepšení diagnostiky a praktického managementu deliria v neurointenzivní péči je zmapování situace v této oblasti v ČR. Vytvořili jsme databázi všech neurologických lůžkových zařízení v ČR s e-mailovými kontakty jejich vedoucích pracovníků a v průběhu roku 2021 jsme těmto zařízením rozeslali dotazník zaměřený na diagnostiku, prevenci a management deliria v neurointenzivní péči (elektronická příloha 1) a po 6 měsících jsme žádost opakovaně zaslali pracovištím, která nereagovala.
Výsledky a diskuze
Do konce roku 2021 se do naší dotazníkové akce zapojilo 28 (37 %) oslovených pracovišť z celkového počtu 76. Odpovědi jsou shrnuty v elektronické příloze 1 a u vybraných otázek grafickou formou (obr. 1). Většina reagujících zařízení (25) uvedla, že hospitalizuje pacienty, kteří vyžadují monitoraci a/nebo intenzivní péči, a ve 23 případech šlo o pracoviště s vlastní JIP nebo iktovou jednotkou.
CAM-ICU – Confusion Assessment Method for the intensive care unit; ICDSC – Intensive Care Delirium Screening Checklist; JIP – jednotka intenzivní
péče; NCSE – nonkonvulzivní status epilepticus (nonconvulsive status epilepticus); UPV – umělá plicní ventilace
Fig. 1. Graphic representation of answers to selected questions of the survey.
CAM-ICU – Confusion Assessment Method for the intensive care unit; ICDSC – Intensive Care Delirium Screening Checklist; JIP – intensive
care unit; NCSE – nonconvulsive status epilepticus; UPV – lung ventilation
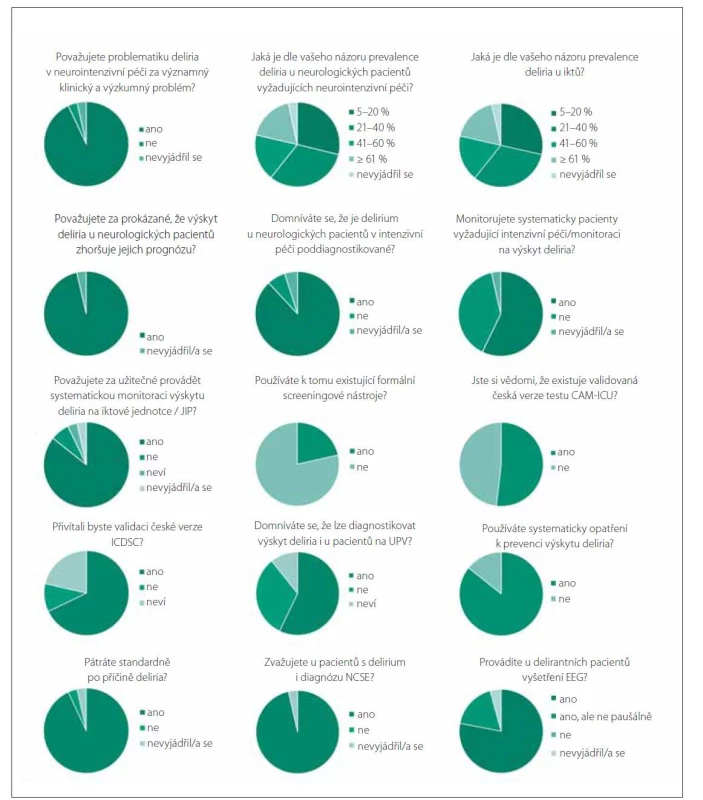
Drtivá většina (93 %) reagujících pracovišť považuje delirium za významný klinický a výzkumný problém, avšak odhadovaná prevalence v neurointenzivní péči a u iktů široce kolísá od 5 až do 60 %, což kromě rozdílů v populacích pacientů poukazuje také na rozdílné standardy diagnostiky deliria. V literatuře udávaná incidence deliria u pacientů po CMP je ovšem také široce variabilní, a to od 10 % [16] do 48 % [17].
U většiny pracovišť (89 %) panuje shoda, že je delirium výrazně poddiagnostikováno, a 86 % považuje systematickou monitoraci deliria za užitečnou. Na druhou stranu, pouze v lehce nadpoloviční většině (57 %) oddělení probíhá pravidelný screening k detekci deliria, a to i přes prokázané vyšší riziko mortality, delší doby hospitalizace a nutnost převzetí většího množství pacientů v zařízeních následné péče v porovnání s hospitalizovanými pacienty bez deliria [17], čehož si byla vědoma prakticky všechna kooperující pracoviště. Skutečný podíl pracovišť monitorujících výskyt deliria však bude pravděpodobně nižší, protože lze předpokládat, že na dotazník odpověděla prioritně ta pracoviště, která si jsou vědoma významu deliria a jeho screening provádějí. I přes existenci validovaných screeningových nástrojů je využívá pouze 21 % pracovišť. Konkrétně se využívají hlavně CAM-ICU nebo formální kritéria deliria podle Diagnostického a statistického manuálu duševních poruch (Diagnostic and Statistical Manual of Mental Disorders; DSM) ve verzi IV nebo V. Většina pracovišť přítomnost deliria vyhodnocuje pouze na základě klinických zkušeností. Polovina z nich zaregistrovala existenci validované české verze CAM-ICU [13], ale i tak by 68 % uvítalo validaci české verze ICDSC.
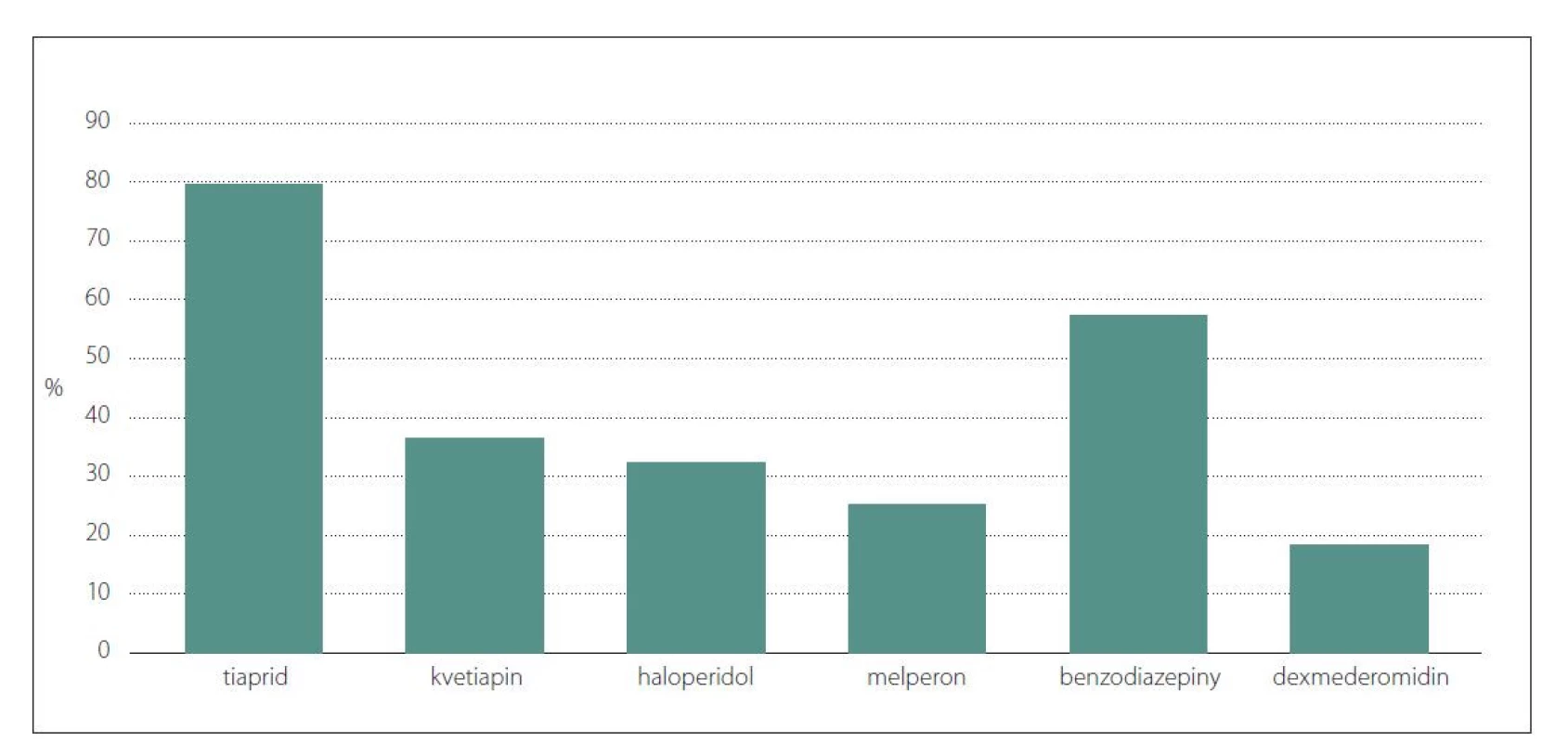
Klíčovou součástí managementu deliria je jeho prevence, což si uvědomuje 86 % pracovišť. Je prokázáno, že ABCDEF přístup (ABCDEF bundle) představuje nástroj ke koordinaci multidisciplinární péče o pacienty na JIP. Tento přístup zdůrazňuje důležitost monitorace deliria a také brzkou mobilizaci. Brzká mobilizace je součástí nefarmakologických postupů v prevenci a terapii deliria, avšak vedle dalších možných preventivních opatření, jako jsou např. reorientace, podpora správného režimu spánku, využívání naslouchátek a brýlí, nebo kontakt s rodinou, právě ona nejvíc snižuje trvání deliria [18]. V případě výskytu hyperaktivního deliria využívají na všech pracovištích farmakosedaci (100 %) (obr. 2) a kurtaci (96 %), které ovšem zároveň patří k rizikovým faktorům rozvoje deliria. Na rozdíl od hyperaktivní formy, u hypoaktivního deliria není jeho farmakoterapie antipsychotiky vhodná a kromě alkoholového deliria bychom se měli obecně vyvarovat benzodiazepinů [19]. Z tohoto pohledu je překvapivý a zřetele hodný vysoký podíl farmakosedace benzodiazepiny (obr. 2). Příčiny vzniku deliria bývají multifaktoriální a diagnostika by měla být zaměřena na anamnézu a fyzikální vyšetření, jelikož je často jediným příznakem skrytého závažného onemocnění [3]. Proto má smysl aktivní pátrání po příčině deliria, což akceptuje i 93 % oslovených pracovišť. V případě rozvoje deliria je vhodné provést základní laboratorní odběry a v případě negativity doplnit zobrazovací vyšetření podle kontextu základního onemocnění. Role EEG v samotné diagnostice deliria je limitována. Její význam narůstá v diferenciální diagnostice deliria vůči jiným stavům vyznačujícím se změnou úrovně vědomí, jakým je i nonkonvulzivní status epilepticus (nonconvulsive status epilepticus; NCSE) [2]. NCSE může představovat život ohrožující stav, který je definovaný změnou chování a/nebo kognice zároveň s přítomnou epileptiformní abnormitou na EEG [20]. EEG bývá standardním vyšetřením u delirantních pacientů na 79 % oddělení, 18 % jej provádí, ale ne v rámci rutiny. V diferenciální diagnostice je rovněž nutné pomýšlet na akutní psychotické poruchy.
Fig. 2. Representation of the most common pharmacotherapy options according to answers.
Návratnost naší dotazníkové akce (37 %) je v porovnání s obdobnými dotazníkovými studiemi velmi dobrá a umožnila nám získat relevantní přehled o managementu deliria v neurointenzivní péči v ČR. Největší zkreslení je dáno pravděpodobně faktem, že s větší pravděpodobností reagovala pracoviště, která považují problematiku deliria za důležitou a systematicky se jí věnují. Celková situace v ČR z hlediska vigilance této problematiky a doporučované systematické diagnostiky, prevence a managementu deliria tak bude pravděpodobně méně příznivá, než ukazují výsledky získané analýzou obdržených dotazníků.
Závěr
Z výsledků vyplývá, že na většině dotázaných pracovišť si uvědomují závažnost deliria, důležitost jeho diagnostiky a jsou obeznámeni i s diferenciální diagnózou NCSE. Na druhou stranu jsou patrné nedostatky v systematické monitoraci deliria, a právě využívání validovaných screeningových nástrojů by mohlo tuto situaci zlepšit. Hledání ideálního dotazníku zůstává i nadále výzvou. Vytvoření jednoduššího dotazníku, jenž by pomohl ke zvýšení využívání screeningových nástrojů k detekci deliria, by mohlo mít smysl i za cenu jeho případné nižší senzitivity.
Etické aspekty
Autoři prohlašují, že studie na lidských subjektech popsaná v manuskriptu byla provedena v souladu s etickými standardy příslušné komise (institucionální a národní) odpovědné za provádění klinických studií a Helsinskou deklarací z roku 1975, revidovanou v roce 2000. Studie nepodléhá schválení etickou komisí. Rukopis byl přečten a schválen k publikaci všemi spoluautory a byly splněny požadavky na autorství.
Grantová podpora
Práce byla podpořena z prostředků MZ ČR – RVO (FNBr, 65269705) a projektem specifického výzkumu č. MUNI/A/1144/2021 z programu podpory studentských projektů na Masarykově univerzitě a Interní grantovou agenturou Masarykovy univerzity MUNI/IGA/1309/ 2020.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
MUDr. Lucia Hrežová
Neurologická klinika
LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: hrezova.lucia@fnbrno.cz
Přijato k recenzi: 11. 4. 2022
Přijato do tisku: 4. 8. 2022
Sources
1. Krewulak KD, Stelfox HT, Leigh JP et al. Incidence and prevalence of delirium subtypes in an adult ICU: a systematic review and meta-analysis. Crit Care Med 2018; 46 (12): 2029–2035. doi: 10.1097/CCM.0000000000003 402.
2. Hshieh TT, Inouye SK, Oh ES. Delirium in the elderly. Clin Geriatr Med 2020; 36 (2): 183–199. doi: 10.1016/j.cger.2019.11.001.
3. Inouye SK, Westendorp RG, Saczynski JS. Delirium in elderly people. Lancet 2014; 383 (9920): 911–922. doi: 10.1016/S0140-6736 (13) 60688-1.
4. Patel MB, Bednarik J, Lee P et al. Delirium monitoring in neurocritically ill patients. Crit Care Med 2018; 46 (11): 1832–1841. doi: 10.1097/CCM.0000000000003349.
5. de la Cruz M, Fan J, Yennu S et al. The frequency of missed delirium in patients referred to palliative care in a comprehensive cancer center. Support Care Cancer 2015; 23 (8): 2427–2433. doi: 10.1007/s00520-015 - 2610-3.
6. Salluh JIF, Wang H, Schneider EB et al. Outcome of delirium in critically ill patients: systematic review and meta-analysis. BMJ 2015; 350: h2538–h2538. doi: 10.1136/bmj.h2538.
7. van den Boogaard M, Schoonhoven L, Evers AWM et al. Delirium in critically ill patients: impact on long-term health-related quality of life and cognitive functioning. Crit Care Med 2012; 40 (1): 112–118. doi: 10.1097/CCM.0b 013e31822e9fc9.
8. Barr J, Fraser GL, Puntillo K et al. Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Crit Care Med 2013; 41 (1): 263–306. doi: 10.1097/CCM. 0b013e3182783b72.
9. Ely EW, Inouye SK, Bernard GR et al. Delirium in mechanically ventilated patients. JAMA 2001; 286 (21): 2703–2710. doi: 10.1001/jama.286.21.2703.
10. Bergeron N, Dubois M-J, Dumont M et al. Intensive care delirium screening checklist: evaluation of a new screening tool. Intensive Care Med 2001; 27 (5): 859–864. doi: 10.1007/s001340100909.
11. Maas M, Naidech A. Critical care neurology perspective on delirium. Semin Neurol 2016; 36 (6): 601–606. doi: 10.1055/s-0036-1592318.
12. Ely EW, Truman B, Shintani A et al. Monitoring sedation status over time in ICU patients: reliability and validity of the Richmond Agitation-Sedation Scale (RASS). JAMA 2003; 289 (22): 2983–2991. doi: 10.1001/jama.289.22. 2983.
13. Mitasova A, Kostalova M, Bednarik J et al. Poststroke delirium incidence and outcomes: validation of the Confusion Assessment Method for the Intensive Care Unit (CAM-ICU). Crit Care Med 2012; 40 (2): 484–490. doi: 10.1097/CCM.0b013e318232da12.
14. Reznik ME, Drake J, Margolis SA et al. Deconstructing poststroke delirium in a prospective cohort of patients with intracerebral hemorrhage. Crit Care Med 2020; 48 (1): 111–118. doi: 10.1097/CCM.0000000000004031.
15. Hrežová L, Bednařík J. Diagnostika deliria v akutní fázi iktu. Cesk Slov Neurol N 2021; 84/117 (Suppl 1): S64.
16. Dahl MH, Rønning OM, Thommessen B. Delirium in acute stroke – prevalence and risk factors: delirium in acute stroke. Acta Neurol Scand Suppl 2010; 122 (190): 39–43. doi: 10.1111/j.1600-0404.2010.01374.x.
17. Shi Q, Presutti R, Selchen D et al. Delirium in acute stroke: a systematic review and meta-analysis. Stroke 2012; 43 (3): 645–659. doi: 10.1161/STROKEAHA.111.643726.
18. Marra A, Ely EW, Pandharipande PP et al. The ABCDEF bundle in critical care. Crit Care Clin 2017; 33 (2): 225–243. doi: 10.1016/j.ccc.2016.12.005.
19. American Geriatrics Society Expert Panel on Postoperative Delirium in Older Adults. American Geriatrics Society abstracted clinical practice guideline for postoperative delirium in older adults. J Am Geriatr Soc 2015; 63 (1): 142–150. doi: 10.1111/jgs.13281.
20. Holtkamp M, Meierkord H. Nonconvulsive status epilepticus: a diagnostic and therapeutic challenge in the intensive care setting. Ther Adv Neurol Disord 2011; 4 (3): 169–181. doi: 10.1177/1756285611403826.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2022 Issue 4
-
All articles in this issue
- Editorial
- Farmakogenetika dabigatranu a sekundární prevence ischemické cévní mozkové příhody
- Validace dotazníku pro hodnocení dopadu cévní mozkové příhody – česká verze Stroke Impact Scale 3.0
- Telemedicínské vyšetření kognitivními testy ALBA, POBAV a ACE-III
- Analýza variability srdeční frekvence během head-up tilt testu v diagnostice reflexních synkop – přehled problematiky a vlastní zkušenosti
- Management deliria v neurointenzivní péči v České republice – dotazníková studie
- Patologické nálezy na zobrazení pomocí magnetické rezonance u onemocnění asociovaného s pozitivními protilátkami proti myelinovému oligodendrocytárnímu glykoproteinu
- Zemřel profesor Zdeněk Mraček
- Účinky výtažku Ditan Tongmai v kombinaci s akupunkturou na rekonvalescenci po cévní mozkové příhodě hodnocené na základě elektroencefalogramu
- Post-COVID-19 vývoj chronické zánětlivé demyelinizační polyneuropatie s akutním začátkem léčené rituximabem
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Validace dotazníku pro hodnocení dopadu cévní mozkové příhody – česká verze Stroke Impact Scale 3.0
- Telemedicínské vyšetření kognitivními testy ALBA, POBAV a ACE-III
- Patologické nálezy na zobrazení pomocí magnetické rezonance u onemocnění asociovaného s pozitivními protilátkami proti myelinovému oligodendrocytárnímu glykoproteinu
- Management deliria v neurointenzivní péči v České republice – dotazníková studie
