Paraneoplastická polymyozitida u karcinomu prostaty – kazuistika
Paraneoplastic Polymyositis – a Case Report
Clinical findings, biochemical results and EMG investigation are important in the diagnosis of myopathy, and muscle biopsy is unavoidable for its further differentiation. In an older man with muscle pain and rapid development of muscle weakness with head-drop and dysphagia, polymyositis with focal endomysial CD8+ lymphocytic infiltrates was diagnosed on muscle biopsy. Once the patient had been hospitalized, an advanced carcinoma of the prostate and anti-Ri paraneoplastic antibodies were found. A paraneoplastic polymyositis was diagnosed, which is a rare diagnosis in patients with prostate cancer.
Key words:
dysphagia – neck muscles weakness – EMG – creatinkinase – muscle biopsy – paraneoplastic polymyositis
Authors:
J. Latta 1; J. Zámečník 2; E. Ehler 1
Authors‘ workplace:
Neurologická klinika FZS UP a Pardubická krajská nemocnice, a. s
1; Ústav patologie a molekulární medicíny, 2. LF UK a FN v Motole, Praha
2
Published in:
Cesk Slov Neurol N 2012; 75/108(1): 80-83
Category:
Case Report
Overview
Pro diagnostiku myopatie je důležitý klinický obraz, biochemické a EMG nálezy, nezbytná a pro další diferenciaci myopatie nezastupitelná je biopsie svalu. U staršího muže s polymyalgiemi a rychlým rozvojem svalové slabosti včetně přepadání hlavy s dysfagií byla diagnostikována polymyozitida s fokálními endomyziálními CD8+ lymfocytárními infiltráty ve svalové biopsii. Při hospitalizaci byl zjištěn pokročilý karcinom prostaty a v mozkomíšním moku anti-Ri paraneoplastické protilátky. Jednalo se tedy o paraneoplastickou polymyozitidu, která se u karcinomu prostaty vyskytuje výjimečně.
Klíčová slova:
dysfagie – slabost šíjových svalů – EMG – kreatinkináza – svalová biopsie – paraneoplastická polymyozitida
Úvod
Paraneoplastické syndromy se vyskytují asi u 8 % nemocných s nádory [1]. Mezi paraneoplastické syndromy patří řada neurologických projevů – senzitivní či senzitivně-motorická polyneuropatie, senzitivní neuronopatie, stiff-person syndrom a paraneoplastická polymyozitida [2]. Tyto syndromy jsou podmíněny působením protilátek, které lze prokázat v séru nemocných. Pokud jsou ve svalech výrazně zastoupeny infiltráty lymfocytů, tehdy se jedná o polymyozitidu [3]. A u této polymyozitidy je nutno zvážit paraneoplastickou patogenezi. Pokud převažují nekrotické změny svalových vláken a infiltráty chybí, nález se pak označuje jako paraneoplastická nekrotizující myopatie [4]. Postižení svalů u nádorových onemocnění není časté. Vyskytuje se u mužů s nádory plic, prostaty, zažívacího traktu a u žen s gynekologickými nádory a karcinomem prsu [5]. Jedná se o buď polymyozitidu s rychlou progresí, anebo o dermatomyozitidu s primárním postižením cév [2,6].
Na Neurologické klinice v Pardubicích jsme hospitalizovali staršího muže s bolestmi svalů a rychlým rozvojem svalové slabosti. V rámci diagnosticko-terapeutického procesu jsme se seznámili s mnoha důležitými klinickými fakty i výsledky pomocných vyšetření. Jsme přesvědčeni, že tyto informace jsou nejen zajímavé, ale mají i velký význam pro racionální postup. Proto jsme se rozhodli publikovat toto kazuistické sdělení.
Kazuistika
Jednasedmdesátiletý muž byl v prosinci 2009 přijat na neurologickou kliniku pro dva měsíce rychle progredující slabosti šíjového svalstva s přepadáním hlavy až ke sternu, od počátku s poruchou polykání, s kašlem při polykání s opakovanou aspirací, celkovou slabostí. Již od srpna 2009 si stěžoval na bolesti svalů a kloubů, otoky kloubů, zhoršené dýchání. Proto byl přijat na interní kliniku, kde koronarograficky prokázána nemoc tří tepen. Nález byl indikací k provedení aorto-koronárního bypassu, avšak pro nejasné svalové onemocnění byla pouze zavedena duální antiagregační léčba. V říjnu a listopadu prodělal opakovanou aspiraci s následnou pneumonií.
V předchorobí byla v roce 1989 provedena operace hiátové hernie, v roce 1994 prodělal infarkt myokardu, od té doby se léčí pro hypertenzi a hyperlipoproteinemii. Před třemi lety byla zjištěna benigní hypertrofie prostaty.
Nemocný užíval Anopyrin (100 mg), Plavix (75 mg), Betaloc ZOK 15 mg, Tritace 1,25 mg, Prednizon 10 mg, Furon 10 mg, Diclofenac Duo při bolesti. Statin (Ortonal 20 mg) byl vysazen již před dvěma měsíci.
Při přijetí na neurologii byl nemocný velmi pomalý, měl unavený vzhled, pomalou řeč, hlava přepadala až k hrudní kosti. Obtížně dotáhl pohled do stran, bez diplopie, patrové oblouky byly níže uložené, avšak zvedaly se symetricky, pomalá diadochokinéza jazyka, na HK byl zadržovaný pokles paží oboustranně a přitom měl silný stisk rukou. Nalezli jsme výrazné oslabení trupových a kořenových svalů končetin s atrofií. Chůze byla nestabilní, kolébavá, měl tendenci k záklonu trupu a nesvedl dřep. Palpace svalů paží i šíje byla bolestivá.
V laboratoři bylo nalezeno ALT 1,88 ukat/l (0,10–0,78), AST 3,72 ukat/l (0,05–0,72), CK 65,83 ukat/l (0,58–3,87), CKMB 7,24 ukat/l (0,00–0,10), přitom normální hodnoty bilirubinu (8 umol/l),GMT (0,39 ukat/l). Volný myoglobin v séru byl 1574 µg/l (25,0–72,0). PSA byla zvýšena 22,1 ng/ml (0,00–4,00).
V likvoru bez buněk, bílkovina 0,44 g/l, mírná elevace beta-2-mikroglobulinu, pozitivita anti-Ri a ANNA 2, s podezřením na paraneoplastický syndrom (Topelex, Praha).
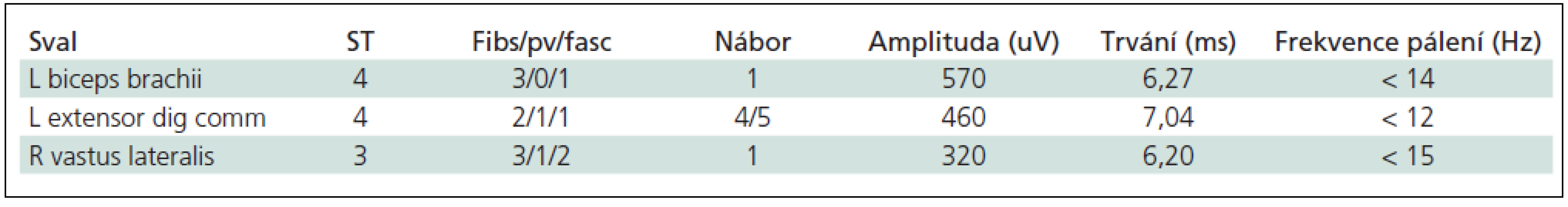
EMG byly nalezeny velmi četné fibrilace, pozitivní vlny, místy fascikulace. Akční potenciály motorických jednotek byly převážně užší a nižší, často polyfazické (až 29 %), avšak malá část z nich měla vyšší amplitudu a delší trvání (tab. 1). Senzitivní i motorická neurografie vykazovaly normální nález.
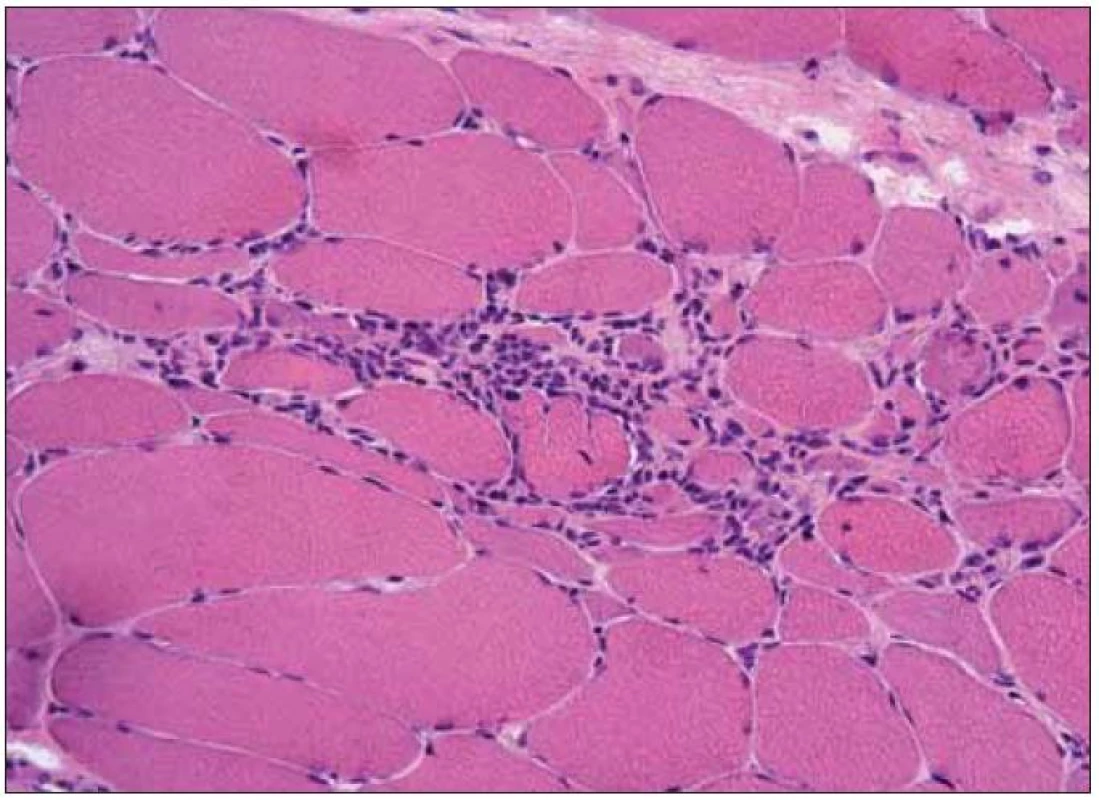
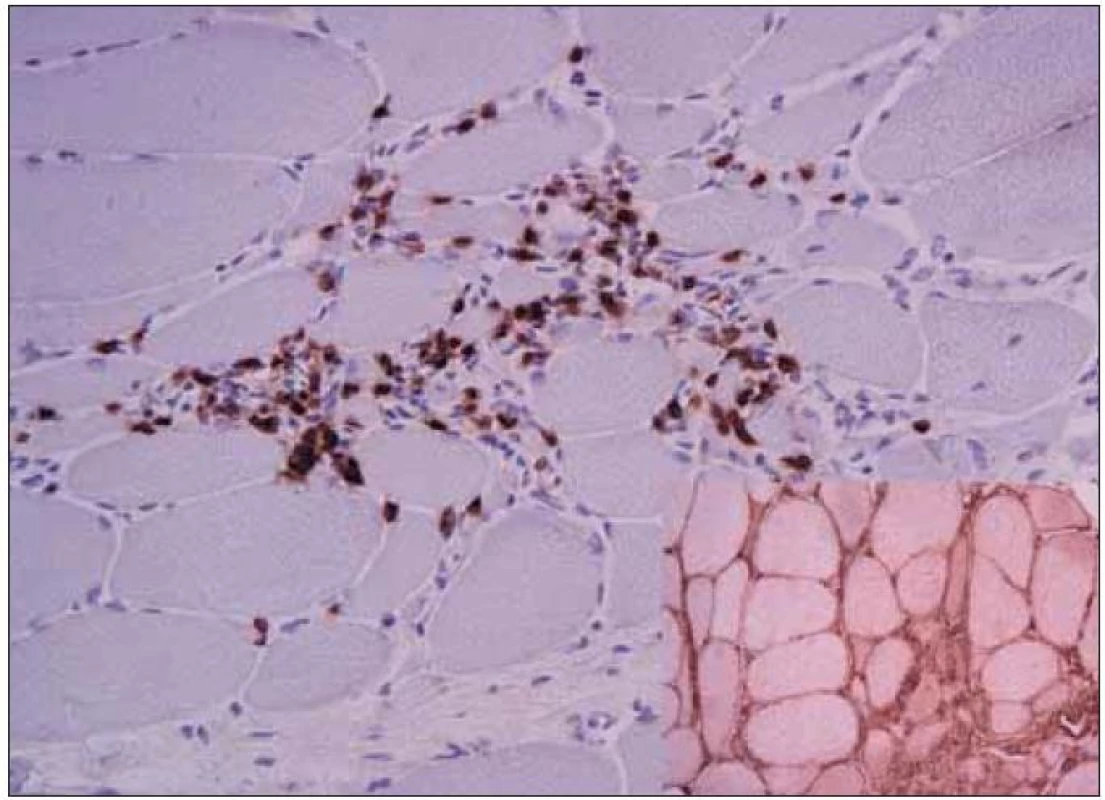
V biopsii m. biceps brachii vpravo byl nalezen myozitický vzorec změn s fokální endomyziální CD8+ lymfocytární infiltrací při silné difuzní expresi HLA-1 na povrchu. IBM-inkluze při elektronmikroskopickém vyšetření nebyly nalezeny. Biopsie svědčila pro polymyozitidu (obr. 1, 2).
Při urologickém vyšetření zjištěna zvětšená prostata a provedena punkční biopsie prostaty. Byl diagnostikován karcinom prostaty s následnou urologickou operační i medikamentózní léčbou. Terapie polymyozitidy byla zahájena intravenózní aplikací metylprednizolonu (1 g po pět dnů) s následným perorálními podáváním prednizonu v denní dávce 80 mg. Po třech týdnech došlo k poklesu hladiny kreatinkinázy a prednizon bylo možno postupně redukovat až na 30 mg obden. Došlo k podstatnému zlepšení myopatického syndromu, a to zejména slabosti šíjových svalů, polykání, abdukce paží. Nemocný velmi dobře toleroval léčbu karcinomu prostaty (operaci i chemoterapii) a po stabilizaci již nedošlo k dalšímu zhoršení myopatického nálezu. Nemocný je sledován praktickým lékařem a neurologem.
Diskuze
Klinický nález s bolestmi svalů, přepadáním hlavy, dysfagií, dysartrií, opakovanou aspirací a kořenovou slabostí zejména horních končetin je charakteristický pro myogenní poruchu [5,7,8]. Může se však vyskytovat i u neurogenních lézí, zvláště ALS či některých neuropatií (CIDP, chronická zánětlivá demyelinizační polyneuropatie). Přepadání hlavy (dropped-head syndrome) se vyskytuje u mnoha chorob a je předmětem rozsáhlé diferenciální diagnostiky (tab. 2). Bývá spojeno s dysartrií, dysfagií a následně i s epizodami aspirace, infektů dýchacích cest i úbytku hmotnosti [9]. U našeho nemocného se nejprve objevily bolesti svalů a po dvou měsících nárůst svalové slabosti s přepadáním hlavy, dysfagií a dysartrií. Nález při jehlové EMG nebyl jednoznačně myogenní (převážně užší a nižší MUP, ale některé s vyšší amplitudou a prodlouženým trváním; přítomnost fascikulací), takže jsme v rámci diferenciální diagnostiky zvažovali i kombinaci s neurogenním postižením (motoneurony, axonální neuropatie) a diagnózu IBM (myopatie s inkluzními tělísky). Na podkladě biopsie svalu byla diagnostikována polymyozitida s endomyziálními infiltráty CD8+ T lymfocytů a difuzní expresí HLA-1 na povrchu svalových vláken.

Dosud byl popsán paraneoplastický syndrom přibližně u 100 nemocných s karcinomem prostaty. Většinou byl diagnostikován u nemocných s agresivní formou karcinomu prostaty a v pokročilém stadiu. Přitom ve více než 70 % byl paraneoplastický syndrom také iniciálním příznakem nádorového procesu a pouze u více než 20 % se jednalo o nemocné již s dříve diagnostikovaným karcinomem prostaty [10]. V dostupné literatuře byly popsány čtyři případy polymyozitidy u karcinomu prostaty, z nichž tři byly hodnoceny jako paraneoplastické syndromy a jeden jako sekundární – ve vztahu k léčbě nádoru acetátem leuprolidu. U dvou nemocných byla diagnóza stanovena na podkladě biopsie svalu [11–14]. Paraneoplastické poruchy kosterního svalu je možno rozdělit do dvou skupin. Polymyozitida se vyskytuje zřídka, má rychlou progresi, postiženy jsou převážně proximálně lokalizované svaly, symetricky, rozvoj je krátký (2–3 měsíce). Je zvýšená kreatinkináza a vyskytuje se malobuněčného karcinomu plic, karcinomu prsu, adenokarcinomu gastrointestinálního traktu [4,15,16]. U dermatomyozitidy stále probíhá diskuze, zda se jedná o pravý paraneoplastický syndrom. Je sdružena s výskytem anti-Jo-1 protilátek [8,15]. Primární je angiopatie svalových arterií vzniklá mechanizmem působení protilátek. Vyskytuje se u adenokarcinomů (ovaria, plic, pakreatu, žaludku, kolorektálního) a non-hodgkinských lymfomů [2,6,17]. Biopsie svalu našeho nemocného prokázala endomyziální CD8+ lymfocytární infiltráty při silné difuzní expresi HLA-1 na povrchu. Klinický obraz s přepadáním hlavy, rychlou progresí, přítomnost anti-Ri protilátek, vysoké hladiny kreatinkinázy i biopsie svalu svědčily pro paraneoplastickou polymyozitidu.
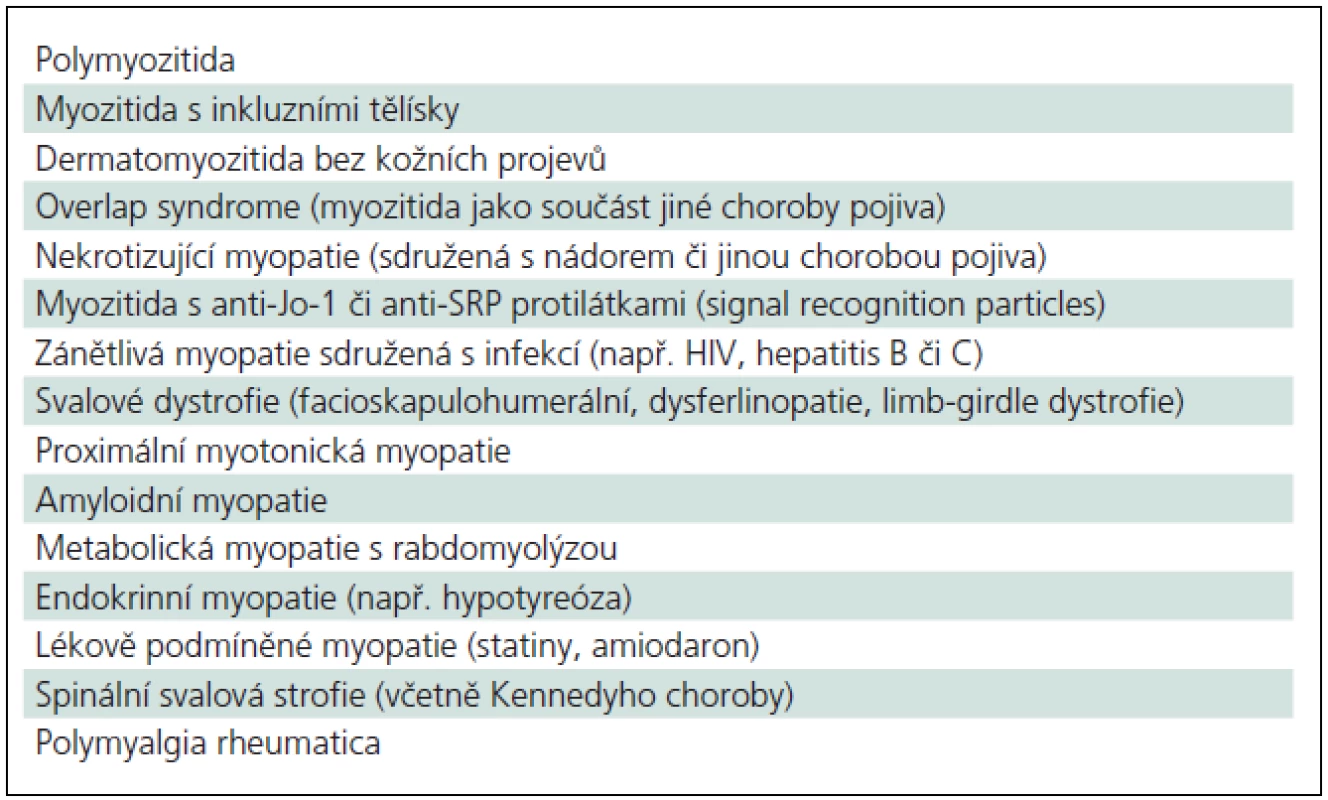
Polymyozitida je diagnostikována na podkladě klinického obrazu, laboratorního nálezu (vyšší ALT, AST, několikanásobně CK, event. volný myoglobin v séru, aldoláza), svalové biopsie a EMG nálezu. Stanovení přesné diagnózy polymyozitidy vyžaduje nejen vyhodnocení svalové biopsie, ale rovněž aktivní vyloučení jiných příčin klinického syndromu (tab. 3) [7,18].
Elektromyografické nálezy u akutní polymyozitidy se u 60–100 % nemocných vyznačují spontánní aktivitou s fibrilacemi, pozitivními vlnami a komplexními repetitivními výboji. Vysoká frekvence fibrilací a pozitivních vln je dle Oha [19] nápadným a charakteristickým rysem akutní polymyozitidy. Akční potenciály motorických jednotek (MUP) jsou krátké, mají nízkou amplitudu a častou jsou polyfázické. Tyto „myogenní MUP“ se vyskytují u 89–100 % nemocných a vyznačují se rychlým náborem; sval má malou sílu kontrakce a přitom se rychle zapojuje velké množství malých jednotek. Je však charakteristické, že tyto MUP mají v počátečních fázích polymyozitidy normální frekvenci a že nedochází ke zrychlení tvorby výbojů motoneuronů („frekvence pálení“) jako odpověď na nízkou sílu kontrakce svalu. Až u pokročilé polymyozitidy se sníží časný nábor MUP, protože se více zapojují ty motoneurony, které se vyznačují rychlou stimulací („mají vyšší frekvenci pálení“) [4,20]. Pro chronickou polymyozitidu je charakteristické i delší trvání MUP s asynchronií MUP [21]. U těžkých polymyozitid dochází až k výpadku celých motorických jednotek [9]. EMG nález našeho nemocného byl charakterizován difuzní přítomností fibrilací, pozitivních vln i fascikulací. Přitom menší část MUP byla polyfázická a měla vyšší amplitudu, větší část spíše myogenní – krátkého trvání s nízkou amplitudou. EMG nález nebyl charakteristický pro myogenní lézi. Na podkladě EMG jsme uvažovali i o kombinaci s neurogenní či míšní poruchou. Nález fibrilací i pozitivních vln byl ekvivalentem léze membrány svalových vláken, tedy akutní a těžká léze svalových vláken.
Při komplexním pátrání po původu polymyozitidy jsme diagnostikovali karcinom prostaty (PSA i biopsie prostaty, scintigrafie skeletu). Vztah mezi nádorem a rozvojem svalových změn je zprostředkován protilátkami [4,18,22]. V terapii paraneoplastické polymyozitidy se zdůrazňuje jak rychlý a výrazný efekt pulzu kortikoidů, tak i efekt léčby vlastního nádoru prostaty na tíži myopatického syndromu [1,9,14]. My jsme prokázali anti-Ri protilátky v likvoru. Po intravenózním podání 5 g metylprednizolonu s navazující perorální kortikoterapií došlo k výraznému zlepšení hybnosti, včetně zlepšení držení hlavy, poruchy polykání, abdukce paží. I když byl nemocný v předchorobí léze statiny, tyto léky byly vysazeny bez podstatnějšího zlepšení hybnosti. Naopak po zavedení kortikoterapie a zejména po zahájení léčby karcinomu prostaty se svalová síla podstatně zlepšila.
Závěr
U 71letého muže s bolestmi svalů, postupným rozvojem poruch polykání, dysartrií, přepadáním hlavy dopředu a oslabením paží jsme diagnostikovali polymyozitidu. Vzhledem k tomu, že jsme prokázali karcinom prostaty a k tomu i paraneoplastické protilátky (anti-Ri) v likvoru, jsme přesvědčeni, že se jednalo o polymyozitidu paraneoplastického původu. Toto naše podezření bylo potvrzeno zlepšením klinického nálezu po imunosupresi i po operační léčbě nádoru prostaty. Diagnóza této velmi vzácně se vyskytující polymyozitidy je založena na zhodnocení klinického obrazu, laboratorní aktivity (CK), EMG nálezu a potvrzena a blíže určena biopsií svalu.
MUDr. Jan Latta
Neurologická klinika
FZS UP a Pardubická krajská nemocnice, a.s
Kyjevská 44
530 03 Pardubice
e-mail: janci82@gmail.com
Přijato k recenzi: 2. 5. 2011
Přijato do tisku: 16. 5. 2011
Sources
1. Pelosof LC, Gerber DE. Paraneoplastic syndromes: an approach to diagnosis and treatment. Mayo Clin Proc 2010; 85(9): 838–854.
2. Posner JB. Paraneoplastic syndromes. Neurologic Clinics 1991; 9(4): 919–936.
3. Darnell RB, Posner JB. Paraneoplastic syndromes involving the nervous system. New Engl J Med 2003; 349(16): 1543–1554.
4. Amato AA, Russel JA. Neuromuscular disorders. New York: McGraw Hill Medical 2007.
5. Minisini AM, Pauletto G., Bergonzi P, Fasola G. Paraneoplastic neurological syndrome and breast cancer. Regression of paraneoplastic neurological sensorimotor neuropathy in a patient with metastatic breast cancer treated with capecitabine: a case study and mini-review of the literature. Breast Cancer Res Treat 2007; 105(2): 133–138.
6. Mowzoon N, Flemming KD. Neurology board review: an illustrated study guide. Rochester: Mayo Clinic Scientific Press 2007.
7. Amato AA, Greenberg SD. Inflammatory myopathies. Continuum 2006; 12(3): 140–168.
8. Bednařík J et al. Nemoci kosterního svalstva. Praha: Triton 2001.
9. Dalakas MC, Karpati G. Inflammatory myopathies. In: Karpati G, Hilton-Jones D, Bushby K, Griggs RC (eds). Disorders of voluntary muscles. 8th ed. Cambridge: Cambridge University Press 2010, 427–452.
10. Hong MK, Kong J, Namdarian B, Longano A, Grummet J, Hovens CM et al. Paraneoplastic syndromes in prostate cancer. Nat Rev Urol 2010; 7(12): 681–692.
11. Crayton H, Bohlmann T, Sufit R, Graziano FM. Drµg induced polymyositis secondary do leuprolide acetate (Lupron) therapy for prostate carcinoma. Clin Exp Rheumatol 1991; 9(5): 515–528.
12. Nakanishi S, Hatayama T. Adenocarcinoma of the prostate associated with anti Jo-1 antibody positive polymyositis. Hinyokika Kiyo 2006; 52(4): 289–191.
13. Park Y, Oster MW, Olarte MR. Prostatic cancer with an unusual presentation: polymyositis and mediastinal adenopathy. Cancer 1981; 48(5): 1262–1264.
14. Tembe AG, Ramteke S, Joshi VR, Balakrishnan C. Dermatomyositis/polymyositis associated with malignancy: our experience with ten patients and review of relevant literature. Internat J Rheum Dis 2008; 11(3): 269–273.
15. Dalakas MC. The future prospects in the classification, diagnosis and therapies of inflammatory myopathies: a view to the future from the “bench-to-bedside”. J Neurol 2004; 251(6): 651–657.
16. Levin MI, Mozaffar T, Al-Lozi MT, Pestronk A. Paraneoplastic necrotizing myopathy. Clinical and pathologic features. Neurology 1998; 50(3): 764–767.
17. Suber TL, Casciola-Rosen L, Rosen A. Mechanisms of disease: autoantigens as clues to the pathogenesis of myositis. Nat Clin Pract Rheumatol 2008; 4(4): 201–209.
18. Dankó K, Ponyi A, Molnar AP, András C, Constantin T. Paraneoplastic myopathy. Curr Opin Rheumatol 2009; 21(6): 594–598.
19. Oh SJ. Clinical electromyography. Case studies. Baltimore: Williams & Wilkins 1998.
20. Pourmand R. Immune-mediated neuromuscular diseases. Basel: Karger 2009.
21. Brown WF, Bolton CF, Aminoff MJ. Neuromuscular function and disease. Philadelphia: W.B. Saunders Company 2002.
22. Hewer E, Goebel HH. Myopathology of non-infectious inflammatory myopathies – the current status. Pathol Res Pract 2008; 204(9): 609–623.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2012 Issue 1
Most read in this issue
- Vertebroplastika – možnost léčby strukturálně narušených obratlů
- Karpální tunel a neurochirurg – zkušenosti po 2 200 operacích
- Kazuistika Guillainova-Barrého syndromu u pacienta s renálním karcinomem
- Klinický standard pro farmakoterapii neuropatické bolesti
