Standardizace české verze The Confusion Assessment Method for the Intensive Care Unit (CAM‑ICUcz)
Standardization of the Czech Version of The Confusion Assessment Method for the Intensive Care Unit (CAM‑ICUcz)
Introduction:
The incidence of delirium in intensive care settings is reported as 62%, and in mechanically-ventilated patients it reaches 82%. Delirium is, however, underdiagnosed because of the non-use of standardised diagnostic tools; no such tool yet exists in the Czech language. The aim was to standardise a Czech version of the most frequently used standard test in the English language – the Confusion Assessment Method for the Intensive Care Unit (CAM-ICU). Patients and method: A Czech version of CAM-ICU (CAM-ICUcz) was prepared by using a “forward-backward translation” method followed by acceptance on the part of the authors of the original test (http://www.icudelirium.org/docs/CAM_ICU_training_Czech.pdf). The assessment of CAM-ICUcz validity to detect delirium, compared with the expert assessment based on standard criteria for delirium of the Diagnostic and Statistical Manual of mental disorders (DSM IV), was performed in patients with: A. Acute cerebral stroke: n = 80; B. Mechanical ventilation: n = 10; C. Dementia: n = 34; D. Depression: n = 20; E. Schizophrenia: n = 22. Results: The expert assessment found an episode of delirium in 37 stroke patients (46.25%). The sensitivity and specificity of CAM-ICUcz were 97.3% and 93.0% respectively. All three patients with false positive for delirium due to CAM-ICUcz had severe aphasia of the global or Wernicke type. The test was performable even in mechanically ventilated patients, with delirium detected in 50% of patients and 100% concordance with the expert assessment. CAM-ICUcz was negative in all patients with dementia, depression and schizophrenia (specificity 100%). The test appeared to be quick (duration up to 10 minutes) and applicable by health care workers not specialised in neuropsychological testing in intensive care patients, including those mechanically ventilated. Conclusion: CAM-ICUcz is a suitable screening test for detection of delirium in the intensive care setting.
Key words:
delirium – intensive care – screening
Authors:
A. Mitášová 1; J. Bednařík 1; M. Košťálová 1; R. Michalčáková 1; M. Ježková 1; T. Kašpárek 2; S. Skutilová 1; E. Straževská 3; P. Šályová 4; V. Šikolová; L. Šrámková
Authors‘ workplace:
Neurologická klinika LF MU a FN Brno
1; Psychiatrická klinika LF MU a FN Brno
2; Klinika anesteziologie, resuscitace a intenzivní medicíny LF MU a FN Brno
3; LF MU
4
Published in:
Cesk Slov Neurol N 2010; 73/106(3): 258-266
Category:
Original Paper
Overview
Úvod:
Incidence deliria v podmínkách intenzivní péče dosahuje 62 % a u nemocných s umělou plicní ventilací až 82 %. Delirium je však poddiagnostikované pro nepoužívání standardizovaných diagnostických nástrojů; v českém jazyce takový standardizovaný test není dosud k dispozici. Cílem studie bylo standardizovat českou verzi nejčastěji používaného standardizovaného testu v angličtině – The Confusion Assessment Method for the Intensive Care Unit (CAM‑ICU). Soubory a metodika: Česká verze CAM‑ICU (CAM‑ICUcz) byla přeložena metodou „forward‑ backward translation“ a akceptována tvůrci originálního testu (http:/ / www.icudelirium.org/ docs/ CAM_ICU_training_Czech.pdf). Stanovení validity CAM‑ICUcz v detekci přítomnosti deliria oproti zlatému standardu – expertnímu stanovení na základě mezinárodně uznávaných kritérií deliria dle diagnostického a statistického manuálu psychických nemocí (DSM IV) – bylo provedeno u nemocných s: A. Akutní cévní mozkovou příhodou (aCMP) n = 80; B. Umělou plicní ventilací: n = 10; C. Demencí: n = 34; D. Depresí: n = 20; E. Schizofrenií: n = 22. Výsledky: Expertní hodnocení zaznamenalo epizodu deliria u 37 nemocných s aCMP (46,25 %). Test CAM‑ICU prokázal senzitivitu 97,3 % a specificitu testu 93,0 %. U všech tří nemocných s falešně pozitivním deliriem dle CAM‑ICUcz šlo o nemocné s těžkou formou globální nebo Wernickeovy afázie. Test byl proveditelný i v podmínkách umělé plicní ventilace, kde jsme zaznamenali delirium u 50 % nemocných a 100% shodu s expertním hodnocením. U žádného z nemocných s demencí, depresí nebo schizofrenií nebyla dle CAM‑ICUcz splněna kritéria deliria (100% specificita). Praktické použití testu prokázalo jeho krátké trvání (do 10 min) a použitelnost zdravotnickými pracovníky – nespecialisty v neuropsychologickém testování u kriticky nemocných včetně umělé plicní ventilace. Závěr: CAM‑ICUcz je vhodný skríningový test pro detekci deliria v intenzivní péči.
Klíčová slova:
delirium – intenzivní péče – skríning
Práce byla vytvořena s podporou grantového projektu IGA MZČR č. NS10216-3/2009 a Výzkumného záměru MŠMT ČR MSM0021622404.
Autoři děkují MUDr. Hynku Sechovskému z Kliniky anesteziologie, resuscitace a intenzivní medicíny 1. LF UK a VFN v Praze za spolupráci při vytvoření definitivní verze CAM-ICUcz.
Data uvedená v této práci byla prezentována na 23. slovenském a českém neurologickém sjezdu v Bratislavě ve dnech 27.–29. 11. 2009 a publikována formou abstraktu v Cesk Slov Neurol N 2009; 72/105 (Suppl 2): S22.
Úvod
Test hodnocení deliria v intenzivní péči (The Confusion Assessment Method for the Intensive Care Unit – CAM‑ICU) byl vytvořen a standardizován skupinou z Vanderbilt University v Nashvillu (USA) pod vedením dr. Ely [1– 4]. Byl adaptován z dosud nejčastěji používaného standardizovaného nástroje pro detekci deliria odborníky mimo psychiatrii – The Confusion Assessment Method (CAM) [5], vytvořeného dr. Inouye z Yale University, ta spolupracovala i na vývoji CAM‑ICU.
V českém jazyce neexistuje dosud žádný standardizovaný skríningový test použitelný k diagnostice deliria v podmínkách intenzivní péče.
Cílem práce bylo
- Vytvořit českou verzi CAM‑ICU akceptovanou tvůrci originálního testu v anglickém jazyce.
- Po zácviku provést validaci české verze CAM‑ICU
(CAM‑ICUcz) vyšetřením souboru nemocných:
- se stavy/ onemocněními, které diferenciálně diagnosticky napodobují delirium: demencí, depresí, schizofrenií,
- s cévní mozkovou příhodou, hospitalizovaných na jednotce intenzivní péče pro ohrožení či poruchu vitálních funkcí a
- se selháním ventilace (léčených umělou plicní ventilací).
K stanovení senzitivity, resp. specificity testu bylo u všech nemocných jako zlatý standard přítomnosti deliria použito hodnocení skupinou expertů na základě kritérií deliria dle diagnostického a statistického manuálu mentálních chorob Americké psychiatrické asociace (revidovaná verze IV z roku 2000) [6].
Soubor a metodika
A. ACE-R
Osmdesát nemocných s akutní cévní mozkovou příhodou (CMP) charakteru intracerebrálního hematomu (ICH) nebo mozkového infarktu ve věku 78 (medián), 37– 93 (rozptyl), 41 mužů a 39 žen, s tíží neurologického deficitu dle National Institute of Health Stroke Scale (NIHSS) ≥ 5. Hodnocení přítomnosti demence před CMP bylo provedeno pomocí skríningového dotazníkového testu Blessed Dementia Scale (BDS) [10]. Premorbidně šlo o pravděpodobnou demenci u 18 nemocných (22,5 %). Hodnocení přítomnosti afázie bylo provedeno prostřednictvím logopedického vyšetření logopedem- afaziologem, kvantifikace deficitu byla provedena 3. a 7. den pomocí škály MASTcz [11,12].
B. Umělá plicní ventilace
Deset nemocných s nutností umělé plicní ventilace (UPV) minimálně po dobu tří dnů ve věku 61,5 (medián), 26– 67 dnů (rozptyl), 9 mužů, 1 žena. Příčinou selhání ventilace bylo 4× plicní onemocnění, 2× kardiální onemocnění, 2× šlo o komplikaci chirurgického zákroku mimo nitrolební prostor, 1× šlo o polytrauma bez postižení mozku, 1× o sepsi bez jasného zdroje, 1× Guillainův‑Barréův syndrom; sepse byla přítomna v době selhání ventilace u čtyř nemocných.
C. Demence
Třicet čtyři nemocných s klinickou diagnózou demence (splňující diagnostická kritéria demence dle MKN- 10 a Diagnostického a statistického manuálu DSM- IV) [6,7] ve věku 71 (medián), 41– 84 (rozptyl) let, 17 mužů a 17 žen. Tíže kognitivního deficitu byla kvantifikována pomocí Adenbrookského kognitivního testu – ACE-R [8,9]. Průměrná hodnota ACE-R byla 56 (medián), 4– 82 (rozptyl) bodů.
Etiologicky šlo o Alzheimerovu demenci (AD) u 14 nemocných; vaskulární demenci (VD) u sedmi nemocných, demence u Parkinsonovy nemoci u sedmi nemocných, u jednoho nemocného šlo o smíšenou demenci (AD + VD), frontotemporální demenci a progresivní supranukleárníobrnu.
D. Deprese
Dvacet nemocných, akutně přijímaných k hospitalizaci pro rozvoj depresivní epizody v rámci depresivní poruchy (splňující diagnostická kritéria dle 10. revize Mezinárodní klasifikace nemocí deprese) ve věku 57 (medián), 22– 80 (rozptyl) let, 10 mužů a 10 žen.
E. Schizofrenie
Dvacet dva nemocných, akutně přijímaných k hospitalizaci pro akutní exacerbaci schizofrenního onemocnění (dle kritérií MKN‑ 10) [7] ve věku 29,5 (medián), 18– 63 (rozptyl) let, 10 mužů a 12 žen.
Test CAM‑ICUcz
Hodnocení deliria je dvoustupňové: prvním krokem je hodnocení stupně vigility (bdělosti) a agitovanosti pomocí validované škály The Richmond Agitation and Sedation Scale (tab. 1) [3,4]. Jde o jednoduchou 10stupňovou škálu hodnotící úroveň vigility (bdělosti) – tedy kvantitativní složku vědomí, a úroveň psychomotorické aktivity, resp. sedace (pacienti v intenzivní péči jsou prakticky obligátně tlumeni sedativně působícími farmaky). Fyziologická úroveň je skórována stupněm „0“, hodnoty se znaménkem + (1– 4) představují hyperaktivitu (agitovanost) a typicky se nacházejí u hyperaktivní formy deliria. Snížení vigility je hodnoceno pěti stupni se znaménkem – ; stupně 1– 3 odpovídají somnolenci různého stupně, pacient reaguje na slovní podnět a lze jej potenciálně dále testovat na přítomnost deliria. Stupeň – 4 (otevření očí či pohyb na fyzický kontakt) a – 5 (bez reakce na fyzický kontakt) odpovídají hlubší poruše vědomí (sopor – kóma) a pacienta nelze dále testovat na přítomnost deliria.
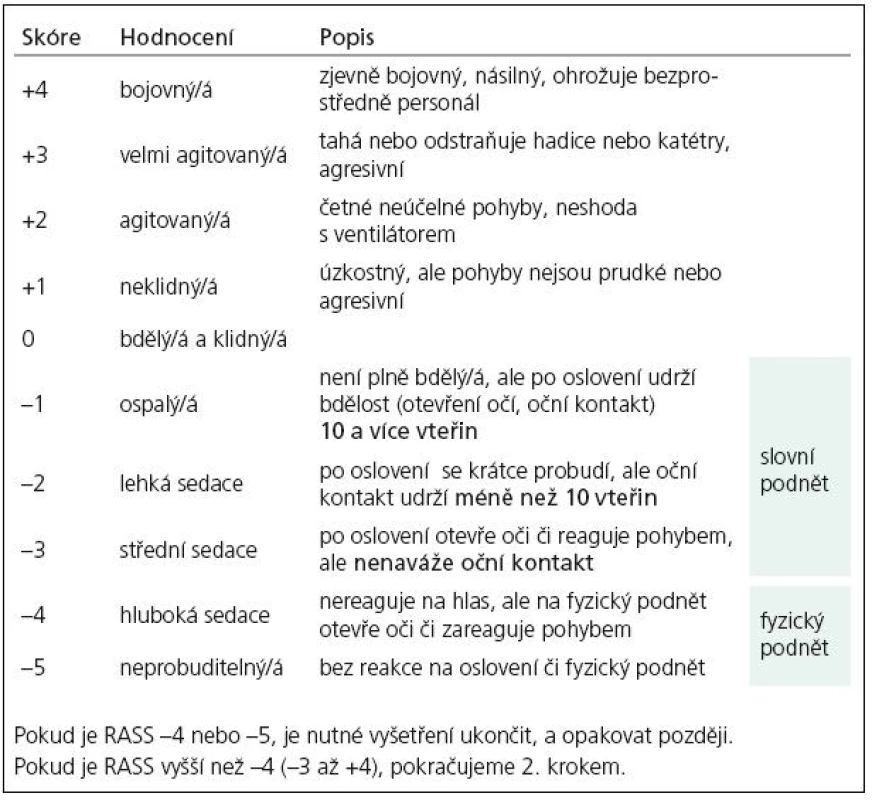
U sedovaných nemocných (zejména nemocných na umělé plicní ventilaci, kteří jsou prakticky vždy sedováni) je důležité načasování vyšetření a snížení sedace v období 1– 2 hod před testováním, pokud to umožňuje stav nemocného.
Druhým krokem testu CAM‑ICU je hodnocení vlastní přítomnosti deliria. Vychází z kritérií deliria dle Americké psychiatrické asociace [6] a je konstruován tak, že pozitivita deliria je podmíněna přítomností rychlého nástupu změny vědomí a/ nebo jeho fluktuací (znak 1), přítomností poruchy pozornosti (znak 2) a dále buďto přítomností poruchy myšlení (znak 3), nebo změněnou aktuální úroveň vigility a psychomotorické aktivity odpovídající hodnotě RASS jiné než 0 (znak 4) (tab. 2). V tab. 3 je pracovní zápis testu CAM‑ICUcz.
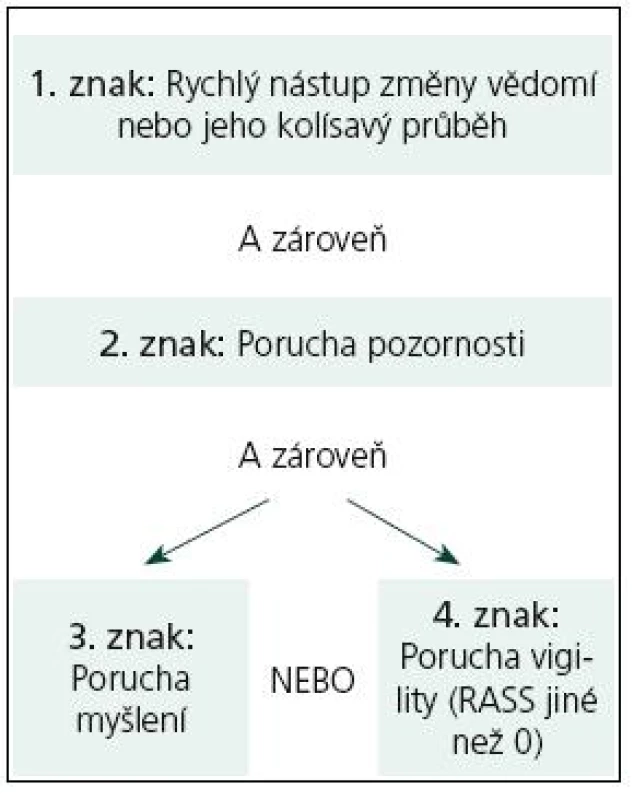

Test CAM‑ICU je konstruován a následně validován pro použití lékařem i sestrou u pacientů v podmínkách intenzivní péče včetně nemocných na umělé plicní ventilaci, kteří často nejsou schopni verbální komunikace. Jednoduchost a krátkost testu (po zácviku 5– 10 min) umožňuje kontinuální monitorování pacienta pomocí opakovaného testování (doporučená frekvence je 2– 3krát během 24 hod, tedy v intervalech 8– 12 hod), což zvýší senzitivitu testu zejména s ohledem na záchyt fluktuace vědomí, chování a psychického stavu.
Pozitivita 1. znaku – Rychlý nástup změny vědomí nebo jeho kolísavý průběh – je dán buďto změnou stavu kvality vědomí se souvisejícími změnami chování a psychického stavu oproti výchozímu stavu (tzv. základnímu stavu vědomí), nebo jeho kolísáním v časovém intervalu od minulého hodnocení. Změna je hodnocena oproti výchozímu stavu („základní stav vědomí“) na začátku sledování. U pacientů hospitalizovaných na jednotce intenzivní péče (JIP) je nutné často výchozí stav vědomí zjišťovat retrospektivně ze všech dostupných zdrojů. Pokud nejsou informace dostupné, řídíme se předpokladem, že u pacienta do 65 let bez anamnézy neurokognitivního onemocnění odpovídá výchozí stav hodnotám RASS = 0 a Glasgowské škály kómat (GCS) = 15. V rámci hodnocení změny či fluktuace hodnotíme nejen úroveň vědomí hodnocenou škálami jako RASS nebo GCS, ale i chování a psychický stav pacienta. Výchozí stav vědomí může být trvale změněn onemocněním, které je příčinou přijetí na JIP (například cévní mozkovou příhodou nebo kraniocerebrálním traumatem) a pak považujeme za základní stav vědomí tento změněný stav. Při opakovaném hodnocení pak používáme stále stejný výchozí stav vědomí jako východisko k hodnocení jeho změny. Změnu způsobenou akutním onemocnění je však obtížné při prvním hodnocení odlišit od změny způsobené případným rozvojem deliria, a proto je lépe při hodnocení znaku 1 použít kritérium fluktuace.
Ke zhodnocení přítomnosti poruchy pozornosti (znak 2) se používá sluchová a/ nebo zraková verze tzv. Attention Screening Examination (ASE) (tab. 4). Začíná se sluchovou verzí, která spočívá v identifikaci hlásky A v sérii deseti postupně předčítaných hlásek pomocí stisku ruky. Maximum dosažených bodů je 10, za abnormální je považováno skóre < 8. Pokud pacient není schopen absolvovat sluchovou verzi (např. porucha sluchu) nebo je výsledek nejednoznačný, pokračuje se zrakovou verzí ASE. K jejímu provedení jsou k dispozici dvě standardní sady deseti obrázků (sada A a B), které se při opakování testu střídají. Pacientovi je předloženo pět náhodně vybraných obrázků použité sady s výzvou, aby si je zapamatoval, a následně je jeho úkolem je identifikovat v kompletní sadě deseti obrázků (abnormální je skóre < 8 z 10 možných bodů).

Přítomnost poruchy myšlení (znak 3) je zjišťována dvěma kroky: sérií čtyř jednoduchých otázek a odpovědí typu ano/ ne (k dispozici jsou dvě sady A a B, které se při opakování střídají) – 3A, a jednoduchým příkazem, kdy pacient je vyzván, aby zopakoval to, co mu předvede vyšetřující – vztyčení dvou prstů jedné ruky – a poté zopakování téhož druhou rukou (nebo – pokud je porucha hybnosti druhostranné končetiny – vztyčení jednoho prstu navíc na téže ruce) – 3B. Sčítá se skóre z obou kroků, maximum je 4 + 1 = 5 bodů, abnormální je < 4 z 5 možných bodů).
Přítomnost poruchy vigility a psychomotorické aktivity (znak 4) je dána hodnotou aktuálního RASS skóre jinou než 0.
Hodnocení přítomnosti deliria
Přítomnost deliria byla u všech nemocných vyšetřena jednak skupinou expertů (neurolog, psychiatr, psycholog, logoped) a jednak pomocí testu CAM‑ICU (vyšetření prováděl psycholog, logoped nebo neurolog). Expertní hodnocení proběhlo na základě zhodnocení aktuálního klinického stavu a veškeré dostupné dokumentace (dekurzy, vyhodnocení stavu nemocného a jeho změn ošetřujícím lékařem a sestrou) a konsenzu celé expertní skupiny, vždy v intervalu 24 hod. Test CAM‑ICU byl vyhodnocen psychologem, logopedem nebo neurologem, rovněž v intervalu 24 hod, a to zaslepeně k výsledku hodnocení expertní skupiny. Před zahájením studie předcházela 3měsíční epizoda, kdy se testující investigátoři nejprve seznámili s testem teoreticky a podíleli se rovněž na vytvoření jeho české verze. Následně pak vyšetřili každý zkušebně minimálně pět nemocných a poté bylo deset nemocných vyšetřeno vždy zaslepeně dvěma investigátory a výsledky porovnány. Vyšetřování nemocných zařazených do studie bylo zahájeno po dosažení shody v hodnocení jednotlivými investigátory.
Skupina nemocných s demencí, depresí a schizofrenií byla vyšetřena jednorázově se zhodnocením 24hodinového intervalu. Skupina nemocných na umělé plicní ventilaci byla hodnocena ve 24hodinových intervalech ve třech po sobě následujících dnech. Skupina nemocných s CMP byla hodnocena prvních sedm dnů od přijetí na jednotku intenzivní péče nebo iktovou jednotku a zařazení do studie. Pokud byly poslední dva dny bez deliria, bylo sledování ukončeno, v opačném případě bylo ve sledování pokračováno až do zjištění dvou po sobě následujících dnů bez deliria.
Výsledek testu CAM‑ICU byl porovnán s výsledkem expertního hodnocení (které bylo použito jako zlatý standard) a vyjádřen jako senzitivita a specificita testu.
Výsledky
Autoři provedli český překlad anglické verze CAM‑ICU metodou forward- backward translation (test přeložen do češtiny a nezávislým překladatelem zpět do angličtiny, obě verze byly porovnány, rozdíly konzultovány s dr. Ely a definitivní česká verze byla umístěna na webových stránkách ICU Delirium and Cognitive Impairment Study Group (www.ICUdelirium.org). První česká verze byla vytvořena v roce 2005 dr. Sechovským, revidovaná verze z r. 2009 byla upravena ve spolupráci s brněnskou skupinou (http:/ / www.icudelirium.org/ docs/ CAM_ICU_training_Czech.pdf) [13].
Cévní mozková příhoda
Expertní hodnocení zaznamenalo epizodu deliria u 37 nemocných (46,25 %). Průměrná doba trvání deliria byla 5 (medián), 1– 28 (rozptyl) dnů. Distribuce výskytu deliria v čase je vyjádřena v grafu 1. Delirium se rozvinulo během 1.– 4. dne od vzniku CMP, u 25 nemocných nastalo během prvních 24 hod od vzniku CMP (67,6 %).

Z celkového počtu 222 dnů s deliriem bylo 99 dnů hodnoceno jako hypoaktivní forma deliria (44,6 %), 47 dnů jako forma hyperaktivní (21,2 %) a 76 jako forma smíšená (tj. během 24 hod se vystřídaly projevy hypo‑ a hyperaktivní formy – 34,2 %). U 6 nemocných (16,2 % pacientů s deliriem) šlo o čistě hypoaktivní formu deliria, u 4 nemocných (10,8 %) o čistě hyperaktivní formu deliria.
Přítomnost pravděpodobné demence před CMP byla zaznamenána pomocí BDS u 22,5 % nemocných s CMP, ani u jednoho však nedošlo k nesouladu mezi expertním hodnocením přítomnosti deliria a výsledkem CAM‑ICU.
Afázie byla přítomna u 33 nemocných (41,2 %) s CMP.
Test CAM‑ICU zachytil výskyt deliria u 36 z 37 nemocných s deliriem, stanoveným expertním hodnocením, což odpovídá senzitivitě 97,3 %.
Test CAM‑ICU vykázal normální výsledek testu u 40 z 43 nemocných bez přítomnosti deliria dle expertního hodnocení, což odpovídá specificitě testu 93,0 %.
Neshody mezi CAM‑ICU a expertním hodnocením
U jednoho nemocného byl test CAM‑ICU falešně negativní (pac. č. 66). Šlo o nemocného, který měl výrazné kolísání stavu vědomí a chování s porušeným rytmem spánku a bdění, psychomotorickým neklidem a dezorientací v nočních hodinách. Při hodnocení CAM‑ICU standardně v dopoledních hodinách (event. při výrazné somnolenci v hodinách odpoledních) však pacient nesplnil kritérium abnormality ve znaku 2 (hodnocení poruchy pozornosti – výsledky testu ASE byly normální).
U třech nemocných byl test CAM‑ICU falešně pozitivní. U všech šlo o pacienty s lézí levé dominantní hemisféry manifestující se globální nebo Wernickeovou afázií se skóre MASTcz < 20 (3. i 7. den). U všech třech nemocných byla splněna kritéria pozitivity znaku 2 (porucha pozornosti) a znaku 3 (porucha myšlení), i když vzhledem k afázii nebylo možno rozlišit podíl poruchy porozumění na abnormálním výsledku testu. Kritérium pozitivního znaku 1 (náhlá změna stavu nebo jeho kolísání) bylo splněno pouze v den 1, kdy nemocní vesměs byli neklidní, úzkostní, snažili se opouštět lůžko, od 2. dne již kritérium pozitivity znaku 1 splněno nebylo.
Umělá plicní ventilace
Pozitivitu testu CAM‑ICUcz jsme zaznamenali u šesti nemocných (60 %). Shoda s expertním hodnocením přítomnosti deliria byla 100 % (tedy senzitivita i specificita byly 100 %). Vyšetření bylo proveditelné u všech testovaných pacientů, pokud byla míra sedace v době testování snížena na minimum.
Demence, deprese, schizofrenie
Pozitivitu testu CAM‑ICU jsme u celkem 76 pacientů s těmito diagnózami nezaznamenali, což představuje specificitu testu 100 %. V tab. 5 jsou shrnuty výsledky hodnocení jednotlivých znaků testu v této podskupině nemocných. Znak 1 (Změna či kolísání stavu) byl pozitivní u některých pacientů se schizofrenií a depresí, znak 2 (Porucha pozornosti) a 3 (Porucha myšlení) byly naproti tomu pozitivní v převážné většině u nemocných s demencí.
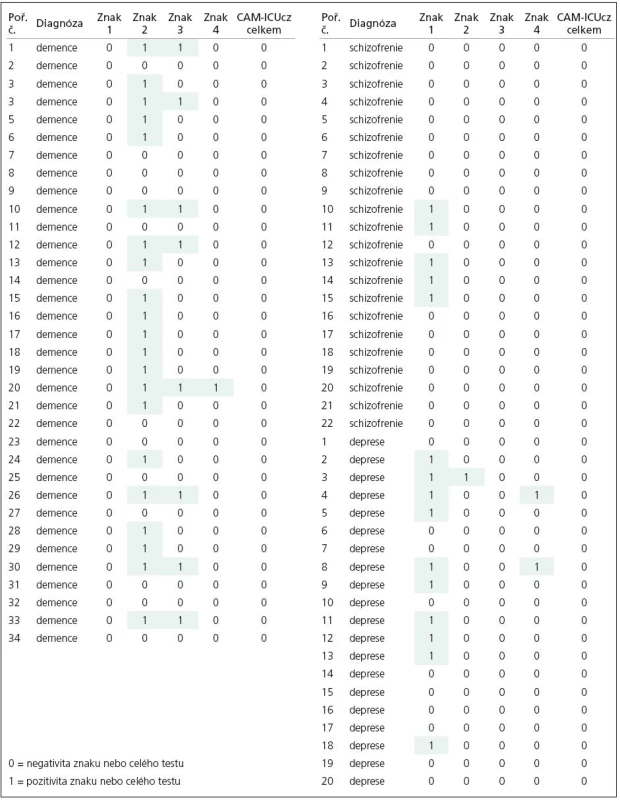
Trvání a proveditelnost testu
Praktické zkušenosti s aplikací CAM‑ICUcz potvrdily, že test může po předchozím zácviku administrovat zdravotnický pracovník s lékařským i nelékařským vzděláním bez erudice v neuropsychologickém testování. Jde relativně krátký test trvající obvykle 5, maximálně 10 minut. Pokud jsou splněna kritéria proveditelnosti testu (absence hlubší kvantitativní poruchy vědomí a možnost jednoduché komunikace), je použitelný i u kriticky nemocných včetně pacientů na umělé plicní ventilaci.
Diskuze
Prospektivní studie ukázaly, že incidence deliria v intenzivní péči dosahuje až 62 % a u mechanicky ventilovaných pacientů až 82 % [14,15]. Delirium je nezávislým prediktorem delšího pobytu v nemocnici a zvýšené 6měsíční mortality [15]. Ekonomicky přináší delirium zvýšení nákladů na intenzivní péči o 37 %, celkovou nemocniční péči o 31 % a představuje významný nárůst zátěže zdravotnických pracovníků [16,17]. Je spojeno s poruchami chování, které interferují s léčbou: agitovanost, odmítání léčby, nemožnost rehabilitace, pády, fraktury. Asi nejzávažnější je agitovanost, která může vést k poranění nejen pacienta, ale i ošetřujícího personálu, pro nějž navíc představuje tato situace zvýšenou emocionální zátěž. Klinický význam stanovení deliria spočívá i v tom, že je často známkou dosud nedetekovaného onemocnění či poruchy („kanárek v uhelném dole“) [18].
V současnosti je věnována velká pozornost vytváření a standardizaci nástrojů pro detekci deliria v prostředí intenzivní péče. Mezi nejlépe validované a nejvíce rozšířené testy patří CAM‑ICU a dále the Intensive Care Delirium Screening Checklist (ICDSCH) [19]. ICDSCH je poněkud náročnější, má vysokou senzitivitu (99 %), avšak o něco nižší specificitu (64 %). Porovnání obou metod však ukázalo vysokou shodu obou metod (kappa koeficient kolem 0,80) [20], což nepřímo favorizuje jednodušší CAM‑ICU.
Nejnovější reprezentativní průzkum mezi profesionály v oblasti intenzivní péče, publikovaný v roce 2009 [21], ukázal, že většina z nich považuje problematiku deliria za prioritní a je přesvědčena, že tato entita je poddiagnostikována (86 % oslovených odborníků). Je však s podivem, jak málo je toto povědomí přenášeno do klinické praxe. Mírná většina (59 %) provádí pravidelně určitou formu skríningu zaměřeného na detekci deliria u pacientů v intenzivní péči, avšak pouze 33 % používá specifický nástroj pro detekci deliria v podmínkách intenzivní péče (i když jde o zlepšení oproti předchozímu průzkumu publikovaného v roce 2004 [22], kdy to bylo pouze 12 %).
Mezi stavy, které je nutné diferencovat oproti deliriu, patří zejména demence, psychóza a deprese. Naše výsledky ukázaly, že CAM‑ICU má vynikající specificitu oproti těmto stavům: ani u jednoho ze 76 vyšetřených nemocných s jednou z těchto diagnóz nebyla splněna kritéria deliria (tedy specificita testu byla 100 %). Existují samozřejmě situace, kdy bude diferenciace mezi deliriem a těmito stavy obtížná. Je to zejména koincidence deliria s další poruchou, což padá zejména v úvahu u demence, která je dle dosavadních poznatků jedním z významných a častých rizikových faktorů deliria [23– 25]. V našem souboru nemocných s CMP jsme pravděpodobnou demenci pomocí skríningové metody Blessed dementia scale zaznamenali u 22,5 % nemocných s CMP, ani u jednoho však nedošlo k nesouladu mezi expertním hodnocením a výsledkem CAM‑ICU.
Nejvýznamnější překážkou hodnocení přítomnosti deliria pomocí CAM‑ICU (ale i hodnocení dalších kognitivních funkcí) představuje afázie. U tří pacientů s těžkým stupněm globální nebo Wernickeovy afázie s těžkou poruchou porozumění nebylo možné rozlišit, zda porucha pozornosti a myšlení je způsobena deliriem nebo afázií. U tří pacientů byla navíc splněna pozitivita znaku 1, kdy během prvních 24 hod došlo i ke kolísání stavu vědomí a chování – tito pacienti byli úzkostní, často i mírně agitovaní, tyto projevy výrazně kolísaly a do 24 hod ustoupily. Domníváme se, že v těchto případech jde spíše o situačně navozenou alterací psychického stavu, potencovanou ztrátou symbolické komunikace. Tento výskyt úzkosti, neklidu a poruch chování u Wernickeovy afázie je popisován i v logopedické literatuře [26– 28], můžeme spekulovat i o možném podílu ložiskové léze v temporálním laloku dominantní hemisféry.
Případ falešně negativního hodnocení deliria pomocí CAM‑ICU u jednoho nemocného dobře ilustruje další problém diagnostiky deliria, který je i příčinou poddiagnostikování v klinické praxi, a těmi jsou kolísání symptomatiky deliria (jako klíčového symptomu deliria) a jeho záchyt.
Doporučený interval hodnocení CAM‑ICU je 8 hod, což má i praktickou výhodu, neboť odpovídá délce směny sestry JIP. My jsme hodnotili vzhledem k organizační a časové náročnosti (bylo nutné zachovat kontinuitu hodnocení jedním investigátorem u každého pacienta), avšak při hodnocení znaku 1 jsme brali v úvahu průběh stavu pacienta uplynulých 24 hod. Při tomto způsobu hodnocení zůstala senzitivita testu velmi vysoká, až na jeden případ, kdy byl pacient opakovaně hodnocen v době, kdy byly symptomy deliria minimální, a nebyla tak splněna pozitivita znaku 2 a 3. V klinické praxi, zejména pokud bude k dispozici dostatek vyškoleních intenzivistických sester, je možno hodnocení v 8hodinových intervalech doporučit.
V běžné klinické praxi bez použití standardizovaného nástroje na diagnostiku deliria lze předpokládat, že detekci unikají i případy hyperaktivního deliria (manifestujícího se v nočních hodinách), pokud nefunguje dobře systém předávání informací o stavu pacienta a komplexní hodnocení stavu pacienta. Zejména však pozornosti unikají případy čistě či převážně hypoaktivní formy deliria, která v klinické praxi převládá – v našem souboru nemocných s CMP tvořil podíl dnů s čistě hyperaktivní formou deliria 21,2 % všech dnů s deliriem a čistě hyperaktivní forma deliria se vyskytla pouze u čtyř nemocných (10,8 %).
Posledním metodologickým problémem, na který jsme narazili, je hodnocení stavu vědomí v případě farmakologické sedace, zejména pak u pacientů na umělé plicní ventilaci. Pokud jde o pooperační stavy, tak je třeba vyčkat odeznění vlivu sedace. U pacientů s hyperaktivní formou deliria vyžadující nutnost farmakologické sedace může sice následně dojít k překrytí některých symptomů deliria, což však z hlediska diagnózy deliria již nevadí. Pro zhodnocení přetrvávání deliria, a tedy i nutnosti sedace začíná řada intenzivistických pracovišť používat standardní protokol sedace, jehož součástí jsou i pravidelné epizody pokusného odtlumení („daily sedation cessation“, „spontaneous awakening trials“), během kterých je optimální testovat pacienta na přítomnost deliria.
Závěrem lze shrnout:
CAM‑ICU je diagnostický test zaměřený na přítomnost deliria, který je použitelný u nemocných léčených v podmínkách intenzivní péče včetně nemocných na umělé plicní ventilaci.
Jde o test relativně krátký (s dobou provedení obvykle do 5, maximálně 10 min) a určený pro zdravotnické pracovníky, kteří nejsou specialisty v neuropsychologickém testování (včetně zaškolených zdravotních sester).
Validovaná česká verze (CAM‑ICUcz) má vysokou senzitivitu i specificitu jak ve srovnání s expertním hodnocením, tak v diferenciaci oproti demenci, depresi a schizofrenii.
Kvalitní detekce přítomnosti deliria je základem jak dalšího výzkumu zvláště rizikových faktorů deliria, tak v praxi zejména postupů vedoucích k vyloučení ovlivnitelných rizikových faktorů, a v budoucnu i hodnocení efektivity léčebných postupů [29].
prof. MUDr. Josef Bednařík, CSc.
Neurologická klinika LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: jbednar@fnbrno.cz
Přijato k recenzi: 16. 2. 2010
Přijato do tisku: 10. 3. 2010
Sources
1. Ely EW, Inouye S, Bernard G, Gordon S, Francis J, May L et al. Delirium in mechanically ventilated patients: validity and reliability of the confusion assessment method for the intensive care unit (CAM‑ICU). JAMA 2001; 286(21): 2703– 2710.
2. Ely EW, Margolin R, Francis J, May L, Truman B, Dittus B et al. Evaluation of delirium in critically ill patients: Validation of the Confusion Assessment Method for the Intensive Care Unit (CAM‑ICU). Crit Care Med 2001; 29(7):1370– 1379.
3. Sessler CN, Gosnell M, Grap MJ, Brophy GT, O‘Neal PV, Keane KA et al. The Richmond Agitation‑ Sedation Scale: validity and reliability in adult intensive care patients. Am J Respir Crit Care Med 2002; 166(10):1338– 1344.
4. Ely EW, Truman B, Shintani A, Thomason JWW, Wheeler AP, Gordon S et al. Monitoring sedation status over time in ICU patients: the reliability and validity of the Richmond Agitation Sedation Scale (RASS). JAMA 2003; 289(22): 2983– 2991.
5. Inouye SK, van Dyck CH, Alessi CA, Balkin S, Siegal AP, Horwitz RI. Clarifying confusion: the confusion assessment method. A new method for detection of delirium. Ann Intern Med 1990; 113(12): 941– 948.
6. American Psychiatric Association. Diagnostic and statistical manual of mental disorders. 4th ed. Washington, DC: American Psychiatric Association 2000.
7. International Statistical Classification of Diseases and Related Health Problems. 10th rev. 2nd ed. Geneva: WHO 2004. Oficiální český překlad je dostupný z URL: http:/ / www.uzis.cz/ cz/ mkn/ .
8. Mioshi E, Dawson K, Mitchell J, Arnold R, Hodges JR. The Addenbrooke’s Cognitive Examination Revised (ACE‑ R): a brief cognitive test battery for dementia screening. Int J Geriatr Psychiatry 2006; 21(11): 1078– 1085.
9. Hummelová‑ Fanfrdlová Z, Rektorová I, Sheardová K,Bartoš A, Línek V et al. Česká adaptace addenbrookského kognitivního testu. Cesk Psychol 2009; 53(4): 376– 388.
10. Blessed G, Tomlinson BE, Roth M. The association between quantitative measures of dementia and of senile change in the cerebral grey matter of elderly subjects. Br J Psychiatry 1968; 114(512): 797– 811.
11. Kostálová M, Bártková E, Sajgalíková K, Dolenská A, Dusek L, Bednarík J. A standardization study of the Czech version of the Mississippi Aphasia Screening Test (MASTcz) in stroke patients and control subjects. Brain Injury 2008; 22(10): 793– 801.
12. Košťálová M, Bednařík J. Screening afázie: MASTcz. Dostupné z URL: http:/ / www.fnbrno.cz/ Article.asp?nDepartmentID=1355&nArticleID=2298&nLanguageID=1.
13. Bednařík J, Košťálová M, Sechovský H. CAM‑ICU: Czech version [cited 2009 Dec 21]. Dostupné z URL: http:/ / www.icudelirium.org/ docs/ CAM_ICU_training_Czech.pdf.
14. McNicoll L, Pisani MA, Zhang Y, Ely EW, Siegel MD, Inouye SK. Delirium in the intensive care unit: Occurrence and clinical course in older patients. J Am Geriatr Soc 2003; 51(5): 591– 598.
15. Ely EW, Shintani A, Truman B, Speroff T, Gordon SM, Harrell FE Jr et al. Delirium as a predictor of mortality in mechanically ventilated patients in the intensive care unit. JAMA 2004; 291(14): 1753– 1762.
16. Milbrandt EB, Deppen S, Harrison PL, Shintani AK, Speroff T, Stiles RA et al: Costs associated with delirium in mechanically ventilated patients. Crit Care Med 2004; 32(4): 955– 962.
17. Franco K, Litaker D, Locala J, Bronson D. The cost of delirium in the surgical patient. Psychosomatics 2001; 42(1): 68– 73.
18. Caplan JP. Don’t ask, don’t tell: delirium in the intensive care unit. Crit Care Med 2009; 37(3): 1129– 1130.
19. Bergeron N, Dubois MJ, Dumont M, Dial S, Skrobik Y. Intensive Care Delirium Screening Checklist: evaluation of a new screening tool. Intensive Care Med 2001; 27(5): 859– 864.
20. Plaschke K, von Haken R, Scholz M, Engelhardt R,Brobeil A, Martin E et al. Comparison of the confusion assessment method for the intensive care unit (CAM‑ICU) with the Intensive Care Delirium Screening Checklist (ICDSC) for delirium in critical care patients gives high agreement rate(s). Intensive Care Med 2008; 34(3): 431– 436.
21. Patel RP, Gambrell M, Speroff T, Scott T; Pun BT, Okahashi J et al. Delirium and sedation in the intensive care unit: Survey of behaviors and attitudes of 1384 healthcare professionals. Crit Care Med 2009; 37(3): 825– 832.
22. Ely EW, Stephens RK, Jackson JC, Thomason JW, Truman B, Gordon S et al. Current opinions regarding the importance, diagnosis, and management of delirium in the intensive care unit: a survey of 912 healthcare professionals. Crit Care Med 2004; 32(1): 106– 112.
23. Haluzová A, Bednařík J, Košťálová M, Michalčáková R, Voháňka S, Mitáš L. Delirium u pacientů s akutním iktem a u pacientů po operačním zákroku. Cesk Slov Neurol N 2008; 71/ 104 (Suppl 3): S60.
24. Haluzová A, Bednařík J, Košťálová M, Baďurová R, Voháňka S, Jura R. Delirium u pacientů s cévní mozkovou příhodu – epidemiologie a rizikové faktory. Cesk Slov Neurol N 2008; 71/ 104 (Suppl 2): S64.
25. Adunsky A, Levy R, Heim M, Mizrahi E, Arad M. The unfavorable nature of preoperative delirium in elderly hip fractured patients. Arch Gerontol Geriatr 2003; 36(1): 67– 74.
26. Cséfalvay Z. Traubner P. Afaziológia pre klinickú prax. Martin: Osveta 1996.
27. Sarno MT, Levita E. Some observations on the nature of recovery in global aphasia after stroke. Brain Lang 1981; 13(1): 1– 12.
28. Kundrátová M. Metodika obnovovania reči při senzorickej afázii. Diplomová práca. Bratislava: PdF UK 1996.
29. Bednařík J. Neurologické poruchy v rámci kritického stavu. Cesk Slov Neurol N 2008; 71/ 104(5): 511– 529.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2010 Issue 3
Most read in this issue
- Spondylogenní cervikální myelopatie
- Zlomeniny pátého bederního obratle
- Standardizace české verze The Confusion Assessment Method for the Intensive Care Unit (CAM‑ICUcz)
- Komplikovaná herpetická nekrotizující meningoencefalitida s nutností neurochirurgické intervence – kazuistika
