Spánková apnoe dospělého věku
Adult Age Sleep Apnoea
Sleep apnoea is characterised by repeated episodes of interrupted/limited breathing during sleep. Such episodes are either caused by an obstruction in the upper respiratory ways and/or a disorder of the control of breathing during sleep. Obstructive sleep apnoea (OSA) in the adult age is a frequent disease with a prevalence of 2 to 4 %. It is associated with significant cardiovascular comorbidity (hypertension, heart failure, atrial fibrillation, cerebrovascular events – CVE), with metabolic syndrome, and also with a higher rate of occurrence of epileptic manifestations. OSA reduces life expectancy. The negative impact of OSA and its symptoms can be eliminated by effective treatment, especially by Constant Positive Airway Pressure (CPAP). Central sleep apnoea (CSA) including Cheyne Stokes’ respiration rarely occurs as an isolated condition and is often accompanied by heart failure, CMP and kidney failure and worsens the prognosis. The treatment of CSA not only brings improved signs of sleep apnoea, but has a positive effect on the underlying disease. This monograph presents an overview of the basics of OSA and CSA pathophysiology, their diagnosis, comorbidities and treatment options.
Key words:
sleep related breathing disorders obstructive sleep apnoea – central sleep apnoea – polysomnography – constant positive airway pressure – comorbidity
Authors:
K. Šonka 1; J. Slonková 2
Authors‘ workplace:
Univerzita Karlova v Praze, 1. lékařská fakulta a Všeobecná fakultní nemocnice v Praze, Neurologická klinika
1; Neurologická klinika FN Ostrava
2
Published in:
Cesk Slov Neurol N 2008; 71/104(6): 643-656
Category:
Minimonography
Poděkování: Minimonografi e vznikla s podporo u VZ MŠMT 0021620816.
Overview
Spánková apnoe je charakterizována opakovanými epizodami přerušení/ omezení dýchání v průběhu spánku. Tato přerušení jso u vyvolána buď obstrukcemi horních cest dýchacích, a/ nebo porucho u řízení dýchání ve spánku. Obstrukční spánková apnoe (OSA) dospělého věku je časté onemocnění s prevalencí 2– 4 %. Je asoci ována s výrazno u kardi ovaskulární komorbidito u (hypertenze, srdeční selhání, fibrilace síňová, cévní mozkové příhody – CMP), s metabolickým syndromem a také s větším výskytem epileptických projevů. OSA zkracuje dožití. Tyto nepříznivé vlivy OSA a její příznaky eliminuje efektivní léčba, zejména trvalý přetlak v dýchacích cestách (CPAP). Centrální spánková apnoe (CSA) včetně Cheyne– Stokesova dýchání se vzácně vyskytuje samostatně, často však doprovází srdeční selhání, CMP a ledvinné selhání a zhoršuje jejich prognózu. Léčení CSA také nejen přináší zlepšení příznaků spánkové apnoe, ale má příznivý vliv i na vyvolávající chorobu. Tato minimonografi e předkládá přehled o základech patofyzi ologi e OSA a CSA, o jejich di agnostice, o komorbidních so uvislostech a o možnostech léčení.
Klíčová slova:
poruchy dýchání vázané na spánek – obstrukční spánková apnoe – centrální spánková apnoe – polysomnografie – trvalý přetlak v cestách dýchacích – komorbidita
Histori e
Je překvapující, že choroba, která má tak manifestní a dramatické příznaky, jako je bezdeší a silné dechové zvuky, a která je tak rozšířená, čekala na zájem lékařské veřejnosti až do posledních dekád 20. století. Podrobné kazuistiky lidí trpících porucho u dýchání ve spánku se sice objevily v hlavních lékařských časopisech již před 150 lety, ale překvapivě nevedly k vymezení nozologické jednotky. Dokonce v první polovině 20. století jakoby poruchy dýchání ve spánku usto upily z již tak malého zřetele lékařů a většina poruch nočního spánku byla spojována s narkolepsi í a se záněty nebo úrazy nervové so ustavy [1,2].
Moderní histori e znalostí poruch dýchání vázaných na spánek (Sleep Related Bre athing Disorders – SRBD) začíná, i když velmi pomalu a nenápadně, roku 1956, kdy Burwell popsal paci enta se syndromem obezita- hypoventilace a nazval jej pickwickovský syndrom [3] podle knihy Charlese Dickense Klub Pickwickův z roku 1835. Dickens dokonale vylíčil toto onemocnění na tlustém spavém pacholku Joe ovi, jenž měl údajně re álno u předlohu v synovi známého hostinského. Apnoe byly prvně identifikovány až teprve v roce 1965 ne urology Gasta utem et al [4]. Zpočátku byly považovány za další symptom mozkové choroby vyznačující se primárně spavostí. Obstrukční příčina některých apnoí byla odhalena teprve ve druhé polovině 60. let. V této době se poruchám dýchání ve spánku věnovali čeští ne urologové Brůhová-Nevšímalová a Nevšímal [5– 7]. V 70. letech se začal po užívat termín sleep apne a syndrome – syndrom spánkové apnoe [8]; v našem písemnictví to bylo však až ve článku Nevšímala et al z roku 1989 [9]. V 70. letech bylo v USA di agnostikováno větší množství nemocných, většino u se však jednalo o syndrom obezita- hypoventilace v kombinaci s apnoemi. Někteří z nich byli úspěšně léčeni trache ostomi í. Do 70. let spadá také rozdělení dvo u nozologických jednotek – obstrukční spánkové apnoe – OSA a centrální spánkové apnoe – CSA [8]. V roce 1981 byly publikovány dva zásadní a dosud nejpo užívanější terape utické postupy OSA. Konzervativní postup: trvalý přetlak v cestách dýchacích (Continuo us Positive Airway Pressure – CPAP) vymyslel Australan Collin Sullivan se spolupracovníky ze Sydney [10] a chirurgicko u léčbu Američané Fujita et al [11]. Objevy efektivního léčení vedly k praktickému zájmu o OSA. Tento zájem ještě více podnítila zjištění vysoké prevalence OSA a první důkazy nepříznivého vlivu OSA na kardi ovaskulární nemocnost a délku přežití. Posledních 20 let přineslo dramatický nárůst poznatků o SRBD, a zejména OSA – o epidemi ologii, o komorbidních komplikacích, o léčení; a hlavně ne uvěřitelně vzrostl počet úspěšně léčených nemocných.
Klasifikace a základní symptomy
Poslední mezinárodní klasifikace poruch spánku a bdění – ICSD 2 [12] rozlišuje pět základních poruch dýchání vázaných na spánek (tab. 1), ale Mezinárodní klasifikace nemocí MKN 10 definuje po uze dvě onemocnění z oblasti SRBD: G47.3 – zástava dýchání ve spánku (apnoe) a E66.2 – extrémní obezita a alve olární hypoventilace. Různé formy SRBD se moho u u jednoho nemocného kombinovat. Pro praxi je nutné doplnit prosté chrápání (ronchopatii) klasifikovano u ICSD 2 ve skupině samostatných symptomů a vari ant normy.
![Rozdělení poruch dýchání vázaných na spánek dle ICSD 2 [12].](https://www.csnn.eu/media/cache/resolve/media_object_image_small/media/image/57f368fa5b614c4c42532e772b0a7780.png)
Apnoe je přerušení ventilace v trvání 10 s a více. Rozlišuje se obstrukční, centrální a smíšená apnoe. Apnoe je považována za obstrukční, pokud je během jejího trvání přerušeno pro udění vzduchu v horních cestách dýchacích (HCD), ale přetrvává dýchací úsilí hrudníku, a za centrální, jestliže není přítomna žádná dechová aktivita. Apnoe se nazývá smíšeno u, jestliže začíná jako centrální bez dýchacího úsilí, ale dýchací úsilí se během jejího trvání obnoví a končí jako obstrukční.
Hypopnoe je přechodné omezení dechových objemů nejméně o 50 % předcházejících objemů po dobu 10 s a více, které je doprovázeno poklesem saturace o 3 % a více.
Respiratory Effort- Related Aro usal (probuzení navozené dechovým úsilím – RERA) je sekvence dechů trvající 10 s a více charakterizovaná vzrůstajícím respiračním úsilím nebo zmenšováním amplitudy křivky z měření nosního tlaku vedo ucí k probo uzecí re akci. Tento děj přitom nesplňuje kritéri a apnoe ani hypopnoe.
Hypoventilace je nedostatečné dýchání vedo ucí k vzestupu arteri ální koncentrace oxidu uhličitého (PaCO2) nad 45 mmHg [12– 15].
Obstrukční spánková apnoe (OSA, obstrukční syndrom spánkové apnoe, obstrukční spánkový apno ický syndrom) dospělého věku
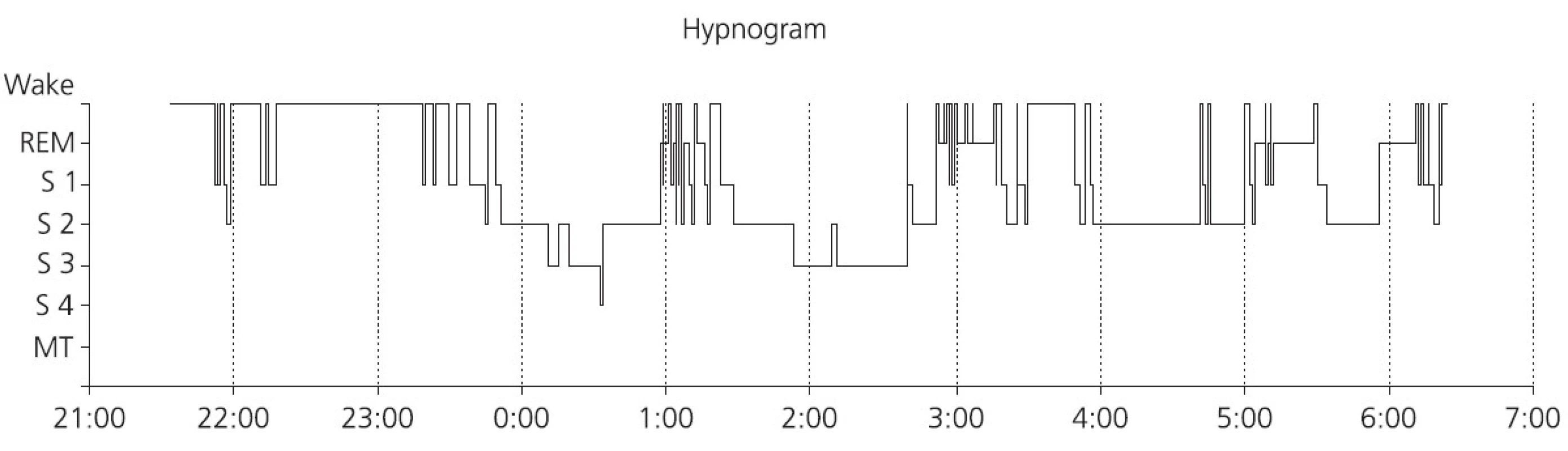
OSA charakterizují opakované epizodyúplné nebo částečné obstrukce HCD vespánku, které vedo u k apnoím nebo k hypopnoím (di agnostická kritéri a, tab. 2). Přestože tato charakteristika je stejná pro OSA v dospělém i dětském věku, existují některé rozdíly v patofyzi ologii a klinických projevech, a proto se rozlišují dvě klinické jednotky: OSA v dospělém a OSA v dětském věku [12]. Apnoe a hypopnoe většino u vyvolávají poklesy saturace hemoglobinu kyslíkem; po obnovení dýchání se saturace obvykle vrací na základní hladinu. Apnoe a hypopnoe jso u většino u ukončeny probo uzecí re akcí (aro usal – elektrofyzi ologické známky bdělosti trvající 3– 15 s) nebo probuzením (známky bdělosti trvající více než 15 s; obr. 1). Opakování probo uzecích re akcí (a probo uzení) fragmentuje noční spánek (obr. 2). Většina apnoí a hypopnoí trvá mezi 20 a 30 s. Objevují se ve všech stadi ích spánku, ale nejčastěji v 1 a 2 NREM a REM. Anamnestické příznaky se dělí na noční a denní.
![Diagnostická kritéria obstrukční spánkové apnoe (OSA) dle ICSD 2 [12].](https://www.csnn.eu/media/cache/resolve/media_object_image_small/media/image/071782d812377955fe82dd321084b53b.png)
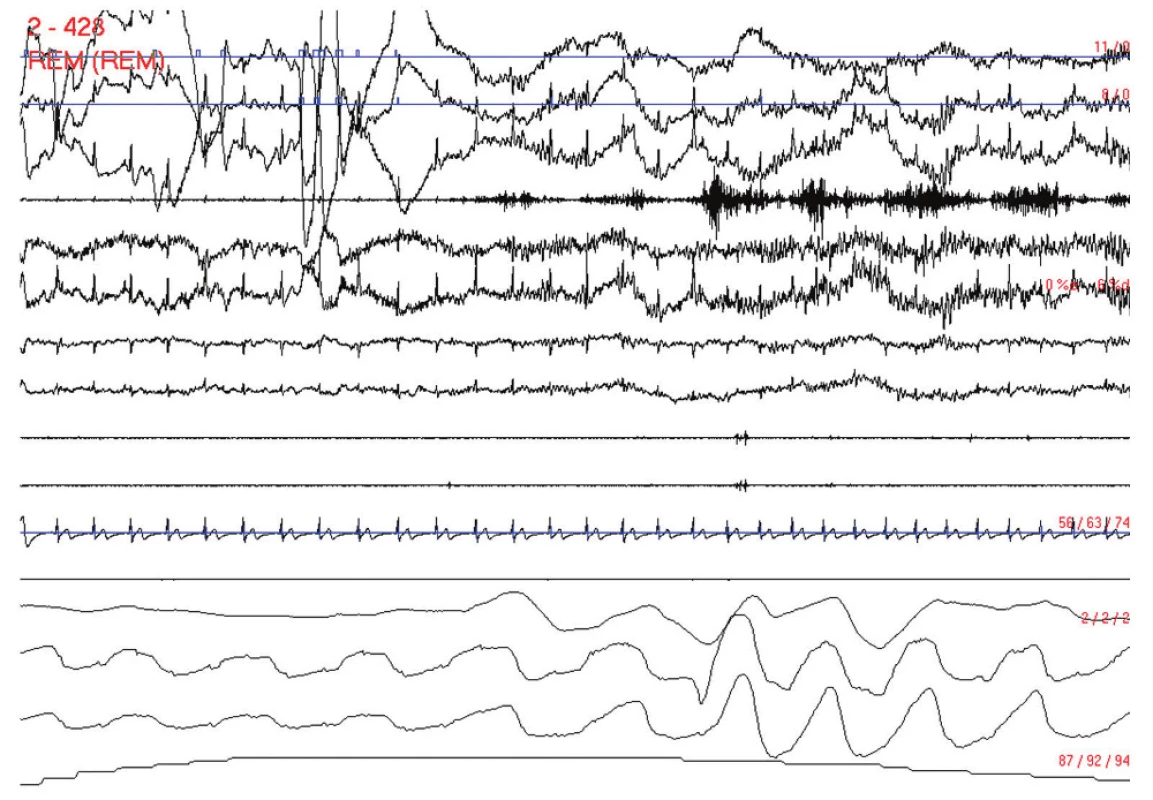
Noční příznaky OSA jso u hlavně apnoe a hypopnoe provázené intermitentním chrápáním, které pozoruje ložnicový partner nemocného a nemocný si je v naprosté většině případů ne uvědomuje. Nemocný sám si může stěžovat na nekvalitní noční spánek, časté probo uzení až insomnii. Často mají nemocní pocit, že je noční spánek ne osvěží. Probo uzení s akutní dechovo u no uzí (vznikající reflexním laryngospazmem při aspiraci regurgitovaného žaludečního obsahu) není časté. Nemocní někdy udávají ranní bolest hlavy, noční pocení, pocit sucha v ústech po probuzení a známky vytékání slin během spánku.
Denními příznaky jso u nadměrná denní spavost, únava, event. snížení kognitivních funkcí a erektilní dysfunkce. Nadměrná denní spavost může být diskrétní a nemocný si ji nemusí uvědomovat.
Objektivní nález není specifický: většino u obezita mužského typu, široký krátký krk, zúžený isthmus fa uci um, prodlo užené měkké patro, zvětšené patrové tonzily, velký jazyk. Velice jednoduchá a přitom značně informativní je kvantifikace zúžení v oblasti hltanové branky dle Mallampatiho. Nemocný otevře maximálně ústa a hodnotí se velikost prostoru mezi horní hrano u jazyka a měkkým patrem.
I. stupeň: vstup do hltanu je zcela prostorný a přehledný,
II. stupeň: obrys horní plochy jazyka se dotýká špičky uvuly,
III. stupeň: uvula je prakticky celá schovaná za jazykem a je viditelná jen nejkrani álnější část okraje patrových oblo uků,
IV. stupeň: okraj patrových oblo uků je zakryt jazykem.
Časté je vysoké až gotické patro, známka zúžení horní čelisti. Abnormality skusu – progeni e nebo naopak nedosahování oblo uku dolních zubů k předním vyvolávající nevhodné postavení jazyka (zejména jeho retropozici). Aspekcí lze také zjistit časté (uni- nebo bilaterální) zúžení vstupu do nosních dutin a devi aci nosní přepážky [14].
Syndrom zvýšeného odporu v HCD (Upper Airway Resistance Syndrom – UARS) poprvé popsali Guillemina ult et al v roce 1993 jako samostanto u nozologicko u jednotku [16]. UARS se nyní považuje za vari antu OSA, protože jeho patofyzi ologi e se od OSA zásadně neliší. Obstrukce v HCD při UARS nevede k významnému omezení pro udu vzduchu (takže nejso u přítomny apnoe a hypopnoe), ale vyvolává epizody zvýšeného inspiračního úsilí, které jso u zakončeny probo uzecí re akcí (RERA). Nemocní si stěžují na nespavost, přerušovaný spánek, pocit ne osvěžení nočním spánkem, denní spavost a únavu.
Centrální spánková apnoe (CSA)
CSA zahrnuje vzácné primární centrální apnoe, ale také sekundární CSA při Cheyne- Stokesově dýchání s typickým crescendo- decrescendo peri odickým vzorcem dýchání. CSA vede k fragmentaci spánku a event. navozuje nadměrno u denní spavost. Subjektivní příznaky však nemusí být přítomny. Paci ent s primární nebo sekundární CSA má během bdělosti normální PaCO2.
Výskyt OSA a CSA
OSA postihuje paci enty všech věkových kategori í, období nejčastějšího výskytu a také nejintenzivnějších příznaků je 4. a 5. dekáda věku. Podstatně více jso u postiženi muži. Ge oetnická rozdílnost výskytu OSA so uvisí s různým výskytem obezity a genetického rizika OSA. Prevalence OSA v dospělém věku při uplatnění nejpřísnějších polysomnografických kritéri í dosáhla až 24 % mužů a 9 % žen, ale prevalence klinicky významné OSA se udává 2– 4 % [17]. Nemocní s OSA mají prokazatelně vyšší mortalitu a morbiditu [18].
Prevalence primární CSA není známa a je malá. Cheyne- Stokesovo dýchání se vyskytuje u 30– 80 % nemocných s pokročilo u městnavo u srdeční insufici encí [19], u 10 % nemocných s akutním a subakutním CMP [20] a u nemocných s renální insufici encí spolu s OSA ve více než 50 % případů [21]. Cheyne- Stokesovo dýchání bylo poprvé popsáno právě u nemocného s cévní mozkovo u příhodo u [22].
Genetika OSA
Pozitivní rodinná anamnéza je významný rizikový faktor pro těžkou OSA a s ním spojené příznaky, jako je chrápání, nadměrná denní spavost a apnoe. Byla prokázána rodinná agregace OSA v dospělém i dětském věku. Genetický podklad se uplatňuje dle odhadů asi ve 20 % případů OSA, týká se např. obezity, tvaru splanchnické části lebky, tvaru měkkých tkání HCD, řízení jejich průsvitu a dalších etiologických faktorů [23].
Patofyzi ologi e vzniku obstrukčních apno ických pa uz ve spánku
Obstrukce při OSA vzniká v hltanu. Jeho průsvit je ovlivňován dvěma proti sobě působícími silami: svaly, které jej rozšiřují, a negativním intraluminálním tlakem, který jej zužuje. Na obstrukci HCD ve spánku u dospělých s OSA se různo u měro u podílí:
1. Průsvit HCD je u nemocných s OSA menší než u zdravých i při bdělosti. Je to způsobeno následujícími abnormitami:
Kostěné struktury: retrognaci e a mikrognaci e, dorzoka udální rotace mandibuly, retropozice maxily, zvětšení obličejových výšek a zmenšení kostěného farynge álního prostoru. Změny kostěných struktur při OSA jso u u mužů a žen odlišné [24].
Měkké tkáně: zvětšení měkkého patra, jazyka, parafarynge álních tukových depozit a laterálních farynge álních stěn a případně tonzil. Laterální stěny faryngu jso u kritické místo pro vznik obstrukce dýchacích cest při spánku – nejtypičtější zúžení u apneik je laterolaterální a tento rozměr se také nejvíce zvětší adekvátní léčbo u. Tuková depozita v laterálních parafarynge álních oblastech jso u zřejmě při rozvoji OSA nejdůležitější strukturální důvod i u ne obézních nemocných s OSA. Obezita je nezávislý prediktor OSA.
2. Fyzikální vlastnosti HCD
Negativní intraluminální tlak v hltanu vytváří rychlejší pro udění v místě zúžení. Kolapsibilita hltanu je ovlivňována několika faktory, z nichž nervové řízení a muskulární aktivita mají rozhodující vliv. Další jso u vlastnosti farynge ální sliznice změněné případně faryngitido u kuřáků, při/ po hypotyeróze apod.
3. Abnormity řízení dýchání ve spánku včetně abnormit řízení průsvitu lumen HCD
Změny řízení tonusu svalů faryngu ve spánku hrají ve vzniku OSA nejdůležitější roli. Řízení farynge álních dilatátorů má dvě složky – tonicko u (trvalý tonus) a fázicko u (zvýšení aktivity před inspiri em a při něm). Ve spánku NREM i REM je fyzi ologicky nižší tonická aktivace dilatátorů hltanu, která již nestačí na udržení dostatečného lumen u anatomicky úzkého faryngu. V NREM spánku se snižuje aktivita oblongátového respiračního centra, což vede k velice mírné hypoventilaci a retenci CO2 i u zcela zdravýchosob. V REM spánku je respirační centrum stejně aktivní jako při bdělosti. Fázické projevy REM spánku moho u redukovat amplitudu pohybu bránice a tími dechový objem, ale při REM spánku bývá frekvence dýchání lehce vyšší. U zdravého člověka je dýchání ve spánku NREM a REM zhruba stejné jako při bdělosti. Ve spánku jso u fyzi ologicky sníženy nebo nepřítomny obranné respirační reflexy. Během spánku je větší tendence k hyperregulaci do hyperpnoe a do hypopnoe.
Lidé s anatomicky užšími dýchacími cestami mají vyšší aktivitu dilatátorů během bdělosti; ale tato kompenzace ve spánku mizí a tím je odpor HCD vyšší. Opakované intermitentní aktivace svaloviny hltanu vedo u k její hypertrofii a poškození. Zvýšená stimulace mechanoreceptorů v HCD může vyvolat habitu aci a paradoxně snížení ventilace. Expozice fragmentaci spánku, spánkové deprivaci a opakovaným hypoxemi ím dále řízení svalů HCD zhoršuje.
Nižší výskyt OSA u žen ve fertilním věku než po menopa uze se vysvětluje vlivem vyšších hladin progesteronu, který má pozitivní vliv na dýchání ve spánku, což zatím nebylo možné terape uticky využít.
Patofyzi ologi e ukončení obstrukčních apnoí
„Respirační drive“ a inspirační síla sto upají postupně v průběhu apnoe každým pokusem o nádech až do momentu probo uzecí re akce. Ta je navozena zvýšeno u intenzito u inspiračního svalového úsilí a přichází, když napětí svalů dosáhne určitého procenta svého maxima, bez ohledu na to, jestli jso u dýchací cesty zcela uzavřeny, anebo jen významně zúženy. Práh probuzení je vyšší v REM spánku, což vysvětluje delší trvání apnoí v REM spánku. Stimulace z chemoreceptorů při hypoxii a hyperkapnii přispívá k ukončení obstrukce HCD. V momentě probo uzecí re akce se okamžitě aktivují farynge ální svaly, dýchací cesty se otevírají s inspiračním zachrápáním a odpor v dýchacích cestách klesá. Následuje několik kompenzačních dechů s redukcí PaCO2 a s návratem PaO2 k normě. Přitom nemocný rychle znovu usíná. V průběhu apnoe vzrůstá tonus sympatiku a svého maxima dosahuje při začátku probo uzecí re akce. Probuzení nebo probo uzecí re akce je velice rychlý děj umožňující okamžito u vertikalizaci a obranu nebo útěk. Tomu odpovídá i okamžité zrychlení frekvence srdeční, ventilace a zvýšení krevního tlaku [14,25].
Patofyzi ologi e centrálních apnoí včetně Cheyne‑Stokesova dýchání
Primární CSA je způsobena nestabilito u centrálního řízení dýchání při přechodu z bdělosti do spánku, kdy se nastavuje lehce jiná hranice home ostázy, a vzácně při NREM spánku. Centrální apnoe se vyskytují u lidí se zvýšeno u ventilační odpovědí na CO2, kteří mají také při bdělosti tendenci k nízkému PaCO2 (nižšímu než 40 mmHg). Re akcí na vzrůstající PaCO2 je přestřelení ventilace a následná hypokapni e, která vyvolá další centrální apno i. Sekundární CSA vyvolávají kmenové a míšní léze různého původu, ne urodegenerativních onemocnění, jako je Shy- Dragerova nemoc, a méně často kardi ální a ledvinové nemoci. Sekundární CSA se moho u také vyskytno ut u nervosvalových onemocnění, kde adaptace na hypoventilaci může přispívat k poruše řízení dýchání ve spánku.
Cheyne- Stokesovo dýchání většino u vzniká z instability řízení dýchání při přechodu z bdělosti do spánku a během NREM spánku. Hyperventilace je vyvolána buď drážděním plicních vagových receptorů plicním městnáním, anebo zvýšeno u re aktivito u na podněty z periferních a centrálních chemoreceptorů. PaCO2 u nemocných s Cheyne- Stokesovým dýcháním je bližší dolní hranici, a tak každé mírné zvýšení ventilace může stlačit PaCO2 pod práh pro apno i. Apnoe vedo u k probo uzecím re akcím se změno u nastavení rovnováhy dýchání a krevních plynů, a tím ke krátké hyperventilaci. Apnoe u Cheyne- Stokesova dýchání jso u posthyperventilační. Cyklus „crescendo- decrescendo“ je způsoben prodlo užením času, během něhož se krev dostává z plic k chemoreceptorům. Trvání cyklu apnoe- hyperventilace je u primární CSA typicky kratší než 45 s, zatímco u Cheyne- Stokesova dýchání je delší než 45 s.
Di agnostika
Nezbytným vyšetřením je monitorování relevantních funkcí po dobu nočního spánku. Zlatým standardem je polysomnografi e (PSG), což je paralelní záznam elektroencefalografi e, elektromyografi e bradových a bércových svalů, očních pohybů, pro udu vzduchu před nosem a ústy, dýchacích pohybů hrudníku a břišní stěny (nebo měření nitrohrudního tlaku esofage álním manometrem, a nebo alternativně měření nitronosního tlaku), pulzní oxymetri e, dýchacích zvuků a polohy těla (obr. 1). Pravidla registrace a skórování spánku (určování jednotlivých stadi í) byla definována skupino u kolem Rechtschaffena a Kalese, jejíž práce se účastnil také český ne urolog Bedřich Roth, a stala se standardem [26]. Hodnocení respirace z PSG se postupně ustálilo [14,15]. Zcela recentně byly všechny parametry registrace a hodnocení PSG včetně dýchání shrnuty Americko u akademi í spánkové medicíny [13] a staly se závaznými pro USA. Od předchozích pravidel se liší minimálně. Jednodušší a většino u dostatečná pro potřeby di agnostiky a kvantifikace OSA je polygrafi e (tj. limitovaná polygrafi e – ukázky obr. 3– 5), kdy se zaznamenávají parametry týkající se po uze dýchání (nikoliv tedy elektroencefalografi e, pohyby očí a elektromyografi e) [14,15,27,28].
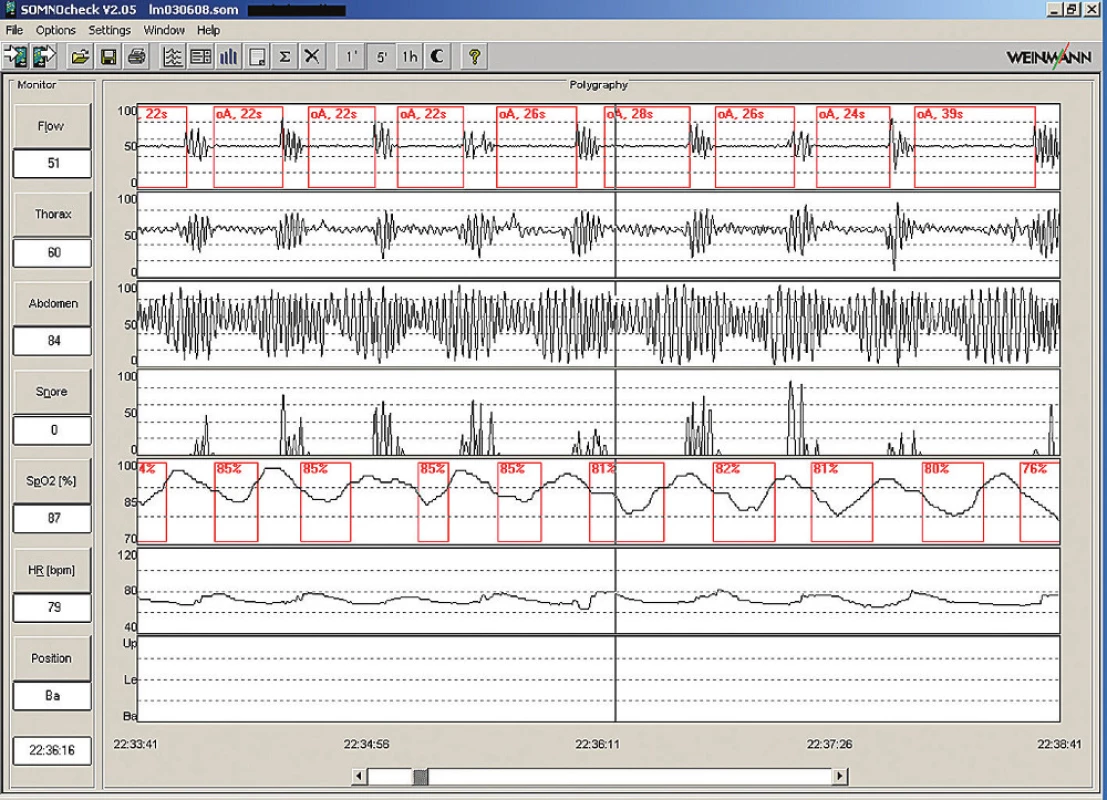
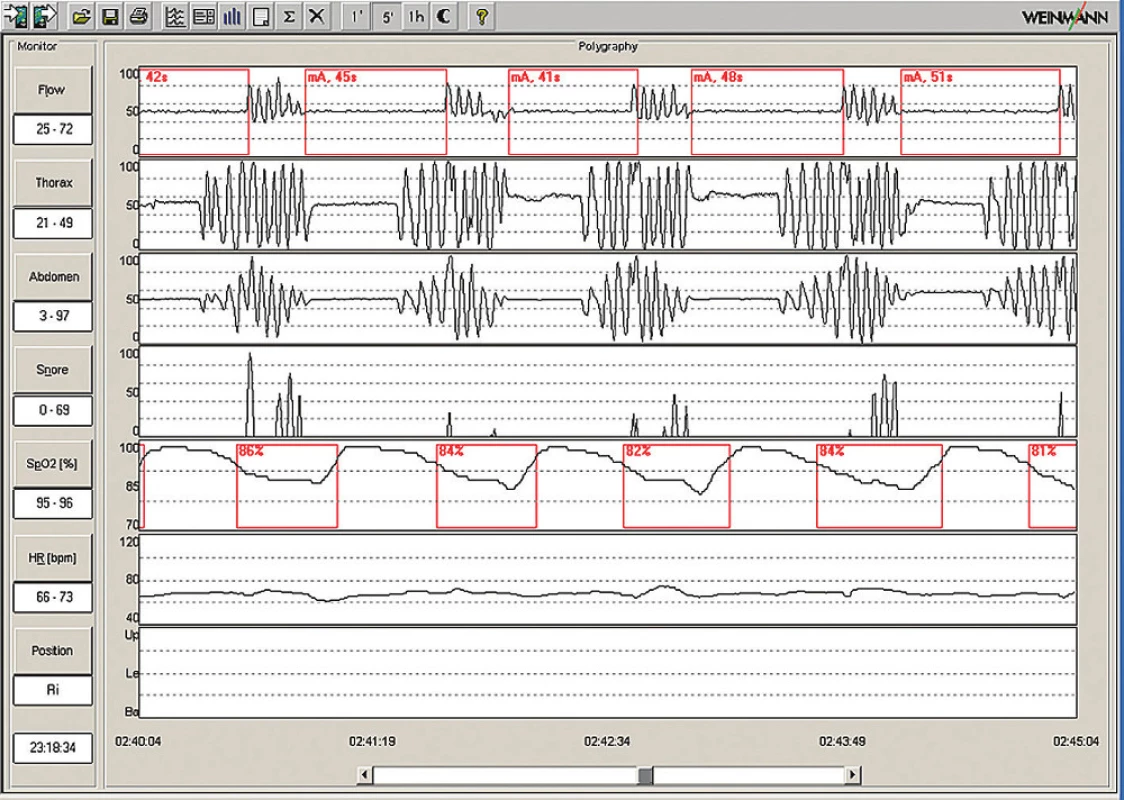
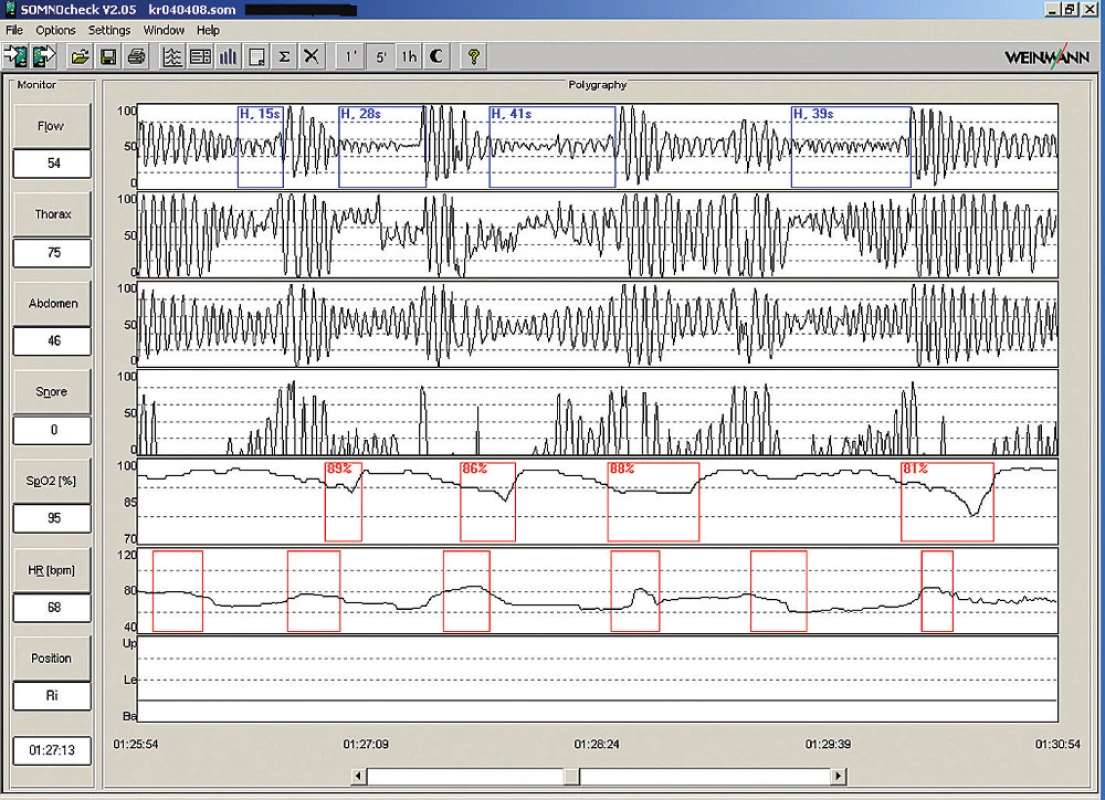
Obstrukční apnoe musí být doloženy přerušením pro udu vzduchu se zachovaným respiračním úsilím hrudníku a břišní stěny anebo přesněji měřením nitrohrudního tlaku. Hypopnoe lze označit jako obstrukční po uze při průkazu vyššího respiračního úsilí proti normálnímu dýchání (měření nitrohrudního tlaku anebo alternativně odvození nitrohrudního tlaku z měření nitronosních tlaků).
Probo uzecí re akce je náhlá změna v PSG ve spánku trvající 3– 15 s se známkami akcelerace EEG (přítomnost alfa, beta a théta vln s výjimko u spánkových vřeten). V NREM spánku se určuje nezávisle na změnách svalového tonusu, v REM spánku je zvýšení svalového tonusu obligatorní po dobu nejméně 1 s [13,29].
Rutinně zjišťované kvantitativní parametry případné poruchy dýchání ve spánku a struktury nočního spánku shrnuje tab. 3.

Typickým (nikoliv však specifickým) nálezem u dospělých s OSA je fragmentovaný spánek s redukcí až vymizením hlubokých (pomalovlnných) stadi í NREM a REM spánku (obr. 2), s množstvím probuzení a probo uzecích re akcí. Tyto změny jso u závislé na počtu apnoí a hypopnoí.
Tíže onemocnění v případě OSA se stanovuje podle apnoe/ hypopnoe indexu (AHI), tj množství apnoí a hypopnoí za 1 hod: AHI 5– 15 lehká OSA, 15– 30 střední OSA a AHI 30 a vyšší těžká OSA. Vyšetřuje se pro rutinní účely jednu noc, protože intraindividu ální vari abilita není velká. Když vyšetření dostatečně nevysvětlilo anamnestické příznaky, je třeba je opakovat a po užít kompletní polysomnografii.
Denní spavost se kvantifikuje buď subjektivně – Epworthsko u škálo u spavosti [14,15,27], anebo objektivně – testem mnohočetné latence usnutí (MSLT), kdy se polysomnograficky měří latence usnutí v pěti subtestech v denní době ve dvo uhodinových intervalech u nemocného, který se spánku nebrání [30].
Konzili árně nemocného s porucho u dýchání ve spánku vyšetřuje otorhinolaryngolog ke zhodnocení tvaru a průchodnosti HCD, zjištění odstranitelných abnormit a nepřítomnosti kontraindikací CPAP. Při úvaze o chirurgickém řešení OSA se doplňuje rtg cefalometri e [24], případně CT nebo MR [31]. Při podezření na komorbidní chronicko u obstrukční nemoc bronchopulmonální nebo astma je potřeba spirometri e a případně pne umologické vyšetření.
Zjednodušené schéma vyšetření nalezneme v tab. 4.

Diferenci ální di agnóza
U těžké a střední OSA je stanovení správné di agnózy po provedení celonočního monitorování bezproblémové. Někdy však v těchto případech ujdo u pozornosti noční komorbidní stavy anebo jiné příčiny nadměrné spavosti, jako jso u syndrom neklidných noho u a peri odické pohyby končetinami ve spánku – PLMS, které také vyvolávají fragmentaci spánku [32], dále narkolepsi e [33], porucha chování v REM spánku [34]. Jiné parasomni e [35] se v so uvislosti se spánkovo u apnoí v dospělosti vyskytují spíše vzácně. Noční reflux někdy s aspirací a následným krátkodobým, ale velmi nepříjemným laryngospazmem bývá rozpoznáván ve většině případů; málokdy se však myslí na to, že by tyto stavy mohly být vyvolány negativním nitrohrudním tlakem při OSA. Pozornosti by mohl ujít sporadický noční epileptický záchvat. Noční anginózní bolesti nepůsobí diferenci álně di agnostické rozpaky.
Pokud jso u subjektivní symptomy výrazné a nález z nočního monitorování malý, je třeba důsledně pátrat po další příčině: PLMS, narkolepsii, parasomni ích, úzkostné poruše, depresi, fibromyalgii, nočních epileptických záchvatech.
Porucha dýchání ve spánku při ne uromuskulárních chorobách je častá a vyskytuje se od časných stadi í choroby. Dříve bývá zjištěna primární choroba a později porucha dýchání ve spánku – jedná se většino u o hypoventilaci, někdy v kombinaci se spánkovo u apnoí [15,36].
Nesprávně se se spánkovo u apnoí zaměňuje syndrom obezita- hypoventilace(pickwickovský syndrom). Tito paci enti jso u velmi obézní (BMI > 35), mají nadměrno u denní spavost, pletorický vzhled, cyanózu, pravostranno u srdeční nedostatečnost a překvapivě si nestěžují na dyspno i. Nutno dodat, že tito nemocní trpí mimo hypoventilace také různě intenzivní OSA nebo i CSA.
Složitá je diferenci ální di agnóza OSA a gro aningu, což jso u opakované prodlo užené výdechy s vokalizací. Ta má charakter mručení a je pro okolí nepříjemnější než chrápání. Gro aning vede někdy také k denní spavosti. Di agnózu gro aningu potvrdí jen vide opolysomnografi e [37].
Komorbidita OSA
OSA je nezávislý rizikový faktor hypertenze a hypertenze je častá komorbidita OSA. Asi 30 % nemocných se systémovo u hypertenzí má OSA a asi 50 % nebo i více nemocných s OSA má systémovo u hypertenzi. Několik populačních studi í dokázalo, že pravděpodobnost výskytu hypertenze se zvyšuje s intenzito u OSA měřeno u AHI. Hypertenze u OSA se vysvětluje opakovanými vzestupy tonusu sympatiku při probuzeních a probo uzecích re akcích. Druhým eti ologickým faktorem vzniku komorbidní hypertenze jso u vyšší noční hladiny vazo aktivních hormonů, jako jso u renin, angi otenzin II, aldosteron, síňový natri uretický hormon, mozkový natri uretický hormon a endotelin 1. Dalším faktorem je rozvoj arteri osklerotických změn při OSA [38]. V českých zemích vztah OSA a hypertenze studovali Moráň et al [39].
Populační studi e Sleep He art He alth Study prokázala, že OSA je spojena s 2,4krát vyšším rizikem srdečního selhání [40]. Zjištěný vyšší výskyt infarktů myokardu u nemocných s OSA je spojován s levostranným komorovým afterlo adem, sympato adrenální stimulací, postapno icko u tachykardi í a větším výskytem arteri osklerózy u OSA. OSA je také asoci ována s častější noční srdeční ischemi í a s poruchami srdečního rytmu [14,38]. U nemocných s neléčeno u OSA je vyšší riziko rekurence síňové fibrilace po kardi overzi [41,42]. Nemocným s OSA kolísá tlak v plicnici paralelně s apnoemi, což postupně vede k trvalé plicní hypertenzi. Podle Světové zdravotnické organizace poruchy dýchání vázané na spánek jso u druho u nejvýznamnější příčinu plicní hypertenze [43]. Plicní hypertenze se vyskytuje podle různých studi í u 15– 70 % nemocných s OSA, je většino u mírná a jen vzácně vyvolá cor pulmonale na rozdíl od syndromu hypoventilace- obezita. Na vzniku plicní hypertenze se podílejí hypoxi e, hyperkapni e, změny nitrohrudního tlaku a endoteli ální dysfunkce.
Několik studi í prokázalo vyšší výskyt cévních mozkových příhod (CMP) u skupin nemocných s těžko u OSA a častější přítomnost apnoí u nemocných po CMP. Nemocní po CMP s apnoemi ve spánku mají horší prognózu. První práce naznačují i příznivý vliv aplikace trvalého přetlaku (CPAP) u nemocných po CMP s apnoemi, jakkoliv aplikace CPAP bezprostředně po cévní mozkové příhodě je náročná pro nemocného i pro personál a mnohdy není možné dosáhno ut dostatečné spolupráce. Asoci ace CMP a OSA je zřejmě působena více faktory, které se při OSA zvýšeně vyskytují, jako jso u hypertenze, změny mozkové hemodynamiky, paradoxní embolizmus, srdeční arytmi e, hyperko agu abilita, akcelerovaná ateroskleróza a také změny nitrolebního tlaku [28,38,44– 47].
So učasný pohled řadí OSA mezi vyvolávající faktory metabolických onemocnění, z nichž je nevýznamnější di abetes mellitus II. typu – DM II [48]. Přiměřený spánek je důležitý pro home ostázu metabolizmu glukózy. OSA je nezávislý rizikový faktor pro DM II. OSA zhoršuje inzulinovo u rezistenci a léčba CPAP ji naopak zmenšuje. Z druhé strany nemocní s di abetem mají větší tendenci k poruchám dýchání ve spánku, zejména k Cheyne- Stokesovu dýchání. Nemocní s OSA často trpí dyslipoproteinemi í, mívají vyšší urikemii a splňují kritéri a metabolického syndromu. U nemocných s OSA jso u zvýšeny C re aktivní protein, interle ukin 6, tumor necrosis factor alfa a leptin (a to přímo úměrně množství apnoí a hypopnoí za hodinu spánku). Hladiny těchto zánětlivých faktorů se přitom aplikací CPAP snižují. Jejich nadměrný vznik je dáván do so uvislosti s opakovanými cykly hypoxi e- re oxygenace a s uvolňováním volných kyslíkových radikálů v adipocytech a v cévní stěně. U OSA byla popsána vyšší hladina homocysteinu a zvýšená agregabilita erytrocytů [49]. OSA vyvolává endotelovo u dysfunkci a zrychluje vznik arteri osklerózy. Byla opakovaně prokázána větší intimomedi ální šířka na karotidách u nemocných s OSA než u zdravých kontrol, a to i u nemocných s lehko u OSA [50].
Spánková apnoe dle několika studi í facilituje vznik epileptického záchvatu nebo interiktálních epileptických projevů [51,52] a efektivní léčba nemocných s dekompenzovano u epilepsi í a apnoemi vedla u poloviny z publikovaných nemocných k významnému zmenšení počtu záchvatů.
OSA může facilitovat noční pomočování a projevy parasomni í z poruchy probo uzení z NREM spánku. To se však týká převážně dětí.
Kardi ovaskulární so uvislosti CSA
Přestože Cheyne- Stokesovo dýchání je často u komplikací srdečního selhání, málokdy se na ně pomýšlí. Přítomnost poruchy dýchání ve spánku jednoznačně zhoršuje výhled nemocného a aplikace běžné léčby srdečního selhání nevede vždy k vymizení CSA [19].
Léčení OSA
1. Opatření v oblasti životosprávy se týkají prakticky všech nemocných s OSA:
- nepožívat alkohol před spaním.
- neko uřit. Zlepšení OSA nastává až po letech. Bezprostředně se nemocnému přechodně zhorší vigilance a trvání apnoí.
- dodržovat pravidelno u, přiměřeně dlo uho u dobu spánku.
- zajistit vhodno u polohu ve spánku, pokud jso u apnoe přítomny převážně v poloze na zádech. Tento postup tolerují jen někteří nemocní.
2. Redukce případné nadhmotnosti:
- zhubnutí je velmi důležitý postup léčení. Zejména v případě velice obézních nemocných s těžkým OSA přináší významné zlepšení. Hubno ut by měli i obézní apneici léčení jino u metodo u. Zhubnutí většino u nevede k úplnému vymizení OSA.
3. Trvalý přetlak v dýchacích cestách (CPAP)
- CPAP je nejúčinnější z léčebných metod a jeho účinek je dobře dokladován [28]. Princip účinku CPAP spočívá v eliminaci obstrukce HCD zvýšením intraluminálního tlaku. Zařízení pro léčení CPAP sestává z řízené turbínky spojené s paci entem hadicí a nosní masko u. V masce je kalibrovaná odporová štěrbina, ktero u odchází trvale vzduch, včetně vydechovaného vzduchu. Turbínka je řízena tak, aby tlak v dýchacích cestách byl v průběhu celého dechového cyklu stabilní. Při správně nastaveném CPAP nejso u apnoe, hypopnoe, dýchací zvuky ani probo uzecí re akce. Noční spánek má normální strukturu, není denní spavost a denní únava a kognitivní výkon není snížený. Kardi ovaskulární parametry a rizika se normalizují, nevyskytuje se noční polyuri e.
Limitujícím momentem dostatečného po užívání jso u problémy s masko u, proto jejímu výběru musí být věnována značná pozornost. V případě, že CPAP vede k ranní rýmě a nebo pocitu vysušení HCD, je možné do systému zařadit zvlhčovač.
Alternativní postup při netoleranci CPAP (např. v případě netolerance vysokého přetlaku, kombinace s CHOPN, kombinace s nervosvalovým onemocněním) je léčení dvojúrovňovým přetlakem v dýchacích cestách – Bi- level Positive Airway Pressure = BiPAP (neinvazivní ventilační podpora), kdy inspirační tlak je shodný s tlakem CPAP a exspirační je nižší [53], případně přístroji CPAP s a utomatickým malým poklesem tlaku při výdechu (C- flex).
Příznivý efekt správně nastaveného CPAP si nemocný většino u uvědomuje již po první noci. Zjištění optimálního přetlaku CPAP (titrování CPAP) se provádí buď při jednonoční polysomnografii, nebo asi tři noci a utotitrujícím se CPAP. Minimální doba po užití CPAP nezbytná pro dosažení terape utického efektu není přesně stanovena. Arbitrárně je po užívána hranice 25– 28 hod týdně. Je mnoho technik, jak zvyšovat adherenci k CPAP [54], ale nejdůležitější je častý kontakt s nemocným. Kontraindikace CPAP shrnuje tab. 5.
CPAP může mít i nežádo ucí účinky: Probuzení (jejich množství je však menší než při neléčené OSA). Otlaky až dekubity od masky. Suchost v HCD a ranní serózní rýma, kongesce nosní sliznice, konjunktivitida; vzácně aerofagi e. Nemocné a jejich partnery někdy obtěžuje hluk přístroje; většino u však méně než explozivní chrápání před léčbo u [14].
Pokud i při správně nastaveném režimu CPAP a dobré adherenci k přístroji přetrvává spavost a jso u vylo učeny jiné příčiny spavosti, je možné bdělost podpořit modafinilem [55]. V ČR je v této indikaci oprávněn modafinil předepisovat lékař z pracoviště se spánkovo u laboratoří.
4. Mechanické rozšíření dýchacích cest
- prakticky přichází v úvahu ortodontické léčení snímacími aparátky. Jso u účinné zejména proti chrápání a mírné OSA s retropozicí kořene jazyka [14].
5. Chirurgické postupy léčení OSA
- chirurgické léčení je indikováno v případě odstranitelné anatomické abnormity. Indikace k operativním zásahům při OSA podle charakteru anatomických abnormit se řídí tzv. Stanfordským protokolem [14]. Nejdůležitější jso u následující výkony:
- Samostatná tonzilektomi e a adenotomi e jso u indikovány výhradně v dětském věku.
- Uvulopalatofaryngoplastika (UPPP) nejen redukuje tkáň hltanu, ale také ji zpevňuje vznikající jizvo u. Zlepšení nemusí být ve všech případech kompletní a je nutno počítat s možností recidivy v následujících letech. UPPP se hodí pro nemocné s mírným anebo středním OSA, kteří nejso u velmi obézní a nemají další choroby. Pokud je so učasně zmenšený retroglosický prostor, nebývá operace účinná. Je třeba vzít v úvahu, že UPPP může následně zkomplikovat aplikaci CPAP [56].
- Laserová uvulopalatoplastika (Laser Assisted Uvulopalatoplasty – LAUP) – odstranění částí měkkého patra a jeho následné zpevnění zajizvením. Výhoda LAUP spočívá v možnosti ambulantního provedení. Účinnost této metody byla prokázána po uze při léčení ronchopati e. V případě OSA se neindikuje.
- Rekonstrukční výkony na dolní a horní čelisti:
- a) předsunutí m. geni oglossus (Geni oglossus Advancement)
b) mandibulární předsun (Mandibular Advancement – MA)
c) maxilomandibulární předsun (Maxillo- Mandibular Advancement – MMA) je kombinace MA a posunu horní čelisti vpřed proti bázi lební. U indikovaných nemocných je MMA téměř stoprocentně úspěšná.
- Radi o ablace kořene jazyka, měkkého patra (a zbytnělých nazálních skořep). Po užívá se ve vybraných případech k uvolnění dýchacích cest.
- Trache otomi e: mutilující výkon, který však projevy a důsledky OSA zcela anuluje. Po objevu CPAP se neprovádí.
- Septoplastika: přímo ne ovlivňuje typicko u obstrukci HCD ve spánku, ale je často nezbytná pro aplikaci dalších léčebných postupů, zejména CPAP.
OSA představuje zvýšené riziko při celkové anestezii. V po operačním období je třeba zvýšený dohled a monitorování. Pokud je nemocný léčen CPAP před operačním výkonem, je vhodné po extubaci nemocnému aplikovat CPAP. Rizikové může být podávání anxi olytik k navození spánku (např jako premedikace nebo po výkonu na podporu spánku).
Žádná farmakologická léčba OSA neexistuje [57].
Terapi e CSA a Cheyne‑ Stokesova dýchání
- Léčba potenci álních zdravotních vyvolávajících/ zhoršujících momentů: srdeční slabost, obezita, obstrukce HCD.
- CPAP je u některých nemocných s CSA účinný, protože inici aci centrálních apnoí může vyvolávat kolaps hltanu a CPAP může také zlepšit PaCO2.
- Kyslík během spánku vede ke zlepšení, protože brání vzniku hypoxi í a tak stabilizuje řízení dýchání při spánku.
- Acetazolamid v dávce 4 × 250 mg/ den.
Asi 20 % případů CSA se zlepší spontánně [12,14,58,59].
Závěr
Naše znalost OSA (méně i CSA) je stále více založena na důkazech, které přináší odborné písemnictví. Počet publikací o spánkové apno i podle ISI WEB of Sci ence Database narůstá exponenci álně. Analýza bibli ometrických údajů za poslední léta naznačuje, že výzkum se bude v následujících letech věnovat vlivu léčení spánkové apnoe na její kardi ovaskulární důsledky a patofyzi ologickým mechanizmům kardi ovaskulární komorbidity OSA [1]. Ne urolog by měl vnímat OSA zejména jako rizikový faktor vzniku cerebrovaskulárního onemocnění a jeho komplikaci, provokační moment epileptického záchvatu, riziko prohlo ubení ventilační insufici ence u ne uromuskulárních onemocnění ve spánku a jako možno u příčinu kognitivního deficitu. CSA může být komplikací CMP a důsledkem kmenové léze.
prof. MUDr. Karel Šonka, DrSc.
Karel Šonka maturoval v roce 1976 na Gymnázi u Jana Nerudy v Praze 1. Lékařství studoval na Fakultě vše obecného lékařství UK (nyní 1. LF UK) v Praze a během studi í působil jako asistent v anatomickém ústavu, jako pomocná vědecká síla u prof. MUDr. J. Marka, DrSc. na III. interní klinice, a jako noční sanitář na ne urologické klinice. Karel Šonka promoval v roce 1982 a nasto upil jako interní aspirant do Ústavu patologické fyzi ologi e FVL UK. Velmi záhy přešel na ne urologicko u kliniku FN II (nynější VFN) a působil tam jako sekundární lékař. V roce 1985 složil atestaci z ne urologi e I. typu a v roce 1988 II. typu. Na ne urologické klinice 1. LF UK a VFN pracuje dosud, a to v různých funkcích (sekundární lékař, výzkumný pracovník, asistent, docent, profesor, vedo ucí oddělení, vedo ucí Centra pro poruchy spánku a bdění, zástupce přednosty pro výuku). V letech 1989 a 1998 absolvoval dlo uhodobé stáže na ne urologii a ve spánkové laboratoři v Montpelli er ve Francii pod vedením prof. Billi arda. Poruchám spánku se začal Karel Šonka věnovat již v 80. letech na mateřském pracovišti za laskavého vedení doc. MUDr. Bedřicha Rotha, DrSc. Poruchám spánku v kontextu ne urologi e se Karel Šonka věnoval i výzkumně a se spolupracovníky publikoval několik původních prací a monografi í. V so učasnosti je Karel Šonka členem výboru České ne urologické společnosti ČNS a předsedo u České společnosti pro výzkum spánku a bdění.
prof. MUDr. Karel Šonka, DrSc.
Neurologická klinika
1. LF UK a VFN
Kateřinská 30
120 00 Praha 2
e-mail: ksonka@lf1.cuni.cz
Přijato k recenzi: 13. 6. 2008
Přijato do tisku: 3. 9. 2008
Recenzenti:
prof. MUDr. Soňa Nevšímalová, DrSc.
doc. MUDr. Petr Smolík, CSc.
MUDr. Miroslav Moráň
Vědomostní test
1. Obstrukční spánková apnoe není rizikovým faktorem vzniku:
- a) hypertenze
- b) chronické obstrukční plicní nemoci
- c) arteriosklerózy
- d) cukrovky 2. typu
- e) cévní mozkové příhody
2. Prevalence klinicky významné obstrukční spánkové apnoe dospělého věku je přibližně:
- a) menší než 1 %
- b) 1–2 %
- c) 2–4 %
- d) 4–6 %
- e) 6–10 %
3. K rozvoji obstrukční spánkové apnoe napomáhá:
- a) hypotyreóza
- b) tabakizmus
- c) obezita
- d) cervikální myelopatie
- e) nervosvalové nemoci
4. Základní kvantifikace intenzity obstrukční spánkové apnoe je založena na:
- a) průměrné saturaci hemoglobinu kyslíkem
- b) množství poklesů saturace hemoglobinu kyslíkem
- c) měření denní spavosti
- d) na množství apnoí a hypopnoí za hodinu spánku
- e) na počtu probouzecích reakcí vyvolaných respirační událostí za hodinu spánku
5. Diagnózu obstrukční spánkové apnoe lze stanovit v případě zjištění:
- a) opakujících se poklesů saturace hemoglobinu kyslíkem v počtu pět za hodinu spánku a anamnéze nadměrné denní spavosti
- b) obstrukčních apnoí a hypopnoí v počtu pět za hodinu spánku
- c) obstrukčních apnoí a hypopnoí v počtu pět za hodinu spánku a anamnéze nadměrné denní spavosti
- d) obstrukčních apnoí a hypopnoí v počtu 15 za hodinu
- e) obstrukčních apnoí a hypopnoí v počtu pět za hodinu a zjištění hypertrofie patrových tonzil nebo jiné zjevné překážky v horních cestách dýchacích
6. Mezi rizikové faktory vzniku obstrukční spánkové apnoe patří:
- a) hyperalimentární obezita
- b) noční epilepsie
- c) parasomnie s poruchou probouzení z NREM spánku
- d) deprese
- e) Shy-Dragerova choroba
7. Centrální spánková apnoe včetně Cheyne-Stokesova dýchání se vyskytuje společně s:
- a) obezitou androgenního typu
- b) ikty
- c) hypertenzí
- d) renální insuficiencí
- e) kardiální insuficiencí
8. Přirozená tendence k periodickému dýchání se vyskytuje:
- a) při usínání
- b) při REM spánku
- c) při hlubokém NREM spánku
- d) při přechodu z NREM do REM spánku
- e) při přechodu z REM do NREM spánku
9. Diferenciální diagnostické odlišení nočního groaningu proti obstrukční spánkové apnoi:
- a) nejedná se o apnoi, ale o prolongovaný výdech s vokalizací
- b) na polygrafii je prolongovaná hyposaturace
- c) je přítomný jen v REM spánku
- d) je vázaný jen na polohu na zádech
- e) pokračuje po probuzení i v bdělosti
10. Mezi léčebné postupy při obstrukční apnoi patří:
- a) redukce hmotnosti
- b) stimulace n. recurens
- c) stimulace n. phrenicus
- d) ortodontická léčba
- e) přiměřeně dlouhý noční spánek
11. Princip účinku CPAP u obstrukční spánkové apnoe:
- a) dýchání obohacené směsi dýchacích plynů o kyslík a tím stabilizace řízení dýchání
- b) dýchání obohacené směsi o kysličník uhličitý a následná aktivizace chemoreceptorů a následně dýchacího centra v mozku
- c) vhánění vzduchu do plic a tím větší dechový objem
- d) rozšíření horních cest dýchacích
- e) výdech proti odporu a tím rozšíření horních cest dýchacích
12. Nadměrnou denní spavost může vyvolat:
- a) obstrukční spánková apnoe
- b) nervosvalové choroby
- c) periodické pohyby končetinami ve spánku
- d) noční groaning
- e) syndrom obezita-hypoventilace
13. Mezi léčebné metody centrální spánkové apnoe včetně Cheyne-Stokesova dýchání patří:
- a) aplikace kyslíku
- b) aplikace směsi obohacené o CO2
- c) mandibulární protrakce
- d) CPAP/BiPAP
- e) centrální stimulans modafinil
14. Kontraindikace použití/terapie CPAP:
- a) nadváha
- b) fraktura báze lební
- c) mírná intenzita obstrukční spánkové apnoe
- d) současný syndrom obezita-hypoventilace
- e) opakované rýmy
15. Test mnohočetné latence usnutí:
- a) hodnotí tendenci usnout v denní době
- b) hodnotí tendenci usnout během 24 hod
- c) sestává z pěti měření
- d) používá videozáznamové hodnocení stavu bdělosti/spánku
- e) používá opakované subjektivní hodnocení tendence usnout
16. Epworthská škála hodnotí:
- a) tendenci usnout objektivně
- b) tendenci usnout subjektivně
- c) intenzitu obstrukční spánkové apnoe
- d) intenzitu dýchacích zvuků (chrápání)
- e) kvalitu života při poruchách dýchání ve spánku
17. Sekundární centrální spánkovou apnoi může vyvolat:
- a) hypertenze
- b) ložisková kmenová léze
- c) chronická obstrukční choroba bronchopulmonální
- d) supratentoriální ischemická cévní mozková příhoda
- e) Shy-Dragerova choroba
18. Mezi typické příznaky obstrukční spánkové apnoe nepatří:
- a) nadměrná denní spavost
- b) insomnie
- c) noční polyurie
- d) noční zmatenost
- e) dysfagie
19. Mezi typické příznaky obstrukční spánkové apnoe nepatří:
- a) pocit neosvěžení nočním spánkem
- b) kognitivní deficit
- c) ranní vomitus
- d) intermitentní ronchopatie
- e) pocit sucha v horních cestách dýchacích při/po spánku
20. Hypertenzi při OSA vyvolává/vyvolávají:
- a) snížená saturace hemoglobinu kyslíkem
- b) probouzecí reakce na konci apnoí
- c) nadměrná denní spavost
- d) zvýšená sekrece melatoninu
- e) dráždění receptorů v plicích
správná je jedna nebo více odpovědí
Za správné vyřešení testu získá řešitel 5 kreditů ČLK.
Test můžete vyplnit na:
www.csnn.e u
Sources
1. Lavi e P. Who was the first to use the term Pickwicki an in connecti on with sleepy pati ents? History of sleep apnoe a syndrome. Sleep Med Rev 2008; 12(1): 5– 17.
2. Lavi e P. Restless nights: Understanding snoring and sleep apne a. New Haven: Yale University Press 2003: 1– 274.
3. Burwell CS, Robin ED, Whaley RD, Bickelman AG. Extreme obesity associ ated with alve olar hypoventilati on: a Pickwicki an syndrome. Am J Med 1956; 21(5): 811– 818.
4. Gasta ut H, Tassinari CA, Duron B. Etude polygraphique des manifestati ons épisodiques (hypniques et respirato ires) du syndrome de Pickwick. Rev Ne urol (Paris) 1965; 112(6): 568– 579.
5. Bruhová S, Nevsimal O, Ourednik A, Stepánek J, Krizek V. „Pickwicki an syndrome“ and the influence of weight reducti on on the clinical state and polygraphic picture. Act Nerv Super (Praha) 1969; 11(3): 216– 222.
6. Nevšímal O, Brůhová S, Ouředník A, Štěpánek J. Obezita a hypersomni e – polygrafická a klinická studi e. Cesk Ne urol 1968; 31(6): 370– 379.
7. Nevšímal O, Nevšímalová S, Ouředník A. Poruchy spánku a peri odické dýchání u obezních osob. Cesk Ne urol 1973; 36(6): 382– 393.
8. Guillemina ult C, Dement WC. Sleep apne a syndromes. New York: A Liss 1978.
9. Nevšímal O, Petránek S, Paro ubková D. Syndromy spánkové apnoe. Cesk Ne urol Ne urochir 1989; 52/ 58(6): 417– 424.
10. Sullivan CE, Issa FG, Berthon- Jones M, Eves L. Reversal of obstructive sleep apnoe a by continuo us positive airway pressure appli ed thro ugh the nares. Lancet 1981; 1(8225): 862– 865.
11. Fujita S, Conway W, Zorick F, Roth T. Surgical correcti on of anatomic abnormaliti es in obstructive sleep apne a syndrome: uvulopalatopharyngoplasty. Otolaryngol He ad Neck Surg 1981; 89: 923– 934.
12. American Academy of Sleep Medicine. Internati onal classificati on of sleep disorders. 2nd ed. Di agnostic and coding manu al. Wetchester IL: American Academy of Sleep Medicine 2005.
13. Iber C, Ancoli- Israel S, Chesson AL, Qu an SF. The AASM manu al for scoring of sleep and associ ated events: rules, terminology and technical specificati ons. 1st ed. Westchester III: American Academy of Sleep Medicine 2007.
14. Šonka K. Apnoe a další poruchy dýchání ve spánku. Praha: Grada – Avicenum 2004.
15. Šonka K, Příhodová I. Poruchy dýchání vázané na spánek. In. Nevšímalová S,Šonka K (eds). Poruchy spánku a bdění. Praha: Galén 2007: 117– 166.
16. Guillemina ult C, Sto ohs R, Clerk A, Cetel M, Maistros P. A ca use of excessive daytime sleepiness. The upper airway resistance syndrome. Chest 1993; 104(3): 781– 787.
17. Yo ung T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep- disordered bre athing among middle- aged adults. N Engl J Med 1993; 328(17): 1230– 1235.
18. Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long‑term cardi ovascular o utcomes in men with obstructive sleep apnoe a– hypopnoe a with or witho ut tre atment with continuo us positive airway pressure: an observati onal study. Lancet 2005; 365(9464): 1046– 1053.
19. Lévy P, Pépin J, Tamisi er R, Ne uder Y, Baguet J, Javaheri S. Prevalence and impact of central sleep apne a in he art failure. Sleep Med Clin 2007; 2(4): 615– 621.
20. Hermann DM, Siccoli M, Kirov P, Gugger M, Bassetti CL. Central peri odic bre athing during sleep in acute ischemic stroke. Stroke 2007; 38(3): 1082– 1084.
21. Hanly P. Sleep disorders and end‑stage renal dise ase. Curr Opin Pulm Med 2008; 14(6): 543– 550.
22. Cheyne JA. A case of apoplexy in which the fleshy part of the he art was converted into fat. Dublin Hosp Rep 1818; 2: 216– 222.
23. Redline S. Genetics of obstructive sleep apne a. In: Kryger MH, Roth T, Dement WC (eds). Principles and practice of sleep medicine. 4th ed. Philadelphi a: Elsevi er Sa unders 2005: 1013– 1022.
24. Dostálová S, Šmahel Z, Šonka K. Srovnání cefalometrických parametrů nemocných se spánkovým apno ickým syndromem s normo u. Čas Lék čes 2000; 139(9): 272– 277.
25. Ayappa I, Rapoport DM. The upper airway in sleep: physi ology of the pharynx. Sleep Med Rev 2003; 7(1): 9– 33.
26. Rechtschaffen A, Kales A. A manu al of standardised terminology, techniques and scoring system for sleep stages in human subjects. Washington DC: Nati onal Instututes of He alth, Government Printing Office 1968. Pub No 204.
27. Šonka K, Jako ubková M, Pa ul K. Vyšetřování poruch spánku a bdění. In: Nevšímalová S, Šonka K (eds). Poruchy spánku a bdění. Praha: Galén 2007: 59– 86.
28. Jennum P, Santamari a J, Members of the Task Force. Report of an EFNS Task Force on Management of Sleep Disorders in Ne urologic Dise ase (degenerative ne urologic disorders and stroke). Eur J Ne urol 2007; 14(11): 1189– 1200.
29. EEG aro usals: scoring rules and examples: a preliminary report from the Sleep Disorders Atlas Task Force of the American Sleep Disorders Associ ati on. Sleep 1992; 15(2): 173– 184.
30. Šonka K. Měření nadměrné denní spavosti nemocných se spánkovým apno ickým syndromem a korelace s výsledky MESAM4. Cesk Slov Ne urol N 1995; 58/ 91: 236– 239.
31. Obenberger J, Šonka K, Dohnalová J. Výpočetní tomografi e horních dýchacích cest u apno iků. Čas Lék čes 1996; 135(5): 145– 149.
32. Šonka K. Syndrom neklidných noho u. 2nd ed. Praha: Jesseni us Maxdorf 2008.
33. Nevšímalová S. Narkolepsi e a hypersomni e. Cesk Slov Ne urol N 2006; 69/ 102(4): 92– 106.
34. Šonka K. Porucha chování v REM spánku. Neurol pro praxi 2008; 9(5): 297–299.
35. Příhodová I, Šonka K. Parasomni e. In:Nevšímalová S, Šonka K (eds). Poruchy spánku a bdění. Praha: Galén 2007: 209– 242.
36. Šonka K, Nevšímalová S, Nešpor E. Ne urologická onemocnění a poruchy spánku. In: Nevšímalová S, Šonka K (eds). Poruchy spánku a bdění. Praha: Galén 2007: 273– 302.
37. Příhodová I. Noční gro aning (catathreni a) – ne obvyklá parasomni e. Ne urol pro praxi 2008; 9(1): 47– 48.
38. Tkáčová R. Spánkové apnoe a ochoreni a kardi ovaskulárného systému. Praha: Galén 2006.
39. Moráň M, Kadaňka Z, Blatný M. Kvalita spánku u paci entů se syndromem spánkové apnoe a její ovlivnění léčbo u trvalým přetlakem, vztah k hypertenzní chorobě. Cesk Slov Ne urol N 2000; 63/ 96(4): 209– 214.
40. Shahar E, Whitney CW, Redline S, Lee ET. Newman AB, Javi er Ni eto F et al. Sleep disordered bre athing and cardi ovascular dise ases: cross- secti onal results of the Sleep He art He alth Study. Am J Respir Crit Care Med 2001; 163(1): 19– 25.
41. Mehra R, Benjamin EJ, Shahar E, Gottli eb DJ, Nawabit R, Kirchner HL et al. Associ ati on of nocturnal arrhythmi as with sleep- disordered bre athing: The Sleep He art He alth Study. Am J Respir Crit Care Med 2006; 173: 910– 916.
42. Kanagala R, Murali NS, Fri edman PA, Ammash NM, Gersh BJ, Ballman KV et al. Obstructive sleep apne a and the recurrence of atri al fibrillati on. Circulati on 2003; 107(20): 2589– 2594.
43. Rich S. Primary pulmonary hypertenzi on: Executive summary from the World symposi um on primary pulmonary hypertenzi on. Geneva: World He alth Organizati on 1998.
44. Salvet A, Šonka K. Obstrukční spánková apnoe a riziko cévních onemocnění mozku. Cesk Slov Ne urol N 2005; 68/ 101(5): 294– 296.
45. Bassetti CL, Milanova M, Gugger M. Sleep- disordered bre athing and acute ischemic stroke – di agnosis, risk factors, tre atment, evoluti on, and long‑term clinical o utcome. Stroke 2006; 37(4): 967– 972.
46. Vorlová T, Šonka K. Obstrukční spánková apnoe a cévní mozkové příhody. Stud Pne umol Phtise ol 2008: In press.
47. Yaggi H, Mohsenin V. Sleep apne a and stroke: a risk factor or an associ ati on? Sleep Med Clin 2007; 2: 583– 591.
48. Basta M, Vgontzas AN. Metabolic abnormaliti es in obesity and sleep apne a are in a continuum. Sleep Med 2007; 8(1): 5– 7.
49. Punjabi NM, Be aner BA. Sleep apne a and metabolic dysfuncti on. In: Kryger MH, Roth T, Dement WC (eds). Principles and practice of sleep medicine. 4th ed. Philadelphi a: Elsevi er Sa unders 2005: 1034– 1042.
50. Szabóová E, Tomori Z, Donic V, Petrovicová J, Szabó P. Sleep apnoe a inducing hypoxemi a is associ ated with e arly signs of carotid atherosclerosis in males. Respir Physi ol Ne urobi ol 2007; 155(2): 121– 127.
51. Jako ubkova M, Sonka K. Monitoring the impact of ventilati on abnormaliti es on the occurrence of interictal epileptiform patterns. Somnologi e 2003; 7: 97– 100.
52. Sonka K, Juklicková M, Pretl M, Dostalova S, Horinek D, Nevsimalova S. Seizures in sleep apne a pati ents: occurence and time distributi on. Sb Lék 2000; 101(3): 229– 232.
53. Sanders MH, Kern N. Obstructive sleep apne a tre ated by independently adjusted inspiratory and expiratory positive airway pressure vi a nasal mask. Physi ologic and clinical implicati ons. Chest 1990; 98(2): 317– 324.
54. Engleman HM, Wild MR. Improving CPAP use by pati ents with the sleep apnoe a/ hypopnoe a syndrome (SAHS). Sleep Med Rev 2003; 7(1): 81– 99.
55. Šonka K. Nové indikace modafinilu. Farmakoterapi e 2007; 3(6): 540– 541.
56. Mortimore IL, Bradley PA, Murray JA, Do uglas NJ. Uvulopalatopharyngoplasty may compromise nasal CPAP therapy in sleep apne a syndrome. Am J Respir Crit Care Med 1996; 154 (6 Pt 1): 1759– 1762.
57. Hedner J, Grote L, Zo u D. Pharmacological tre atment of sleep apnoe a: Current situ ati on and future strategi es. Sleep Med Rev 2008; 12(1): 33– 47.
58. White DP. Central sleep apne a. In: Kryger MH, Roth T, Dement WC (eds). Principles and practice of sleep medicine. 4th ed. Philadelphi a: Elsevi er Sa unders 2005: 969– 982.
59. Bradley TD, Logan AG, Kimoff RJ, Sériès F, Morrison D, Ferguson K et al. Continuo us positive airway pressure for central sleep apne a and he art failure. N Engl J Med 2005; 353(19): 2025– 2033.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2008 Issue 6
Most read in this issue
- Roztroušená skleróza mozkomíšní a magnetická rezonance: současnost a nové trendy
- Spánková apnoe dospělého věku
- Subakutně probíhající reverzibilní hypertenzní leukoencefalopatie – kazuistika
- Vyšetřování proteinu 14-3-3 v mozkomíšním moku – klinicko‑patologická korelace


