Hemangioblastom a jeho léčba pomocí Leksellova gama nože
Hemangioblastoma and its treatment using Leksell Gamma Knife
Between 1993 and 2006, 15 hemangioblastoma patients were treated at our department with the use of stereotactic radiosurgery. The group consisted of 8 men and 7 women aged between 14 and 72 years (mean age being 39 years). In 9 patients hemangioblastomas were associated with von Hippel-Lindau disease; in 6 patients sporadic hemangioblastomas were diagnosed. Solitary hemangioblastomas were detected in 6 multilocular in 9 patients, respectively. A total of 43 hemangioblastomas with a diameter ranging from 2 to 30 mm (the mean diameter being 10.7 mm) were irradiated. The mean tumour margin dose was 18.8 Gy (ranging from 9 to 22 Gy, the median being 20 Gy), the maximum dose into the tumour centre was 35.4 Gy (ranging from 20 to 44 Gy, the median being 36). For 13 patients, post-op follow-up results were obtained within 11 to 120 months (with the mean of 55 months and the median of 48 months). Stabilisation or improvement of clinical status was recorded for 10 patients, progression occurred in 3 patients (23 %). Among the irradiated tumours, 11 regressed and 14 showed no change in diameter, i.e. local control was attained in 80.6 % of tumours (25 out of the 31 controlled tumours). 6 irradiated tumours progressed (of which 2 due to solid part progression and 4 due to cystic part progression: stereotactic punction was performed in 3 and open neurosurgery in 1 of the 4 tumours, respectively). One patient died of extracranial organ complications associated with von Hippel-Lindau disease. Radiosurgical treatment of hemangioblastomas proved effective in patients with both solitary and multiloculary small or middle size hemangioblastomas, with a good clinical response and a low risk of complications.
Key words:
hemangioblastoma – von Hippel-Lindau disease – Leksell Gamma Knife – radiosurgery
:
J. Valchář; R. Liščák; G. Šimonová; J. Vymazal
:
Oddělení stereotaktické a radiační neurochirurgie, Nemocnice Na Homolce, Praha
:
Cesk Slov Neurol N 2008; 71/104(2): 216-222
:
Short Communication
V letech 1993–2006 bylo na našem pracovišti léčeno 15 pacientů s hemangioblastomem prostřednictvím radiochirurgického zákroku Leksellovým gama nožem. Soubor tvořilo 8 mužů a 7 žen ve věku 14–72 let (průměr 39 let). U 9 pacientů šlo o hemangioblastomy asociované s von Hippel-Lindauovou chorobou, u 6 pacientů o hemangioblastomy sporadické. U 6 nemocných se jednalo o hemangioblastom solitární, u 9 o vícečetné. Celkem bylo ozářeno 43 ložisek o průměru 2–30 mm (průměr rozměrů ložisek 10,7 mm). Aplikovaná dávka ionizujícího záření na periferii byla v průměru 18,8 Gy (rozmezí 9–22 Gy, medián 20 Gy), maximální dávka do centra tumoru byla v průměru 35,4 Gy (rozmezí 20–44 Gy, medián 36). Kontrolní vyšetření s odstupem 11–120 měsíců (průměr 55 měsíců, medián 48 měsíců) mělo 13 pacientů. U 10 pacientů byla zaznamenána stabilizace nebo zlepšení klinického stavu, u 3 nemocných došlo k jeho progresi (23 %). 11 ozářených ložisek zregredovalo, 14 ozářených ložisek bez změn ve velikosti, tzn. u 80,6 % ložisek (25 z 31 kontrolovaných ložisek) bylo dosaženo lokální kontroly. 6 tumorů zprogredovalo (2 ložiska progrese solidní složky, 4 ložiska progrese složky cystické – u 3 provedena stereotaktická aspirace obsahu cysty, 1 vyžadovalo mikrochirurgickou resekci). 1 pacient zemřel 8 let po radiochirurgické léčbě na extrakraniální orgánové komplikace související s von Hippel-Lindauovou nemocí. Radiochirurgická léčba u hemangioblastomů se ukázala být jako vhodná a efektivní pro pacienty se solitárními, ale i vícečetnými hemangioblastomy malé a střední velikosti s dobrou klinickou odpovědí a s nízkým rizikem komplikací.
Klíčová slova:
hemangioblastom, von Hippel-Lindauova nemoc – Leksellův gama nůž – radiochirurgická léčba
Úvod
Hemangioblastom (HGB), též angioretikulom nebo Lindaův nádor, je benigní tumor s převažujícím výskytem v CNS. Jedná se o tumor poměrně vzácný, ve skupině všech mozkových nádorů je zastoupen asi 1–2,5 % [1].
Hemangioblastom se vyskytuje buď sporadicky (asi v 80 %) nebo ve spojitosti s von Hippel-Lindauovou chorobou (VHL). VHL je autosomálně dominantní onemocnění s incidencí přibližně 1/36 000. Je způsobeno defektem tumor supresorového genu VHL (dosud je identifikováno asi 300 různých mutací) lokalizovaného na chromozomu 3p26-p25. Ztráta produktu genu VHL (proteinu VHL) může následně vést k tomu, že v normoxických podmínkách dojde ke zvýšené expresi hypoxií indukovaných proteinů (jako je například vascular endothelial growth factor – VEGF), o čemž vypovídá i hypervaskularizace tumorů asociovaných s VHL. Pro VHL je typická přítomnost mnohočetných hemangioblastomů v oblasti mozku, míchy nebo sítnice. Dalším charakteristickým rysem této choroby je výskyt cystického postižení parenchymatózních orgánů (ledviny, pankreas, játra), u nemocných je možné také laboratorně zachytit polyglobulii v důsledku nadprodukce erytropoetinu buňkami tumoru. Pacienti s VHL predisponují též k vyššímu výskytu feochromocytomu a karcinomu ledvin, proto je nutné u těchto nemocných důsledně provádět screeningová vyšetření (ultrazvuk břišních orgánů je doporučován minimálně 1 až 2krát za rok) se zaměřením na postižení těmito zhoubnými tumory. Pokud je pozitivní rodinný výskyt hemangioblastomu v oblasti retiny anebo centrální nervové soustavy, k diagnóze VHL onemocnění postačuje průkaz 1 ložiska hemangioblastomu a 1 viscerální léze [2]. Bez rodinného výskytu je k diagnóze postačující průkaz 2 a více hemagioblastomů anebo 1 hemangioblastomu a 1 viscerální léze [3].
Vzhledem k tomu, že VHL patří k onemocněním s predispozicí ke zvýšenému výskytu zhoubných nádorů, stala se dnes DNA analýza (stejně tak jako screeningová vyšetření) součástí klinické praxe a genetické testování u VHL se běžně provádí. Mimo jiné i díky molekulární diagnostice VHL se mění i celková léčebná strategie tohoto onemocnění [4–10].
Hemangioblastom CNS je nejčastěji lokalizován v mozečku, zvláště pak jedná-li se o hemangioblastom sporadický. Dále, zejména u pacientů s VHL, se může nacházet v mozkovém kmeni, míše, ale i supratentoriálně (poměrně vzácně). Jedná se převážně o tumor solidní, může být též tvořen cystou se stěnou složenou z vrstvy astroglie a drobným angiomem umístěným na stěně cysty. Pokud jde o diagnostiku, v případě VHL se může jednat o náhodný nález při screeningu pacientů s prvotními příznaky mimo centrální nervový systém. U sporadických forem je pak spektrum klinických příznaků širší. Při obvyklé lokalizaci v zadní jámě jsou dominantními příznaky vertigo, cefalea (někdy z rychlého nárůstu nitrolební hypertenze), poruchy taxe [8,9,11–14].
Vhodnou zobrazovací metodou hemangioblastomu, je kombinace vyšetření magnetickou rezonancí (MRI) spolu s angiografickým vyšetřením (DSA). Na MRI se hemangioblastom zobrazuje jako expanzivní, cystické ložisko s nidem solidní tkáně uvnitř cysty, který výrazně zvyšuje signál po aplikaci kontrastní látky. Obecně platí, že nádor je nejprve drobnější a solidní se sytým postkontrastním zvýrazněním. Později se vytváří cystická složka s typicky sníženou intenzitou signálu na T1 vážených obrazech a vysokým signálem na T2 vážení. Je-li hemangioblastom solidní, pak je někdy obtížné jej odlišit od jiného patologického procesu, a proto je vhodné doplnit ještě angiografické vyšetření, na kterém se typicky zobrazuje hypervaskularizovaný nádorový nidus [15,16].
Materiály a metody
Léčba pacientů s hemangioblastomy se uskutečnila od 2/1993 do 11/2006 na oddělení stereotaktické a radiační neurochirurgie Nemocnice Na Homolce v Praze Leksellovým gama nožem model C (Elekta Instruments AB, Stockholm). K hlavě pacientů byl nejdříve připevněn v lokální anestezii stereotaktický rám. Poté se pacienti podrobili centračním zobrazovacím metodám. U většiny pacientů byla jako plánovací centrační metoda použita MRI (13 nemocných MRI, u 2 CT). Snímky pořízené touto metodou byly následně prostřednictvím interní počítačové sítě přeneseny do plánovacího softwaru.
Soubor pacientů
Radiochirurgické léčbě Leksellovým gama nožem se podrobilo 15 pacientů (tab. 1). Soubor tvořilo 8 mužů a 7 žen, věkové rozmezí pacientů bylo 14–72 let (průměrný věk 39 let). U 9 pacientů šlo o hemangioblastomy asociované s von Hippel-Lindauovou chorobou, u 6 pacientů se jednalo o hemangioblastomy sporadické. U 6 nemocných se jednalo o HGB solitární, u 9 o vícečetné. 11 pacientů se před radiochirugickým zákrokem podrobilo neurochirurgickému výkonu otevřenému, 1 z nich prodělal též zevní frakcionovanou radioterapii. U 4 pacientů bylo ozáření gama nožem primárním způsobem léčby (u 1 z těchto nemocných se jednalo o retinální HGB a indikace k radiochirurgické léčbě byla zvolena po dohodě s oftalmology, 2 pacienti byli kontraindikováni k otevřenému zákroku pro nevhodnou lokalizaci ložisek v mozkovém kmeni nebo v jeho bezprostřední blízkosti, poslední pacient byl primárně doporučen k ozáření na základě podrobného diagnostického vyšetření včetně MRI a DSA s typickým obrazem pro hemangioblastom).
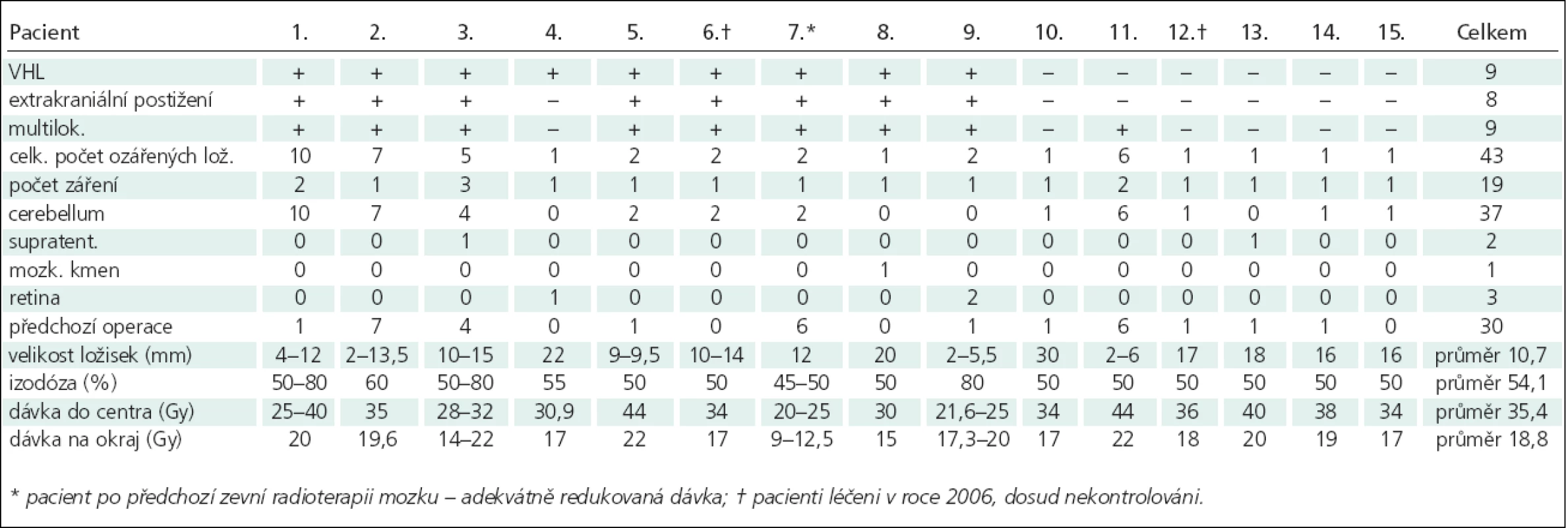
Celkem bylo ozářeno 43 ložisek (32 solidních, 11 cystických), o průměrech v rozmezí od 2–30 mm (průměrný rozměr ložisek 10,7 mm). Aplikované dávky ionizujícího záření se na periferii objevovaly v průměru 18,8 Gy (v rozmezí 9–22 Gy, medián 20 Gy) na 45–80 % (průměr 54,1 %, medián 50 %) izodózy, maximální dávky do centra tumoru se pohybovaly v průměru 35,4 Gy (v rozmezí 20–44 Gy, medián 36 Gy). Pro volbu dávky je určující objem nádoru, jeho histologický typ, vzdálenost od případných okolních kritických struktur a případná předchozí radioterapie.
Klinické příznaky
37 z 43 ozařovaných ložisek (86 %) bylo lokalizováno cerebellárně, 1 se nacházelo v mozkovém kmeni, 2 supratentoriálně. U 2 pacientů (3 ložiska) byly ozářeny retinální hemangioblastomy.
- VHL. U 9 pacientů s VHL, kteří byli léčeni na našem pracovišti, přicházelo 8 s anamnestickými údaji poukazujícími na extracerebrální postižení. U všech těchto nemocných bylo detekováno postižení jiných orgánů (pankreas, ledvina, mícha, retina). U 2 pacientů se jednalo o retinální hemangioblastomy, u jednoho z nich se klinicky objevilo zhoršení vízu levého oka, u druhého rozmazané vidění spolu s přetrvávajícím vertigem a instabilitou z dob z předchozího postižení mozečku. U 5 nemocných s VHL byla ozářena pouze cerebellární ložiska, 1 z nich byl asymptomatický (odhaleno v rámci screeningového vyšetření mozku), u 4 zbývajících dominovaly v pořadí tyto příznaky: cefalea, instabilita, vertigo, ataxie. Co se týče 2 zbývajících pacientů s VHL, u jednoho z nich byl léčen tumor lokalizovaný v oblasti prodloužené míchy, klinicky u nemocného dominovaly příznaky související s postižením orgánů mimo centrální nervový systém (bolesti břicha, zvracení) a ložisko bylo odhaleno v rámci screeningového vyšetření mozku, u dalšího nemocného byla léčena cerebellární ložiska spolu s tumorem lokalizovaným supratentoriálně, klinicky se manifestující úpornou cefaleou.
- Sporadický HGB. 5 z celkového počtu 6 pacientů se sporadickým HGB se v minulosti podrobilo otevřenému neurochirurgickému výkonu. U 3 z nich bylo ozařováno reziduum tumoru, u 1 se objevila recidiva a u 1 nemocného šlo o nález nový. Zbývající 1 pacient, který nebyl v minulosti léčen, byl diagnostikován na základě objevení klinických příznaků (prekolapsové stavy, vertigo, pády) a následně provedeném diagnostickém vyšetření magnetickou rezonancí a vyšetření angiografickém s typickým obrazem pro hemangioblastom. Klinické příznaky u pacientů léčených se sporadickým HGB korelovaly s lokalizací patologických ložisek. U 5 pacientů se jednalo o cerebellární HGB (u 4 z nich odpovídal neurologický nález mozečkové symptomatologii – v pořadí: cefalea, vertigo, nestabilita s pády, ataxie, zvracení, jeden z těchto nemocných byl asymptomatický a diagnostikován byl v rámci pooperačního kontrolního vyšetření). U zbývajícího 1 pacienta se supratentoriálně lokalizovaným HGB byla zaznamenána progrese pravostranné hemiparézy, alterace chůze, zárazy řeči.
Výsledky
Kontrolní vyšetření s odstupem 11–120 měsíců (průměr 55 měsíců, medián 48 měsíců) mělo 13 pacientů. 4 vykazovali známky klinického zlepšení, u 6 byl klinický nález stabilní. U 3 nemocných (23 %) jsme zaznamenali progresi klinického stavu (u 2 kvůli progresi cystické složky tumoru, u 1 pak kvůli progresi solidní části ložiska). Kolaterální edém se při kontrolních vyšetřeních objevil u 3 pacientů v rozmezí 3, 7 a 11 měsíců po ozáření a vyžádal si u všech nemocných antiedematózní terapii kortikoidy. K radionekróze nedošlo u žádného pacienta. Vzhledem k tomu, že ke kolaterálnímu otoku došlo u 3 ložisek z 31 sledovaných, představuje riziko této komplikace 10 %. 1 pacient zemřel 8 let po radiochirurgické léčbě na orgánové komplikace spojené s VHL. Nová ložiska se v průběhu kontrolních vyšetření objevila u 5 pacientů v rozmezí 2–60 měsíců po léčbě (průměr 22,5 měsíců, medián 19 měsíců). 4 z nich byli nemocní s VHL, 1 se sporadickým HGB.
Velikost ložisek
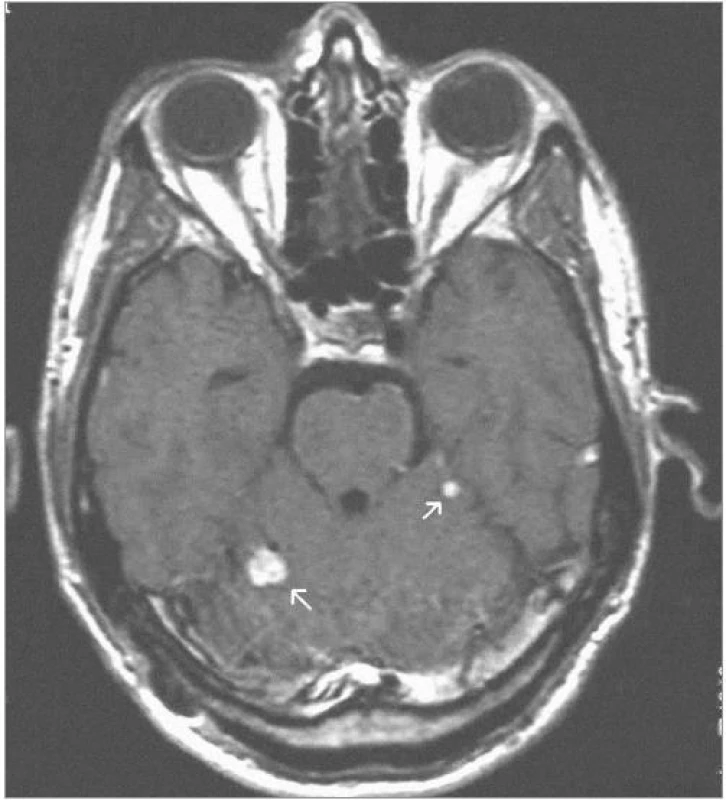
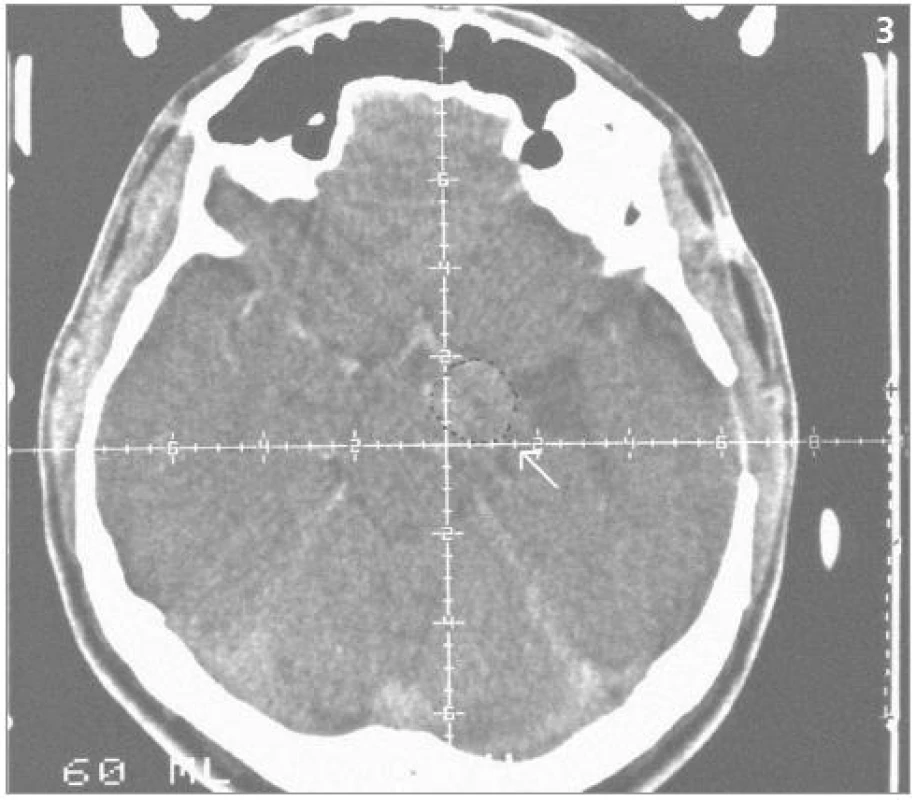
11 ozářených ložisek zregredovalo (obr. 1 a 2), 14 ozářených ložisek bylo bez změn ve velikosti, tzn. u 25 z 31 kontrolovaných ložisek, tedy u 80,6 % ložisek, bylo dosaženo lokální kontroly. 6 ložisek zprogredovalo: 2 ložiska vykazovala známky progrese solidní složky tumoru. U 4 ložisek (obr. 3–5) byla detekována progrese složky cystické, u 3 z nich byla provedena stereotaktická aspirace obsahu cysty s tím, že u 2 takto invazivně léčených ložisek byla v průběhu následujících kontrolních vyšetření zaznamenána lokální kontrola růstu. 1 takto zprogredované ložisko vyžadovalo otevřený mikrochirurgický zákrok.
Obrazová část I. – Pacient s vícečetnými hemangioblastomy zadní jámy lební léčenými radiochirurgickým zákrokem Leksellovým gama nožem.
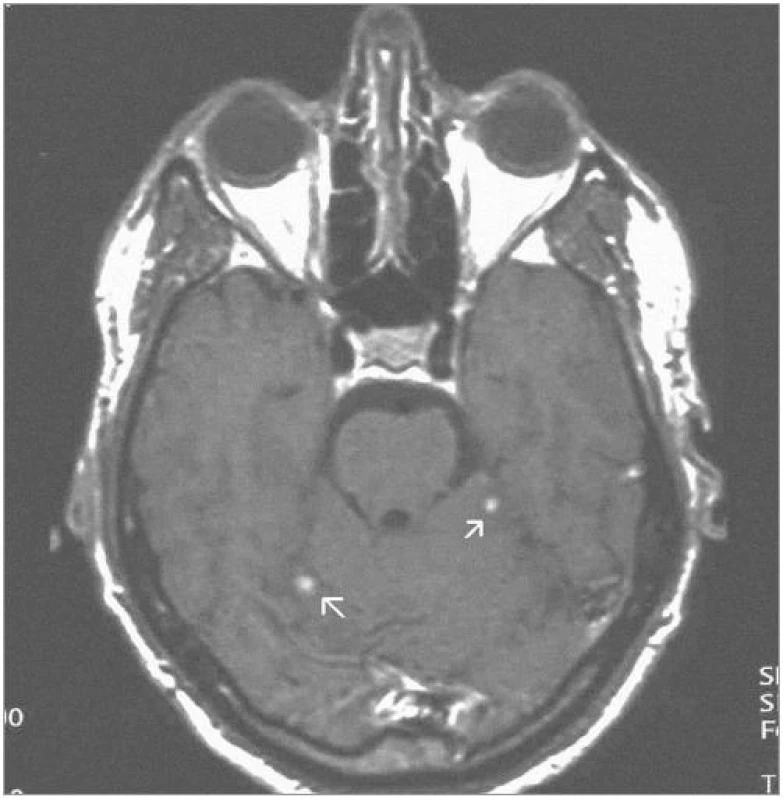
Obrazová část II. – Pacient s hemangioblastomem temporálně vlevo v blízkosti III. komory léčeným radiochirurgickým zákrokem Leksellovým gama nožem s detekovanou progresí cystické části tumoru a s její následnou stereotaktickou punkcí.
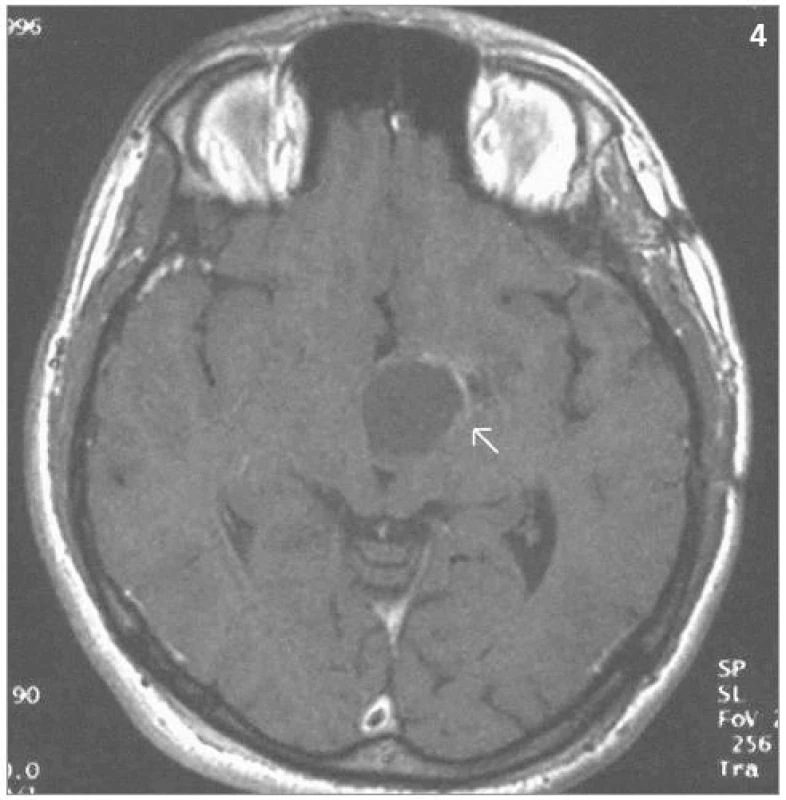
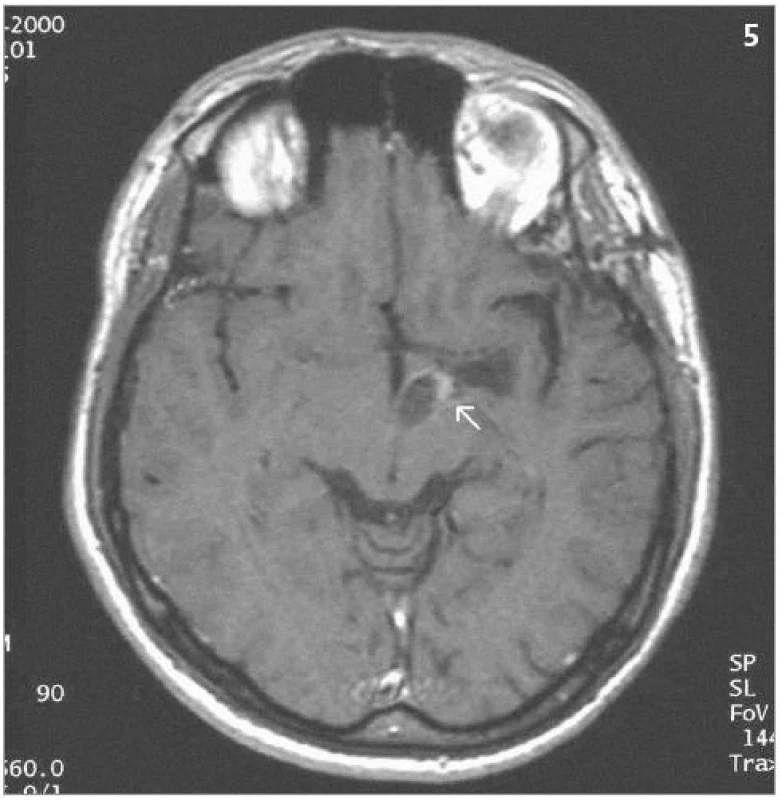
Diskuse
Chirurgický otevřený výkon, jehož cílem je odstranění tumoru (totální resekce), je (u solitárních hemangioblastomů) metodou kurativní. Mikrochirurgická technika umožňuje obvykle totální exstirpaci tumoru, zejména u cystických forem [8]. Úspěch léčby však záleží na lokalizaci tumoru, jeho velikosti, přítomnosti cysty a charakteru vaskularizace (solidní hemangioblastomy může být obtížné takto léčit právě pro jejich hypervaskularizaci) [14,17]. Jinak je tomu u vícečetných hemangioblastomů. Pacient s VHL je obtížně léčitelný vzhledem k možné přítomnosti většího počtu ložisek v mozku a častým objevením ložisek nových. Nezřídka je takový pacient operován opakovaně s kumulativním rizikem výskytu komplikací, jako je krvácení, infekce, či rizika spojenýma s užitím celkové anestezie. Stavy spojené například s hydrocefalem a známkami nitrolební hypertenze, stejně tak jako ložiska větších rozměrů, jsou operovány bezodkladně.
Za další možný terapeutický zásah lze považovat předoperační endovaskulární embolizaci solidní části tumoru [18,19], která může vést dle některých autorů k redukci vaskularizace tumoru a následnému snížení krevních ztrát v průběhu jeho resekce. Právě u vysoce vaskularizovaných či větších tumorů je nutné zohlednit riziko krvácení. Jsou uváděny i příklady spontánního krvácení z ložiska. Zakrvácení z ložiska je možné, ale jeho pravděpodobnost je uváděna jako poměrně nízká. U tumorů pod 1,5 cm je riziko spontánní hemoragie v podstatě minimální. Ve studii zabývající se rizikem krvácení z hemangioblastomů byla u 277 pacientů s HGB v CNS zaznamenáno 7 případů spontánního krvácení. Jako průměrná hodnota rozměrů ložisek se zaznamenaným krvácením byl uváděn průměr 3 cm. Ač je riziko spontánního krvácení nízké, přesto je nutné na tuto komplikaci myslet zejména u tumorů větších rozměrů [20].
Co se týče radiochirurgického zákroku, jeví se tento způsob léčby vhodný pro pacienty s vícečetnými hemangioblastomy, protože v průběhu 1 procedury lze zaléčit i několik ložisek najednou. I když je po radiochirurgické léčbě dosaženo kontroly růstu u většiny hemangioblastomů, prognóza pacientů zejm. s VHL syndromem často závisí na progresi projevů onemocnění mimo centrální nervový systém (karcinom ledviny je některými autory uváděn jako hlavní příčina smrti u pacientů s VHL) či progresi nových intrakraniálních ložisek [8,21]. Zákrok gama nožem je možné také indikovat u ložisek lokalizovaných v elokventních oblastech CNS. Tumory větších rozměrů (zhruba nad 3 cm) však pro tuto metodu nejsou vhodné. Horší výsledky byly zaznamenány při radiochirurgické léčbě u objemnějších ložisek, u kterých byla s ohledem na větší rozměr aplikována nižší dávka [22]. Problematické mohou být také objemné cysty u cystických hemangioblastomů. V takovém případě je u některých pacientů možná stereotaktická aspirace cystického obsahu a iradiace kolabované stěny cysty. Pokud jde o komplikace, je radiochirurgický zákrok zatížen rizikem vzniku poradiačního kolaterálního edému asi u 10 % ozařovaných ložisek. V případě výskytu takové komplikace, jako je kolaterální edémová reakce, je možné použít antiedematózní terapii kortikoidy, která ve většině případů vykazuje příznivý léčebný efekt bez nutnosti řešit tuto komplikaci otevřenou operací.
Otevřená operace a radiochirurgický zákrok se mohou také vzájemně kombinovat. Např. u vysoce vaskularizovaných tumorů lze provést předoperační ozáření ložiska, zabránit jeho další progresi a docílit redukce jeho vaskularizace, a tím snížit riziko peroperačního krvácení při následném otevřeném zákroku [23] (na našem pracovišti tento způsob léčby nebyl aplikován). Úspěšně lze také ozářit pooperační rezidua tumoru či recidivy v původně operované oblasti.
Výsledky jiných pracovišť aplikovaných radiochirurgický zákrok k léčbě hemangioblastomů poukazují na možnost využití této alternativy. Jawahar et al uvádějí soubor 27 pacientů s hemangioblastomy CNS léčených Leksellovým gama nožem. U 16 pacientů z 21 sledovaných přeživších (2 pacienti zemřeli na onemocnění srdce, 4 v důsledku progrese ložisek) byl neurologický nález stabilní nebo zlepšen. U 5 došlo ke zhoršení klinického stavu (u 3 v důsledku progrese cystické části tumoru, u 2 v důsledku progrese míšních ložisek) [24]. Wang et al popisují soubor 35 pacientů s hemangioblastomy léčených gama nožem. U 21 z 29 (72 %) kontrolovaných přeživších pacientů bylo dosaženo stabilizace nebo zlepšení klinického nálezu. U 8 pacientů zapříčinilo zhoršení klinických příznaků zvětšení cystické složky nebo se objevila ložiska nová [25]. Park et al popisují soubor 9 pacientů léčených gama nožem. Celkem bylo léčeno 84 hemangioblastomů, u 81 z nich bylo dosaženo lokální kontroly [26], Niemela et al zmiňují soubor 10 pacientů s 11 hemangioblastomy léčených gama nožem. U 10 ložisek bylo dosaženo lokální kontroly [27]. Patrice a spol. popisují léčbu 38 hemangioblastomů pomocí gama nože nebo lineárního urychlovače s dosažením stabilního nebo zlepšeného neurologického nálezu u 78 % přeživších pacientů [28]. Chang et al zaznamenali léčbu 29 HGB u 13 pacientů pomocí lineárního urychlovače. 1 léčený tumor zprogredoval, 5 tumorů zmizelo, 16 vykazovalo známky regrese a 7 bylo v průběhu kontrolních vyšetření bez změn ve velikosti. 1 pacient zemřel v důsledku progrese neléčeného HGB v míše, u 3 pacientů se objevila poradiační nekróza. Celkově u 5 léčených pacientů (z 9 nemocných, jejichž příznaky korelovaly s lokalizací ložisek) bylo zaznamenáno zlepšení jejich klinického stavu [29].
Conway et al popisují léčbu 40 pacientů s 61 HGB CNS otevřeným neurochirurgickým zákrokem. Úprava klinických příznaků nebo zástava progrese ložisek byla zaznamenána u 88 % pacientů [30]. Smrčka et al popisují léčbu 8 pacientů (2 pacienti s VHL), u 7 z nich byl proveden radikální chirurgický zákrok a tumor byl totálně exstirpován, u 1 byla indikována iradiace pomocí lineárního urychlovače. Všichni pacienti byli po prodělané léčbě v dobrém klinickém stavu (střední doba sledování 1 rok) [8].
Jako další možný způsob léčby je mimo jiné popisován i antiangiogenický konzervativní způsob léčby užitý u hemangioblastomů míchy. Podstatou této léčby je specifická inhibice růstových faktorů, zejm. VEGF (vascular endothelial growth factor), které jsou považovány za hlavní patogenetické faktory při vzniku hemangioblastomů u pacientů s mutací genu VHL při von Hippel-Lindauově chorobě [31].
Závěr
Radiochirurgická léčba hemangioblastomů pomocí Leksellova gama nože se ukázala být jako vhodná léčebná modalita, a to zejména u HGB malých až středních rozměrů (do 3 cm) s lokální kontrolou růstu tumoru v 80,6 % a klinickou úpravou v 77 % případů. Radiochirurgický zákrok je možné zvážit jako primární metodu zejména tam, kde se jedná o vícečetné postižení mozku, rozměry tumorů nepřesahují indikační kritéria a je předpoklad častých recidiv (VHL). Možná je kombinace radiochirurgie se zákrokem otevřeným. Komplikace radiochirurgické léčby byly pozorovány u 10 % iradiovaných ložisek s pozitivní reakcí na antiedematózní terapii kortikoidy. Vzhledem k mnohočetnému výskytu hemangioblastomů u pacientů s VHL se radiochirurgický zákrok u těchto nemocných ukazuje jako vhodná metoda s ohledem na fakt, že lze ozářit více ložisek během 1 procedury a ev. ji opakovat v případě odhalení ložisek nových.
doc. MUDr. Roman Liščák, CSc.
Oddělení stereotaktické a radiační neurochirurgie
Nemocnice Na Homolce
Roentgenova 2
150 30 Praha 5
Roman.Liscak@homolka.cz
Přijato k recenzi: 9. 7. 2007
Přijato do tisku: 13. 2. 2008
Sources
1. Jeffreys R. Clinical and surgical aspects of posterior fossa haemangioblastoma. J Neurol Neurosurg Psychiatry 1975; 38: 105–111.
2. Melmon KL, Rosen SW. Lindau's disease. Review of the literature and study of a large kindred. Am J Med 1964; 36: 595–617.
3. Wanebo JE, Lonser RR, Glenn GM, Oldfield EH. The natural history of hemangioblastomas of the central nervous system in patients with von Hippel–Lindau disease. J Neurosurg 2003; 98: 82–94.
4. Neumann HPH, Berger DP, Sigmund G, Blum U, Schmidt D, Parmer RJ et al. Phaeochromocytomas, multiple endocrine neoplasia type 2, and von Hippel-Lindau disease. N Engl J Med 1993; 329: 1531–1538.
5. Křepelová A. Dědičné formy nádorů ledvin – spektrum predispozičních genů a jejich testování. Klinická onkologie 2006; 19(Suppl): 82–84.
6. Lonser RR, Glenn GM, Walther M, Chew EY, Libutti SK, Linehan WM et al. Von Hippel-Lindau disease. Lancet 2003; 361: 2059–2067.
7. Richard S, David P, Marsot-Dupuch K, Giraud S, Béroud C, Resche F. Central nervous system hemangioblastomas, endolymphatic sac tumors, and von Hippel–Lindau disease. Neurosurg Rev 2000; 23: 1–22.
8. Smrcka M, Smrcka V. Central nervous system hemangioblastoma: its role in von Hippel-Lindau disease. Bratisl Lek listy 2000; 101: 503–506.
9. Kozler P, Kramář F. Von Hippelova-Lindauova choroba a kapilární hemangioblastom. In: Kozler P et al. Intrakraniální nádory. Praha: Galén 2007: 177–179.
10. Catapano D, Muscarella LA, Guarnieri V, Zelante L, D'Angelo VA, D'Agruma L. Hemangioblastomas of central nervous system: molecular genetic analysis and clinical management. Neurosurg 2005; 56: 1215–1221.
11. Neumann HP, Eggert HR, Weigel K, Friedburg H, Wiestler OD, Schollmeyer P. Hemangioblastomas of the central nervous system. A 10-year study with special reference to von Hippel-Lindau syndrome. J Neurosurg 1989; 70: 24–30.
12. Chakraborti PR, Chakrabarti KB, Doughty D, Plowman PN. Stereotactic multiple are therapy. IV-Haemangioblastoma. Br J Neurosurg 1997; 11: 110–115.
13. Richard S, Campello C, Taillandier L, Parker F, Resche F. Haemangioblastoma of the central nervous system in von Hippel-Lindau disease. French VHL Study Group. J Intern Med 1998; 243: 547–553.
14. Slavin KV. Hemangioblastoma. eMedicine Specialties [online]; last revision 13th of April 2006. Dostupné z <http://www.emedicine.com/med/topic2991.htm>.
15. Filling-Katz MR, Choyke PL, Patronas NJ, Gorin MB, Barba D, Chang R et al. Radiologic screening for von Hippel-Lindau disease: the role of Gd-DTPA enhancened MR imaging of the CNS. J Comput Assist Tomogr 1989; 13: 743–755.
16. Vymazal J. Ostatní nádory mozkových obalů. In: Vymazal J. Magnetická rezonance nervové soustavy. Radiologické a klinické aspekty. I. Mozkové nádory. Praha: M-DIAG Publishing 2006: 109–112.
17. Dow GR, Sim DW, O'Sullivan MG. Excision of large solid haemangioblastomas of the cerebellopontine angle by a skull base approach. Br J Neurosurg 2002; 16: 168–171.
18. Eskridge JM, McAuliffe W, Harris B, Kim DK, Scott J, Winn HR. Preoperative endovascular embolization of craniospinal hemangioblastomas. AJNR Am J Neuroradiol 1996; 17: 525– 531.
19. Takeuchi S, Tanaka R, Fujii Y, Abe H, Ito Y. Surgical treatment of hemangioblastomas with presurgical endovascular embolization. Neurol Med Chir (Tokyo) 2001; 41: 246–251.
20. Gläsker S, Van Velthoven V. Risk of hemorrhage in hemangioblastomas of the central nervous system. Neurosurgery 2005; 57: 71–76.
21. Rajaraman C, Rowe JG, Walton L, Malik I, Radatz M, Kemeny AA. Treatment options for von Hippel-Lindau's haemangioblastomatosis: the role of gamma knife stereotactic radiosurgery. Br J Neurosurg 2004; 18: 338–342.
22. Georg AE, Lunsford LD, Kondziolka D, Flickinger JC, Maitz A. Hemangioblastoma of the posterior fossa. The role of multimodality treatment. Arq Neuropsiquiatr 1997; 55: 278–286.
23. Kamitani H, Hirano N, Takigawa H, Yokota M, Miyata H, Ohama E et al. Attenuation of vascularity by preoperative radiosurgery facilitates total removal of a hypervascular hemangioblastoma at the cerebello-pontine angle: case report. Surg Neurol 2004; 62: 238–243.
24. Jawahar A, Kondziolka D, Garces YI, Flickinger JC, Pollock BE, Lunsford LD. Stereotactic radiosurgery for hemangioblastoma of the brain. Acta Neurochirurg (Wien) 2000; 142: 641–645.
25. Wang EM, Wang BJ, Zhang N, Pan L, Dong YF, Zhou LF et al. Analysis of the results of gamma knife radiosurgery for hemangioblastomas of the brain and the factors related to the tumor recurrence. Zhonghua Yi Xue Za Zhi 2004; 84: 813–817.
26. Park YS, Chang JH, Chang JW, Chung SS, Park G. Gamma knife surgery for multiple hemangioblastomas. J Neurosurg 2005; 102(Suppl): 97–101.
27. Niemelä M, Lim YJ, Söderman M, Jääskeläinen J, Lindquist C. Gamma knife radiosurgery in 11 hemangioblastomas. J Neurosurg 1996; 85: 591–596.
28. Patrice SJ, Sneed PK, Flickinger JC, Shrieve DC, Pollock BE, Alexander E et al. Radiosurgery for hemangioblastoma: results of a multiinstitutional experience. Int J Radiat Oncol Biol Phys 1996; 35: 493–499.
29. Chang SD, Meisel JA, Hancock SL, Martin DP, McManus M, Adler JR jr. Treatment of hemangioblastomas in von Hippel-Lindau disease with linear accelerator-based radiosurgery. Neurosurgery 1998; 43: 28–34.
30. Conway JE, Chou D, Clatterbuck RE, Brem H, Long DM, Rigamonti D Hemangioblastomas of the central nervous system in von Hippel-Lindau syndrome and sporadic disease. Neurosurgery 2001; 48: 55–62.
31. Schuch G, de Wit M, Höltje J, Laack E, Schilling G, Hossfeld DK et al. Case 2. Hemangioblastomas: diagnosis of von Hippel-Lindau disease and antiangiogenic treatment with SU5416. J Clin Oncol 2005; 23: 3624–3626.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2008 Issue 2
Most read in this issue
- Multiple sclerosis
- Hemangioblastoma and its treatment using Leksell Gamma Knife
- Treatment Results of Low-Grade Gliomas in Children (a Retrospective Data Analysis)
- Smith-Magenis syndrome: a case report
